Kỹ sư CNSH Cao Vân Anh, Ths. Nguyễn Thị Liên Thi
Đơn vị HTSS IVFMD FAMILY, BVĐK Gia Đình, Đà Nẵng
Giới thiệu
Một trong những khó khăn thường gặp khi tìm kiếm tinh trùng trong các mẫu tinh trùng sau thủ thuật là sự hiện diện dày đặc của các tế bào hồng cầu. Việc xác định tinh trùng trong các cụm hồng cầu này không chỉ tốn nhiều thời gian mà còn làm giảm tỷ lệ thu hồi. Để khắc phục vấn đề này, Verheyen và cộng sự (1995) là những người đầu tiên mô tả việc sử dụng dung dịch ly giải hồng cầu (Erythrocyte lysing buffer- ELB) nhằm loại bỏ hồng cầu trong các mẫu mô tinh hoàn ở bệnh nhân vô tinh do tắc (obstructive azoospermia-OA) và vô tinh không do tắc (non-obstructive azoospermia-NOA) [1]. Tuy nhiên, thời gian tiếp xúc kéo dài giữa tinh trùng và ELB có thể ảnh hưởng bất lợi đến tính toàn vẹn màng tế bào và cấu trúc nhiễm sắc thể, từ đó làm suy giảm chất lượng tinh trùng trong quá trình xử lý mẫu [1],[2]. Do đó, việc đánh giá hiệu quả và giới hạn của dung dịch ly giải hồng cầu (ELB) trong xử lý mẫu tinh hoàn thu được từ thủ thuật trở nên cần thiết nhằm tối ưu hóa quy trình trích xuất tinh trùng và nâng cao hiệu quả của kỹ thuật hỗ trợ sinh sản.
Nguyên lý
Dung dịch ELB ly giải hồng cầu thông qua cơ chế phá vỡ cân bằng amoni (NH₄⁺), trong đó protein vận chuyển anion Band 3 đóng vai trò là kênh trung gian chính. Band 3 là một protein trao đổi ion Cl⁻/HCO₃⁻ nằm trên màng hồng cầu, có chức năng duy trì cân bằng điện giải và pH nội bào. Khi cơ chế này bị phá vỡ, áp lực thẩm thấu tăng, dẫn đến vỡ màng hồng cầu. Đáng chú ý, các kênh trao đổi Band 3 tương tự cũng được phát hiện trên màng tinh trùng. Do đó, tinh trùng có thể bị ảnh hưởng tương tự khi tiếp xúc với ELB, đặc biệt trong điều kiện ủ kéo dài, có thể gây tổn thương màng tế bào và rối loạn cân bằng nội bào. Các bằng chứng gần đây cũng cho thấy việc tiếp xúc ELB có thể làm tăng phân mảnh DNA và rối loạn cấu trúc chromatin của tinh trùng [2].
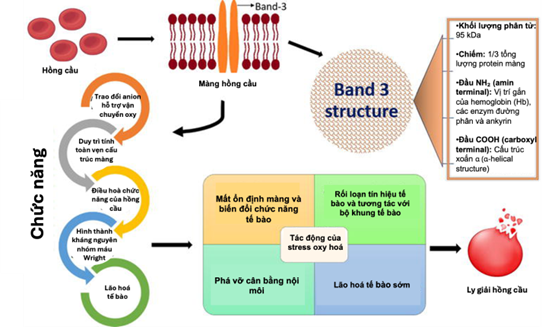
Hình 1. Cấu trúc và chức năng của kênh trao đổi band 3 trên màng hồng cầu [3]
Quy trình thực hiện
Sau khi thu nhận mẫu tinh hoàn từ phòng thủ thuật, đối với mẫu PESA, có thể xử lý bằng cách rửa đơn giản hoặc ly tâm gradient nồng độ. Với mẫu TESE/mTESE, mô tinh hoàn được xé nhuyễn cơ học để giải phóng tinh trùng. Trong trường hợp mẫu còn nhiễm nhiều hồng cầu, có thể pha loãng và ly tâm với 2 mL dung dịch ly giải hồng cầu (ELB). Lực và thời gian ly tâm cần được kiểm soát cẩn thận để tránh tổn thương khả năng di động của tinh trùng. Huyền phù cặn được trộn với 2,0 mL ELB và ủ ở nhiệt độ phòng trong 10 phút, sau đó ly tâm ở 300g trong 5 phút, loại bỏ phần dịch nổi và huyền phù lại phần cặn trong 0,2 mL môi trường nuôi cấy có đệm HEPES [4],[5].
Chuẩn bị dung dịch ELB: Pha 155 mM NH₄Cl (Merck), 10 mM KHCO₃ (Merck, Đức), và 2 mM EDTA vào nước vô trùng, điều chỉnh pH = 7,2, lọc qua màng 0,22 µm và bảo quản ở 4°C [4], [5].

Hình 2. Hình ảnh minh hoạ loại bỏ hồng cầu bằng cách sử dụng dung dịch ly giải hồng cầu. (A) Cặn tế bào trước khi ly giải (B) cặn tế bào sau khi ly giải [6]
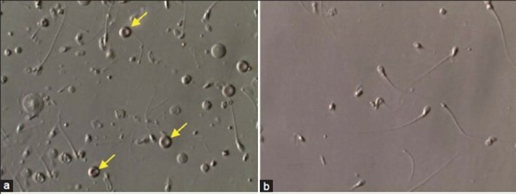
Hình 3. Ảnh chụp hiển vi cho thấy mô hình tổng thể của các mẫu mào tinh hoàn thu được bằng phương pháp hút tinh trùng từ mào tinh hoàn qua da (PESA) [4]
(a) Mẫu thô cho thấy sự nhiễm bẩn của các mảnh vụn và hồng cầu (mũi tên vàng). (b) Mẫu đã được xử lý sau khi pha loãng và rửa bằng dung dịch đệm ly giải hồng cầu.
Thảo luận
Xử lý mẫu tinh trùng bằng ELB giúp tăng tỷ lệ thu hồi, duy trì vận động tinh trùng, và không ảnh hưởng đến tiềm năng thụ tinh, phát triển phôi.
Verheyen và cộng sự (1995) là những người đầu tiên báo cáo sử dụng đệm ly giải hồng cầu để thu nhận tinh trùng từ tinh hoàn. Nghiên cứu này chỉ ra rằng dung dịch EBL không có tác động tiêu cực nào đến khả năng di chuyển và sức sống của tinh trùng [1]. Năm 1997, Nagy và cộng sự phát hiện rằng dung dịch ly giải hồng cầu (ELB) giúp tăng khả năng thu hồi tinh trùng từ những mẫu sinh thiết tinh hoàn ban đầu gần như không có tinh trùng. Trong 15 trường hợp NOA, 7 trường hợp có thể tiến hành ICSI nhờ xử lý bằng ELB. Khi so sánh giữa mẫu có và không xử lý bằng ELB, tỷ lệ thụ tinh (83% so với 68%) và phát triển phôi (87% so với 89%) không có khác biệt đáng kể [5]. Ngoài các chỉ số về khả năng di chuyển và sức sống, nhiều nghiên cứu đã xem xét thêm các thông số chức năng và mức độ trưởng thành của tinh trùng nhằm đánh giá chất lượng tinh trùng và khả năng thành công của điều trị vô sinh.
Thời gian xử lý mẫu mô trong dung dịch ELB cần được kiểm soát chặt chẽ nhằm giảm thiểu tác động bất lợi lên tinh trùng
Một số ý kiến cho rằng việc xử lý huyền phù tinh trùng bằng ELB có thể làm suy giảm chất lượng tinh trùng. Yazdinejad và cộng sự (2020) chứng minh rằng việc ủ tinh trùng trong ELB trong 10 phút làm giảm đáng kể khả năng vận động và sức sống, đồng thời tăng tỷ lệ phân mảnh DNA và tổn thương cấu trúc nhiễm sắc thể. Tác động này có xu hướng tăng theo thời gian tiếp xúc, cho thấy việc giới hạn thời gian xử lý là cần thiết để giảm thiểu ảnh hưởng bất lợi. Nhóm tác giả cũng đề xuất thời gian tiếp xúc từ 10 xuống 5 phút có thể gây ra ít tổn thương hơn cho các tế bào tinh trùng. Những giả thuyết này cần được xác nhận trong các nghiên cứu trong tương lai. Bên cạnh đó, nếu ELB được sử dụng, ICSI nên được thực hiện càng sớm càng tốt để giảm thiểu tác động phá hủy theo thời gian [2]. Năm 2018, Soygur và cộng sự đã thử nghiệm cho tinh trùng chỉ được tiếp xúc với ELB trong 5-10 giây, ngắn hơn đáng kể so với thời gian ủ thông thường (5-10 phút). Kết quả báo cáo cho thấy xử lý ELB không gây ra thay đổi đáng kể về khả năng di chuyển của tinh trùng, hình thái bình thường, khả năng sống, khả năng gắn HA (axit hyaluronic), độ trưởng thành của chromatin và sự phân mảnh DNA. Điều này có thể do thời gian tiếp xúc ngắn nên không đủ thời gian để ELB gây ra tổn thương, tuy nhiên phương pháp của Soygur vẫn còn giới hạn trong ứng dụng lâm sàng [7].
Ngoài ra, tác động tiêu cực của ELB lên tinh trùng được lý giải rằng do cơ chế phá vỡ cân bằng amoni gây ra sự ly giải trong hồng cầu cũng có trong tinh trùng. Bên cạnh đó, căng thẳng áp suất thẩm thấu do thành phần hóa học của dung dịch đệm có thể làm tổn thương màng tế bào và thay đổi chuyển hóa nội bào của tinh trùng [8], [9].
Mặc dù ảnh hưởng tiềm ẩn của ELB đối với các thông số tinh trùng vẫn chưa được làm rõ hoàn toàn, dung dịch này hiện vẫn được sử dụng rộng rãi trong quy trình thu nhận tế bào mầm tinh hoàn để loại bỏ hồng cầu, giúp làm trong mẫu và cải thiện khả năng quan sát dưới kính hiển vi [9], [10], [11].
Kết luận
Việc sử dụng dung dịch ly giải hồng cầu (ELB) mang lại lợi ích rõ rệt trong làm sạch mẫu mô tinh hoàn, rút ngắn thời gian thao tác, và tăng hiệu quả thu hồi tinh trùng. Tuy nhiên, tiếp xúc kéo dài với ELB có thể ảnh hưởng tiêu cực đến chất lượng và tính toàn vẹn di truyền của tinh trùng. Do đó, thời gian xử lý cần được giới hạn tối thiểu, và ICSI nên được thực hiện sớm sau xử lý để giảm thiểu tổn thương. Những nghiên cứu sâu hơn về cơ chế tác động phân tử của ELB đối với tinh trùng là cần thiết nhằm xác định ngưỡng an toàn và tối ưu hóa ứng dụng lâm sàng của dung dịch này trong hỗ trợ sinh sản.
Từ khoá: Vô tinh, vô tinh do tắc, vô tinh không do tắc, trích xuất tinh trùng từ tinh hoàn, xử lý trong phòng thí nghiệm, dung dịch ly giải hồng cầu.
Tài liệu tham khảo
[1] Verheyan G, De Croo I, Tournaye H, Pletincx I, Devroey P, van Steirteghem AC. Comparison of four mechanical methods to retrieve spermatozoa from testicular tissue. Hum Reprod. 1995;10:2956–9. doi: 10.1093/oxfordjournals.humrep.a135828.
[2] Yazdinejad, F.; Heydari, L.; Motamed Zadeh, L.; Seifati, S.M.; Agha-Rahimi, A. Application of erythrocyte lysing buffer (ELB) has detrimental effects on human sperm quality parameters, DNA fragmentation and chromatin structure. Andrologia 2020, 52, e13702.
[3] Vani, R., Anusha, B. A., Christina, R. M., Kavin, P., Mohammed, O., Inchara, S., ... & Sindhu, H. S. (2024). Band 3 Protein: A Critical Component of Erythrocyte. In Red Blood Cells-Properties and Functions. IntechOpen.
[4] Esteves SC, Varghese AC. Laboratory handling of epididymal and testicular spermatozoa: What can be done to improve sperm injections outcome. J Hum Reprod Sci. 2012 Sep;5(3):233-43. doi: 10.4103/0974-1208.106333. PMID: 23533051; PMCID: PMC3604828.
[5] Nagy, Z. P., Verheyen, G., Tournaye, H., Devroey, P., & Van Steirteghem, A. (1997). An improved treatment procedure for testicular biopsy specimens offers more efficient sperm recovery: case series. Fertility and sterility, 68(2), 376-379.
[6] [Li Y, Nakka K, Olender T, Gingras-Gelinas P, Wong MM, Robinson DCL, Bandukwala H, Palii CG, Neyret O, Brand M, Blais A, Dilworth FJ. Chromatin and transcription factor profiling in rare stem cell populations using CUT&Tag. STAR Protoc. 2021 Aug 19;2(3):100751. doi: 10.1016/j.xpro.2021.100751. PMID: 34467227; PMCID: PMC8384913.]
[7] Soygur, B.; Celik, S.; Celik-Ozenci, C.; Sati, L. Effect of erythrocyte-sperm separation medium on nuclear, acrosomal, and membrane maturity parameters in human sperm. J. Assist. Reprod. Genet. 2018, 35, 491–501.
[8] Ball, B.A. Oxidative stress, osmotic stress and apoptosis: Impacts on sperm function and preservation in the horse. Anim. Reprod. Sci. 2008, 107, 257–267.
[9] Aydos K, Aydos OS. Sperm Selection Procedures for Optimizing the Outcome of ICSI in Patients with NOA. J Clin Med. 2021 Jun 18;10(12):2687. doi: 10.3390/jcm10122687. PMID: 34207121; PMCID: PMC8234729.
[10] Tanaka, A.; Nagayoshi, M.; Takemoto, Y.; Tanaka, I.; Kusunoki, H.; Watanabe, S.; Kuroda, K.; Takeda, S.; Ito, M.; Yanagimachi, R. Fourteen babies born after round spermatid injection into human oocytes. Proc. Natl. Acad. Sci. USA 2015, 112, 14629–14634.
[11] Goswami, G.; Singh, S.; Devi, M.G. Successful fertilization and embryo development after spermatid injection: A hope for nonobstructive azoospermic patients. J. Hum. Reprod. Sci. 2015, 8, 175–177.