Nội dung chính
- 1. MỞ ĐẦU
- 2. Yếu tố di truyền liên quan đến bất thường đa hình thái đuôi (MMAF) ở tinh trùng di động yếu
- 3. Tinh trùng bất động do khiếm khuyết chức năng
- 4. Khiếm khuyết con đường chuyển hóa năng lượng
- 5. Sàng lọc di truyền và quản lý bệnh nhân
- 7. Chẩn đoán bất động tinh trùng trong bối cảnh bệnh lý lông chuyển (ciliopathies)
- 8. Ứng dụng lâm sàng
- 9. Kết luận
- 10. Tài liệu tham khảo
Trong quá trình biệt hóa và trưởng thành, bất kỳ sai lệch nào ở cấp độ phân tử cũng dẫn đến khiếm khuyết về mặt cấu trúc hoặc chức năng của đuôi tinh trùng, dẫn đến tình trạng tinh trùng di động yếu (asthenozoospermia). Đây được xem là tình trạng bệnh lý phổ biến nhất liên quan đến vô sinh nam ở người, ước tính khoảng 82% trong các trường hợp[1].
Mặc dù các nguyên nhân như giãn tĩnh mạch thừng tinh, nhiễm trùng cơ quan sinh dục, rối loạn nội tiết, hoặc lối sống và độc chất đã được ghi nhận, phần lớn các trường hợp bất động tinh trùng vẫn chưa được giải thích rõ ràng[1,2]. Các nghiên cứu gần đây đã xác định được nhiều gen liên quan đến sự hình thành đuôi tinh trùng, các kênh ion màng, enzyme chuyển hóa và các con đường tín hiệu liên quan đến khả năng di động tinh trùng[2].
Bài viết này cung cấp những thông tin về di truyền học của tình trạng tinh trùng di động yếu ở người, liên quan đến các đột biến gen gây ra hội chứng đa bất thường hình thái đuôi tinh trùng (Multiple Morphological Abnormalities of Flagella - MMAF) và các đột biến ảnh hưởng đến sự hoạt hóa và tăng động của tinh trùng. Đồng thời, bài viết cũng cập nhật những khuyến nghị trong quản lý bệnh nhân, từ tư vấn di truyền, chẩn đoán đến việc xây dựng các chiến lược điều trị mới và tiềm năng phát triển thuốc tránh thai nam giới trong tương lai.
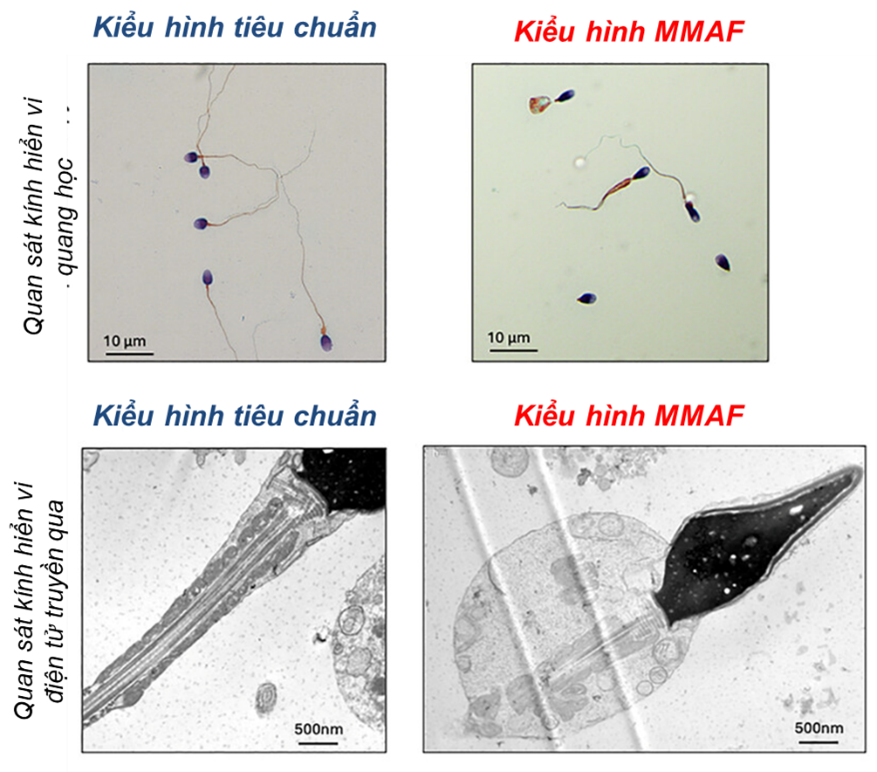
Kiểu hình tinh trùng MMAF
Dạng khiếm khuyết hình thái đuôi tinh trùng nghiêm trọng nhất là MMAF. Kiểu hình này đặc trưng bởi sự hiện diện đồng thời của nhiều dạng bất thường đuôi trong cùng một mẫu tinh dịch như: tinh trùng không có đuôi, đuôi ngắn, đuôi cuộn, đuôi không đều hoặc đuôi có đường kính bất thường, v.v... (Hình 1)[1].
Đuôi tinh trùng là một loại lông chuyển vận động đặc biệt, được cấu tạo dựa trên một khung xương tế bào vi ống gọi là sợi trục (axoneme). Lực đẩy tạo sự di động của đuôi được cung cấp bởi các nhánh dynein (Outer Dynein Arm - ODA) và nội vi (Inner Dynein Arm - IDA), đây là các phức hợp đa protein hoạt động như các động cơ phụ thuộc ATP (Adenosine Triphosphate)[3].
Ở mức độ siêu cấu trúc, MMAF gây ra sự mất tổ chức nghiêm trọng của cả sợi trục và các cấu trúc quanh sợi trục[1]. Các quan sát dưới kính hiển vi điện tử truyền qua (TEM) cho thấy tinh trùng thường thiếu cặp vi ống trung tâm hoặc các cặp vi ống ngoại vi, thiếu nhánh dynein và bao xơ (fibrous sheath) thường bị dày lên bất thường. Tình trạng này dẫn đến khả năng di động tinh trùng giảm hoặc mất hoàn toàn, với tỷ lệ tinh trùng di động tiến tới gần như bằng không[1,3].
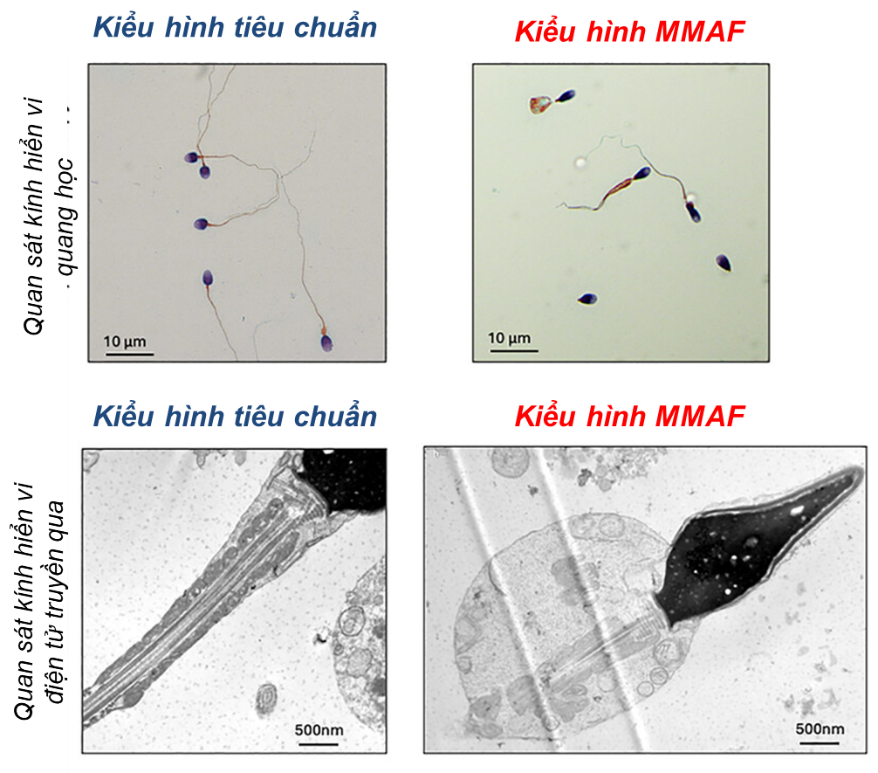
Hình 1. Kiểu hình của hội chứng tinh trùng di động yếu-dị dạng liên quan đến MMAF. K Khiếm khuyết cấu trúc và siêu cấu trúc của tinh trùng được quan sát trong tinh dịch của bệnh nhân có kiểu hình MMAF dưới kính hiển vi. Tinh trùng không đuôi, ngắn, cuộn, đường kính bất thường, kèm theo vỏ ty thể bị suy yếu và dư thừa tế bào chất[1].
Các gen liên quan đến MMAF
Mặc dù kiểu hình MMAF đã được mô tả từ lâu nhưng nguyên nhân di truyền của tình trạng này chỉ mới được sáng tỏ gần đây, bắt đầu với việc xác định gen dynein axonemal heavy chain 1 (DNAH1) vào năm 2014. Đến nay, số lượng gen liên quan đến MMAF được xác định đã lên đến gần 40 gen giúp giải thích được khoảng 50% đến hơn 60% các trường hợp lâm sàng trong các đoàn hệ nghiên cứu khác nhau[1]. Các gen này có thể được chia thành các nhóm chức năng chính dựa trên vai trò của protein mà chúng mã hóa (Hình 2):
Các thành phần sợi trục bao gồm các gen mã hóa cho các nhánh dynein và các phức hợp sợi trục liên quan như cilia and flagella associated protein 57 (CFAP57), 61 (CFAP61), 65 (CFAP65), 70 (CFAP70), 91 (CFAP91), 251 (CFAP251), dynein axonemal heavy chain 12 (DNAH12), 17 (DNAH17), dynein heavy chain domain 1 (DNHD1), leucine rich repeat containing 23 (LRRC23) và zinc finger MYND-type containing 12 (ZMYND12)[4].
Quá trình IFT (Intraflagellar transport - IFT) là một quá trình chuyên biệt được điều khiển bởi động cơ phân tử đảm bảo việc vận chuyển có chọn lọc các protein từ phần gần đến phần xa của bào quan đang phát triển, đóng vai trò thiết yếu cho sự hình thành đuôi tinh trùng ở người[1]. Các đột biến ở các gen như coiled-coil domain containing 38 (CCDC38), cilia and flagella associated protein 53 (CFAP53), 58 (CFAP58), tetratricopeptide repeat domain 21A (TTC21A), 29 (TTC29) và WD repeat domain 19 (WDR19) ảnh hưởng đến quá trình IFT dẫn đến sai sót trong quá trình biệt hóa đuôi tinh trùng[1,4].
Trung thể là một yếu tố quan trọng khác, bởi lẽ trung thể là nền tảng khởi đầu cần thiết để lắp ráp sợi trục ở đuôi tinh trùng, các đột biến ở các gen mã hóa protein liên quan đến trung thể như centrosomal protein 128 (CEP128) và DAZ interacting zinc finger protein 1 (DZIP1) cũng dẫn đến kiểu hình MMAF[5].
Cấu trúc quanh sợi trục bị đột biến cũng ảnh hưởng đến MMAF. Theo đó, một số gen MMAF mã hóa cho các thành phần cấu tạo nên các cấu trúc quanh sợi trục đã được chỉ ra như A-kinase anchoring protein 3 (AKAP3), 4 (AKAP4), fibrous sheath interacting protein 2 (FSIP2) và outer dense fiber protein 2 (ODF2)[5].

Hình 2. Di truyền của hội chứng tinh trùng di động yếu-dị dạng liên quan đến MMAF. Các gen gây bệnh liệt kê theo chức năng protein ở người. Đột biến đã xác thực (màu đen), đột biến giả định (màu xám), các khiếm khuyết hình thái tinh trùng khác (màu xanh)[1].
Khiếm khuyết vòng Annulus và các bất thường khác
Bên cạnh MMAF, các khiếm khuyết ở các cấu trúc khác của đuôi cũng dẫn đến tình trạng tinh trùng bất động.
Vòng Annulus là cấu trúc vòng đậm đặc điện tử nằm ở điểm nối giữa đoạn cổ và đoạn đuôi tinh trùng. Cấu trúc này chủ yếu được cấu tạo từ các polyme protein Septin và chất vận chuyển anion[1,6]. Các đột biến ở gen septin 4 (SEPT4), 12 (SEPT12) và solute carrier family 26 member 8 (SLC26A8) (còn được gọi là testis anion transporter 1 - TAT1) dẫn đến việc mất hoàn toàn cấu trúc vòng annulus (Hình 2). Hệ quả là đuôi tinh trùng bị mỏng đi đáng kể tại điểm nối và thường xuyên bị gập lại, dẫn đến tình trạng bất động nghiêm trọng[6].
Bất thường bao ty thể cũng là yếu tố dẫn đến bất động tinh trùng. Gen armadillo repeat containing 12 (ARMC12) mã hóa cho một protein nằm ở màng ngoài ty thể của tinh trùng. Đột biến ở gen này dẫn đến sự vắng mặt gần như hoàn toàn của ty thể ở đoạn cổ, khiến cổ hoặc đuôi tinh trùng bị gập và các vi ống của sợi trục bị phân tán, gây mất khả năng vận động[7].
Quá trình sinh tinh đòi hỏi sự kiểm soát biểu hiện gen cực kỳ nghiêm ngặt. Rối loạn điều hòa mRNA cũng có thể dẫn đến tinh trùng mất khả năng di động[8]. Các đột biến ở các gen liên quan đến điều hòa như TATA-box binding protein associated factor 7 like (TAF7L), gen đảm bảo độ ổn định của mRNA như terminal nucleotidyltransferase 5D (TENT5D), hoặc gen điều hòa việc huy động mRNA vào ribosome như eukaryotic translation initiation factor 4 gamma 1 (EIF4G1) đã được xác định là nguyên nhân gây ra các khiếm khuyết hình thái đuôi và bất động tinh trùng (Hình 2)[8]. Điều này cho thấy bất kỳ sai sót nào trong việc kiểm soát các phân tử mRNA đều có thể làm gián đoạn quá trình hình thành đuôi[1,8].
Trong nhiều trường hợp lâm sàng, tinh trùng không biểu hiện các dị dạng nghiêm trọng ở đuôi nhưng lại bị suy giảm hoặc mất hoàn toàn khả năng di động. Tình trạng này thường do sự gián đoạn trong quá trình trưởng thành chức năng tại mào tinh hoặc thất bại trong quá trình hoạt hóa và tăng động diễn ra trong đường sinh dục nữ.
Rối loạn kênh ion và chất vận chuyển
Hệ thống kênh cation của tinh trùng (cation channel of sperm - CatSper) là kênh canxi đặc hiệu của tinh trùng đóng vai trò then chốt cho sự tăng động[1-3]. Các đột biến ở gen cation channel sperm associated 1 (CATSPER1), 2 (CATSPER2) và đơn vị phụ epsilon (CATSPERε) đã được xác định ở những bệnh nhân có tinh trùng không thể tăng động, dẫn đến thất bại trong việc thụ tinh dù các thông số tinh dịch đồ khác có thể bình thường (Hình 2)[1,9].
Kênh Kali và các bộ trao đổi Natri/Proton cũng đóng vai trò quan trọng trong việc điều hòa môi trường ion nội bào. Đột biến đồng hợp tử ở gen mã hóa kênh kali nhạy cảm với pH đặc hiệu của tinh trùng gây ra bất động tinh trùng đi kèm với các bất thường ở acrosome và ty thể[10]. Tương tự, gen spermatozoa-specific cation/proton antiporter (SLC9C1) đóng vai trò thiết yếu trong việc kiềm hóa tế bào chất. Các biến thể của gen này đã được chứng minh gây bất động tinh trùng nghiêm trọng ở người[10].
Ngoài ra, các thành viên thuộc họ gen solute carrier family 26 (SLC26) cũng ảnh hưởng đến sự tăng động của tinh trùng[10]. Các đột biến ở gen solute carrier family 26 member 3 (SLC26A3) và 8 (SLC26A8) không chỉ gây ra các khiếm khuyết hình thái nhẹ mà còn làm rối loạn sự hợp tác chức năng với kênh cystic fibrosis transmembrane conductance regulator – CFTR[10]. Sự gián đoạn này gây mất cân bằng nội môi ion và ngăn cản các dòng tín hiệu phosphoryl hóa protein liên tục cần thiết cho vận động tinh trùng[1].
Khiếm khuyết con đường tín hiệu và bộ khung tế bào
Enzyme Adenylyl Cyclase hòa tan (sAC) được mã hóa bởi gen adenylyl cyclase 10 (ADCY10) chịu trách nhiệm sản xuất cyclic adenosine monophosphate (cAMP) để kích hoạt con đường PKA. Các biến thể dịch khung ở ADCY10 gây ra bất động tinh trùng chức năng nghiêm trọng, vốn có thể được phục hồi một phần trong ống nghiệm bằng việc bổ sung các chất tương tự cAMP[11].
Bên cạnh đó, gen IQ motif containing H (IQCH) mã hóa cho một protein liên kết với Calmodulin (CaM) cũng gây ra thất bại trong quá trình hoạt hóa và vận động khi bị đột biến[12]. Ngoài ra, các đột biến ở Tektin 3 (TEKT3), Kinesin family member 9 (KIF9) và IQ motif and ubiquitin-like domain-containing (IQUB) ảnh hưởng đến sự linh hoạt của bộ khung xương đuôi, dẫn đến các kiểu uốn cong và đánh đuôi không đối xứng hoặc mất khả năng truyền lực cơ học (Hình 2)[12].
Vận động của tinh trùng là một quá trình tiêu tốn rất nhiều năng lượng. Quá trình này đòi hỏi sự phối hợp nhịp nhàng giữa đường phân và phosphoryl hóa, oxy hóa để duy trì mức ATP cao nhằm hỗ trợ các hoạt động cơ học và tín hiệu[1].
Đột biến bộ gen ty thể
Do ty thể tinh trùng nằm tập trung ở đoạn cổ, bất kỳ khiếm khuyết nào trong DNA ty thể (mitochondrial DNA - mtDNA) đều ảnh hưởng trực tiếp đến lực đẩy của tinh trùng[1].
Những mất đoạn quy mô lớn mtDNA (phổ biến nhất là đoạn 4977-bp, ngoài ra còn có các đoạn 4866, 7345, 7436 và 7599-bp) dẫn đến việc mất hoàn toàn hoặc làm biến đổi các gen thiết yếu mã hóa cho các phức hợp của chuỗi vận chuyển điện tử. Các gen bị ảnh hưởng bao gồm mitochondrially encoded NADH: ubiquinone oxidoreductase core subunit 4 (MT-ND4) (thuộc phức hợp I), mitochondrially encoded cytochrome c oxidase subunit III (MT-COIII) (thuộc phức hợp IV) và mitochondrially encoded ATP synthase membrane subunit 6 (MT-ATPase6) (thuộc phức hợp V). Sự thiếu hụt này gây suy giảm năng lượng nghiêm trọng và bất động tinh trùng (Hình 2)[1].
Các biến thể điểm trong các mtDNA cũng được xác định là nguyên nhân gây bệnh. Cụ thể, các biến thể ở gen MT-ND4 hoặc các gen mã hóa đơn vị phức hợp IV như mitochondrially encoded cytochrome c oxidase subunit I (MT-COI) và II (MT-COII) đã được tìm thấy với tần suất cao hơn đáng kể ở nam giới bị bất động tinh trùng so với nhóm bình thường[1].
Các gen sản xuất năng lượng trong nhân
Gen adenylate kinase 9 (AK9) mã hóa cho một enzyme adenylate kinase biểu hiện chủ yếu tại tinh hoàn, đóng vai trò quan trọng trong việc duy trì sự cân bằng nucleotide bằng cách xúc tác chuyển đổi hai phân tử adenosine diphosphate (ADP) thành một phân tử ATP và một phân tử adenosine monophosphate (AMP). Bệnh nhân mang biến thể gen AK9 có mức ATP thấp và bị rối loạn các chất trung gian của quá trình đường phân, khiến tinh trùng hoàn toàn không có khả năng bơi[13].
Đột biến hoặc sự suy giảm biểu hiện của protein polypeptide N-acetylgalactosaminyltransferase-like protein 5 (GALNTL5) (ảnh hưởng đến việc tải protein và enzyme đường phân) hoặc các enzyme đường phân đặc hiệu cho tinh trùng như glyceraldehyde-3-phosphate dehydrogenase, spermatogenic (GAPDS) và lactate dehydrogenase C (LDHC) làm giảm đáng kể mức ATP, dẫn đến suy giảm tiềm năng thụ tinh và khả năng di động của tinh trùng (Hình 2)[1].
Sự thiếu hụt enzyme adipose triglyceride lipase (ATGL) có chức năng xúc tác phản ứng đầu tiên của quá trình phân giải mỡ, làm gián đoạn quá trình chuyển hóa triglyceride acid béo chuỗi dài gây ảnh hưởng tiêu cực đến quá trình sinh tinh và làm giảm đáng kể khả năng vận động của tinh trùng[14].
Sàng lọc di truyền trên quy mô lớn có thể xác định được nguyên nhân phân tử cho 30% - 60% bệnh nhân có kiểu hình MMAF[15]. Việc có một chẩn đoán di truyền rõ ràng không chỉ giúp bệnh nhân chấp nhận tình trạng bệnh lý mà còn là cơ sở để tư vấn các bước tiếp theo. Tuy nhiên, do hầu hết các đột biến gây bất động tinh trùng là di truyền lặn trên nhiễm sắc thể thường hoặc liên kết X, việc sử dụng các kỹ thuật hỗ trợ sinh sản chắc chắn sẽ truyền gen bệnh cho thế hệ sau[1]. Vì vậy, chẩn đoán tiền sản là cần thiết cho các cặp vợ chồng này. Đối với bệnh nhân MMAF, phần lớn các nghiên cứu cho thấy tỷ lệ thụ tinh và tạo phôi sau ICSI là tương đương với các nhóm vô sinh nam khác, cũng như kết cục trẻ sinh sống[1].
Vì roi tinh trùng được coi là một loại lông chuyển vận động đặc biệt, có cấu trúc sợi trục tương tự như lông chuyển trong các cơ quan khác của cơ thể, tình trạng bất động tinh trùng thường không chỉ xuất hiện đơn thuần mà là một phần của các hội chứng bệnh lý rộng hơn gọi là bệnh lý lông chuyển[1].
Rối loạn vận động lông chuyển nguyên phát (Primary Ciliary Dyskinesia - PCD) là bệnh lý điển hình nhất liên quan đến sự bất thường của các lông chuyển vận động (cấu trúc 9 + 2). Bệnh nhân PCD thường xuyên bị nhiễm trùng đường hô hấp mãn tính, viêm xoang và giãn phế quản do lông chuyển ở mũi và phế quản bị lỗi cấu trúc, không thể làm sạch dịch nhầy. Nhiều đột biến ở các gen mã hóa thành phần sợi trục như dynein axonemal heavy chain 1 (DNAH1), coiled-coil domain containing 39 (CCDC39), 40 (CCDC40) hoặc các gen liên quan đến hệ thống IFT đã được xác nhận gây ra cả MMAF ở tinh trùng và các triệu chứng hô hấp ở bệnh nhân[16].
Các đột biến ở gen intraflagellar transport 74 (IFT74) có thể dẫn đến các hội chứng hệ thống nặng nề như hội chứng Bardet-Biedl (BBS) hoặc hội chứng Joubert (JBTS) với các biểu hiện như béo phì, đa ngón và khuyết tật trí tuệ. Tuy nhiên, trong một số trường hợp lâm sàng, các biến thể nhẹ hơn ở cùng gen này chỉ biểu hiện đơn thuần là vô sinh nam do kiểu hình MMAF mà không kèm theo các dấu hiệu khác[17].
Đột biến ở gen POC1 centriolar protein B (POC1B) đã được chứng minh là ảnh hưởng đồng thời đến cả tế bào thụ cảm quang ở võng mạc và sự hình thành đuôi tinh trùng. Trong khi đó, đột biến ở gen nephronophthisis 4 (NPHP4) có liên quan mật thiết đến bệnh thận nang (Nephronophthisis) đi kèm với tình trạng tinh trùng bị bất động[1].
Việc nhận diện chính xác các gen này không chỉ giúp chẩn đoán nguyên nhân vô sinh mà còn cho phép các bác sĩ chủ động tầm soát sớm các biến chứng tiềm ẩn ở thận, mắt hoặc hệ hô hấp, từ đó mang lại sự chăm sóc toàn diện cho bệnh nhân.
Các chiến lược điều trị tiềm năng
Nghiên cứu hiện nay đang tập trung vào việc phục hồi khả năng vận động của tinh trùng thông qua nhiều phương pháp tiếp cận khác nhau. Bổ sung peptide và yếu tố tăng trưởng là một chủ đề được nghiên cứu nhiều gần đây. Việc bổ sung các peptide có nguồn gốc từ mào tinh như Beta-defensin 126 (DEFB126) đã được quan sát thấy làm tăng khả năng vận động của tinh trùng người trong môi trường nuôi cấy. Tương tự, C-type Natriuretic Peptide (CNP) giúp cải thiện sự vận động và chức năng sinh sản thông qua kích hoạt con đường cyclic guanosine monophosphate/ protein kinase G (cGMP/PKG) và các làn sóng canxi nội bào[18].
Ngoài ra, liệu pháp hỗ trợ vật lý (Mechanotherapy) như sử dụng sóng siêu âm tần số cao trong thời gian ngắn (20 giây) hoặc liệu pháp ánh sáng LED (bước sóng 470–850 nm) đã cho thấy những cải thiện đáng kể về độ di động tiến tới của tinh trùng mà không ảnh hưởng đến khả năng sống hay gây đứt gãy DNA[19].
Liệu pháp gen và ATP đã được chứng minh trên các mô hình động vật cho thấy, việc sử dụng các hạt nano mang ATP hoặc các chất ức chế miRNA (như miR-24-3p) trực tiếp vào tinh hoàn đã giúp phục hồi thành công các khiếm khuyết về năng lượng và vận động của tinh trùng[19].
Điều trị bằng chất chống oxy hóa là phương pháp phổ biến nhất trên lâm sàng. Bổ sung Vitamin D3, Coenzyme Q10, hoặc sự kết hợp giữa L-carnitine và các vitamin (E, C) đã cho thấy hiệu quả nhất định trong việc giảm tác động của stress oxy hóa và cải thiện nhẹ các thông số tinh dịch đồ[20].
Phát triển thuốc tránh thai nam giới
Việc xác định các protein thiết yếu cho sự vận động nhưng chỉ biểu hiện đặc hiệu tại tinh trùng đã tạo tiền đề cho các loại thuốc tránh thai nam giới không chứa hormone.
Isoform của protein phosphatase 1 đặc hiệu ở tinh trùng (protein phosphatase 1 isoform gamma 2 - PP1γ2) đóng vai trò chủ chốt trong việc điều hòa sự vận động của tinh trùng. Các peptide tổng hợp có khả năng xâm nhập vào tinh trùng và làm rối loạn sự tương tác của enzyme PP1γ2 với các protein điều hòa (RIPPO), từ đó làm giảm mạnh tỷ lệ tinh trùng di động tiến tới[21].
Enzyme adenylyl cyclase hòa tan (soluble adenylyl cyclase - sAC) là một enzyme then chốt trong các con đường tín hiệu điều hòa sự vận động và hoạt hóa. Chất có tên TDI-11861 là một hợp chất ức chế chọn lọc có thể làm tinh trùng ngừng vận động hoàn toàn chỉ khoảng 15 phút sau khi sử dụng và khả năng sinh sản được phục hồi hoàn toàn sau 24 giờ. Đây là một loại thuốc tránh thai nam giới tức thời, không chứa hormone và có khả năng phục hồi hoàn toàn khả năng di động tinh trùng sau đó[22].
Tinh trùng bất động là một thách thức lớn trong nam khoa, nhưng những tiến bộ về di truyền học giúp thay đổi quá trình chẩn đoán và quản lý bệnh nhân. Việc xác định nguyên nhân di truyền giúp bệnh nhân hiểu rõ tình trạng của mình và cung cấp cơ sở để tư vấn về nguy cơ truyền gen bệnh cho thế hệ sau. Ngoài ra, chẩn đoán di truyền cho phép bác sĩ tầm soát sớm các bệnh lý lông chuyển đi kèm, từ đó bảo vệ sức khỏe tổng quát cho bệnh nhân. Trong tương lai, việc xây dựng các quy trình sàng lọc di truyền quy mô lớn hơn là điều cần thiết, đây cũng là cơ sở vững chắc để tối ưu hóa kết quả hỗ trợ sinh sản ở nhóm bệnh nhân có tinh trùng di động yếu.
- Cavarocchi E và cs. Human asthenozoospermia: Update on genetic causes, patient management, and clinical strategies. Andrology. 2025;13(5), 1044-1064.
- Touré A và cs. The genetic architecture of morphological abnormalities of the sperm tail. Hum Genet. 2021;140(1), 21-42.
- Ishikawa T. Axoneme structure from motile cilia. Cold Spring Harb Perspect Biol. 2017;9(1), a028076.
- Wang J và cs. Clinical detection, diagnosis and treatment of morphological abnormalities of sperm flagella: a review of literature. Front Genet. 2022;13, 1034951.
- Ishikawa H và cs. Intraflagellar transport and ciliary dynamics. Cold Spring Harb Perspect Biol. 2017;9(3), a021998.
- Kuo YC và cs. SEPT12 orchestrates the formation of mammalian sperm annulus by organizing core octameric complexes with other SEPT proteins. J Cell Sci. 2015;128(5), 923-934.
- Liu W và cs. Biallelic mutations in ARMC12 cause asthenozoospermia and multiple midpiece defects in humans and mice. J Med Genet. 2023;60(2), 154-162.
- Zhang YT và cs. Novel variations in TENT5D lead to teratozoospermia in infertile patients. Andrology. 2024;12(6), 1336-1346.
- Wang H và cs. Sperm ion channels and transporters in male fertility and infertility. Nat Rev Urol. 2021;18(1), 46-66.
- Cavarocchi E và cs. The sodium/proton exchanger SLC9C1 (sNHE) is essential for human sperm motility and fertility. Clin Genet. 2021;99(5), 684-693.
- Akbari A và cs. ADCY10 frameshift variant leading to severe recessive asthenozoospermia and segregating with absorptive hypercalciuria. Hum Reprod. 2019;34(6), 1155-1164.
- Cavarocchi E và cs. Identification of IQCH as a calmodulin-associated protein required for sperm motility in humans. iScience. 2023;26(8).
- Sha Y và cs. Deficiency in AK9 causes asthenozoospermia and male infertility by destabilising sperm nucleotide homeostasis. EBioMedicine. 2023;96.
- He JY và cs. DEFB126 polymorphisms and association with idiopathic asthenozoospermia in China. Asian J Androl. 2022;24(6), 607-614.
- Coutton C và cs. Bi-allelic mutations in ARMC2 lead to severe astheno-teratozoospermia due to sperm flagellum malformations in humans and mice. Am J Hum Genet. 2019;104(2), 331-340.
- Lehti MS và cs. Formation and function of sperm tail structures in association with sperm motility defects. Biol Repro. 2017;97(4), 522-536.
- Ren Z và cs. Cilia‐related diseases. J Cell Mol Med. 2023;27(24), 3974-3979.
- Li N và cs. C-type natriuretic peptide (CNP) could improve sperm motility and reproductive function of asthenozoospermia. Int J Mol Sci. 2022;23(18), 10370.
- Zhou Q và cs. Curcumin improves asthenozoospermia by inhibiting reactive oxygen species reproduction through nuclear factor erythroid 2‐related factor 2 activation. Andrologia. 2020;52(2), e13491.
- Condorelli RA và cs. Poor efficacy of L-acetylcarnitine in the treatment of asthenozoospermia in patients with type 1 diabetes. J Clin Med. 2019;8(5), 585.
- Ferreira AF và cs. PP1, PP2A and PP2B interplay in the regulation of sperm motility: lessons from protein phosphatase inhibitors. Int J Mol Sci. 2022;23(23), 15235.
- Balbach M và cs. On-demand male contraception via acute inhibition of soluble adenylyl cyclase. Nat Commun. 2023;14(1), 637.