Nội dung chính
Trong những năm gần đây, khái niệm về vai trò của vi sinh vật trong sức khỏe sinh sản nữ đã có sự thay đổi đáng kể. Thay vì chỉ xem nhiễm trùng đường sinh dục như một yếu tố bệnh lý đơn lẻ cần loại bỏ, các nghiên cứu hiện đại đã chỉ ra rằng microbiome – hệ sinh thái vi sinh vật cư trú tại đường sinh dục và các cơ quan liên quan – là một thành phần sinh học có tính điều hòa, ảnh hưởng đến chức năng sinh sản [1], [2]. Đặc biệt, microbiome đang nổi lên như một yếu tố quyết định môi trường làm tổ của phôi và kết cục thai kỳ trong điều trị thụ tinh trong ống nghiệm.
1.1. Microbiome đường sinh dục dưới: âm đạo và cổ tử cung
Ở phụ nữ trong độ tuổi sinh sản, hệ vi sinh âm đạo khỏe mạnh thường do Lactobacillus, đặc biệt là L. crispatus, L. gasseri và L. jensenii chi phối, giúp duy trì pH thấp do chuyển hóa glycogen thành acid lactic dưới tác động của estrogen [3], [4]. Môi trường acid này hạn chế sự phát triển của vi khuẩn có hại và giảm đáp ứng viêm. Bên cạnh đó, microbiome âm đạo được phân loại thành các kiểu trạng thái khuẩn hệ âm đạo (community state types - CSTs). CSTs giàu Lactobacillus liên quan đến cân bằng vi sinh ổn định, còn CSTs có độ đa dạng cao (được gọi là CST IV) thường dẫn đến mất cân bằng và viêm âm đạo [5]. Do đó, đánh giá microbiome cần xem xét cả thành phần lẫn chức năng sinh học của chúng.
1.2. Microbiome đường sinh dục trên: nội mạc tử cung và các cơ quan liên quan
Các nghiên cứu cho thấy là nội mạc tử cung có microbiome mật độ thấp nhưng có chức năng sinh học quan trọng [6]. Lactobacillus chiếm ưu thế giúp tăng khả năng tiếp nhận phôi và mang thai thuận lợi, trong khi vi khuẩn khác liên quan đến viêm nhẹ và thất bại làm tổ [6], [7]. Bên cạnh đó, microbiome còn tác động lên quá trình làm tổ qua kiểm soát viêm, cấu trúc biểu mô và mạng lưới cytokine. Ngoài ra, một số vi sinh vật cũng được phát hiện ở vòi trứng và buồng trứng, đặc biệt trong bệnh lý như lạc nội mạc tử cung, dẫn đến mất cân bằng vi sinh từ đó góp phần vào các rối loạn chức năng sinh sản [8].
1.3. Microbiome, miễn dịch và nội tiết trong hệ sinh dục nữ
Microbiome điều hòa miễn dịch tại đường sinh dục nữ bằng cách cân bằng các quần thể tế bào miễn dịch (đại thực bào, NK, T helper). Khi mất sự cân bằng hệ vi sinh (Dysbiosis) xảy ra sẽ kích hoạt tín hiệu viêm qua Toll-like receptors - TLRs và con đường NF-κB, làm tăng cytokine tiền viêm và phá vỡ dung nạp miễn dịch cần thiết cho quá trình làm tổ [9]. Bên cạnh tác động tại chỗ, microbiome – đặc biệt là microbiome đường ruột – còn ảnh hưởng gián tiếp đến hệ sinh dục thông qua điều hòa hormone. Các vi khuẩn này tham gia chuyển hóa estrogen thông qua hệ gen estrobolome, từ đó tác động đến trục hạ đồi – tuyến yên – buồng trứng [10]. Sự mất cân bằng microbiome có thể dẫn đến rối loạn hormone, góp phần vào các bệnh lý như hội chứng buồng trứng đa nang, suy buồng trứng sớm và lạc nội mạc tử cung [11], [12].
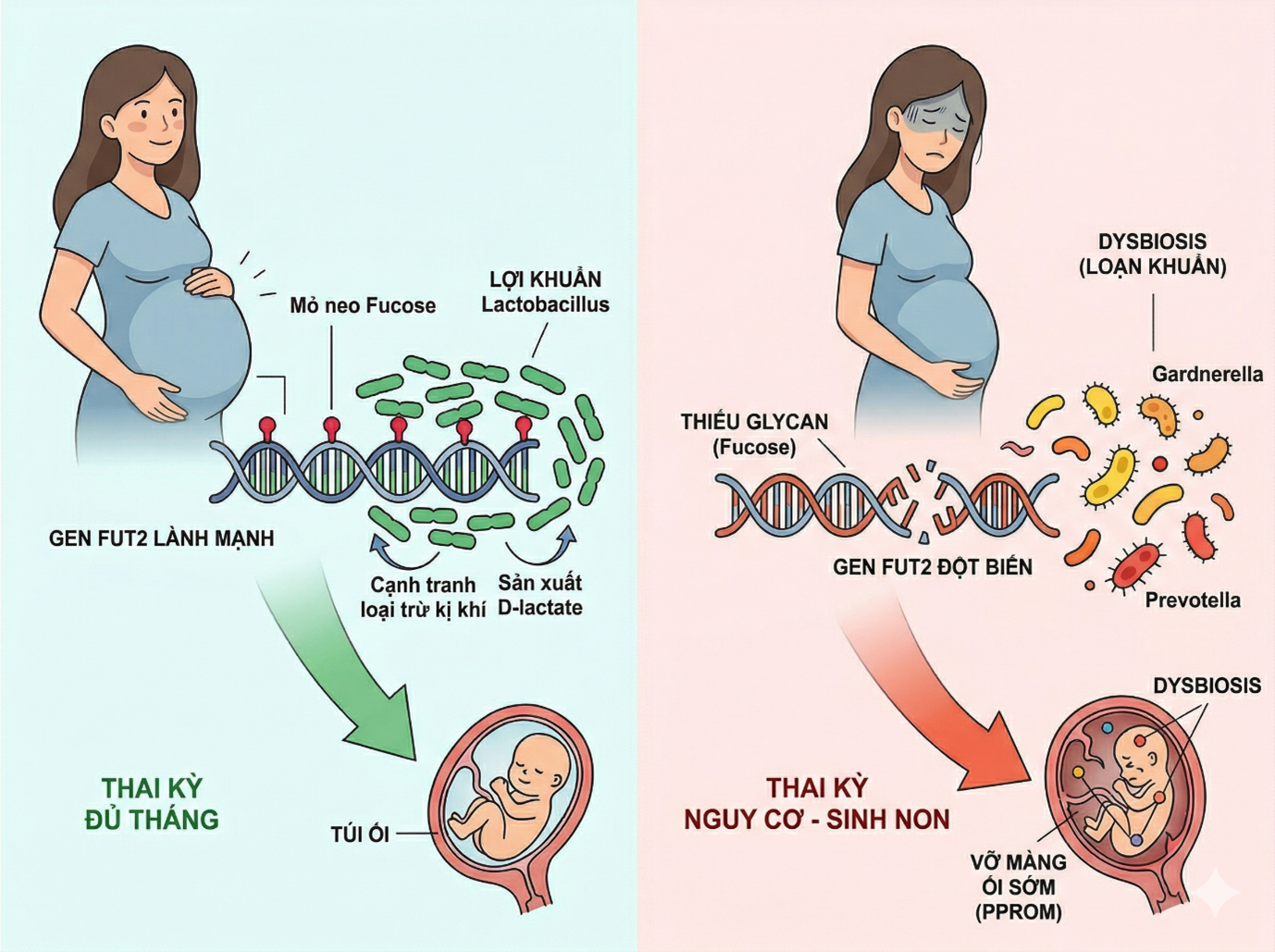
Nhiều nghiên cứu lâm sàng đã chỉ ra rằng microbiome nội mạc tử cung và âm đạo là yếu tố dự báo quan trọng đối với kết cục IVF. Đây còn được xem là một yếu tố độc lập với tuổi mẹ và chất lượng phôi. Phụ nữ với microbiome nội mạc tử cung ưu thế Lactobacillus, nhất là L. crispatus giúp ổn định hệ vi sinh, thường có tỷ lệ thành công làm tổ, thai lâm sàng và sinh sống cao hơn so với nhóm đa dạng vi khuẩn hoặc giàu vi khuẩn kỵ khí [13]. Mặt khác, nhóm vi khuẩn như Gardnerella, Atopobium, Prevotella, Streptococcus và Enterococcus liên quan sự mất cân bằng hệ vi sinh. Chúng thông qua ba cơ chế: (i) kích hoạt viêm nội mạc tử cung qua TLR–NF-κB; (ii) thay đổi chuyển hóa tại chỗ, tác động pH và môi trường vi mô; (iii) rối loạn điều hòa miễn dịch, đặc biệt là mất cân bằng Th17/Treg, giảm dung nạp phôi, từ đó liên quan đến thất bại chuyển phôi, sảy thai sớm và thất bại làm tổ do gây viêm kéo dài, thay đổi chuyển hóa và phá vỡ điều hòa miễn dịch [14]. Do đó, thành công IVF phụ thuộc không chỉ vào chất lượng phôi mà môi trường microbiome nội mạc tử cung tại thời điểm chuyển phôi cũng đóng vai trò quan trọng.
Lối sống là một trong những yếu tố thiết yếu có thể điều chỉnh microbiome, đặc biệt là hệ vi sinh đường ruột, từ đó ảnh hưởng gián tiếp đến sức khỏe sinh sản nữ. Đầu tiên là về chế độ ăn, chúng có tác động nhanh và rõ rệt nhất. Các nghiên cứu cho thấy thay đổi khẩu phần có thể làm biến đổi cấu trúc microbiome chỉ trong vài ngày [15]. Chế độ ăn giàu chất xơ giúp tăng các vi khuẩn có lợi và sản xuất acid béo chuỗi ngắn (SCFAs), từ đó giảm các phản ứng viêm và hỗ trợ cân bằng nội tiết. Ngược lại, chế độ ăn nhiều đường và chất béo bão hòa có thể gây mất cân bằng vi sinh, tăng phản ứng viêm và rối loạn chuyển hóa [16], [17]. Bên cạnh đó, các yếu tố như stress, giấc ngủ và tập thể dục cũng đóng vai trò quan trọng. Stress mạn tính thông qua trục ruột – não có thể làm thay đổi thành phần vi sinh và tăng đáp ứng viêm [18]. Thiếu ngủ liên quan đến rối loạn microbiome và giảm nhạy cảm insulin [19]. Ngược lại, hoạt động thể lực mức độ vừa phải giúp cải thiện đa dạng vi sinh và tăng cường chức năng chuyển hóa [20].
Ngoài ra, một số chiến lược can thiệp microbiome như kháng sinh chọn lọc, probiotic chứa Lactobacillus crispatus, điều chỉnh microbiome đường ruột và ghép microbiome âm đạo (vaginal microbiota transplantation) đã cho thấy tiềm năng cải thiện microbiome và kết cục IVF trong một số nghiên cứu tiền lâm sàng và lâm sàng quy mô nhỏ [21], [22]. Mặc dù các hướng tiếp cận này cho thấy nhiều hứa hẹn, nhưng bằng chứng lâm sàng hiện tại vẫn còn hạn chế. Vì vậy, việc ứng dụng microbiome trong IVF cần được tiếp cận một cách thận trọng, dựa trên dữ liệu khoa học và cá thể hóa theo từng bệnh nhân.
Microbiome không chỉ đóng vai trò là một yếu tố điều hòa sinh học then chốt trong hệ sinh dục nữ mà còn có ảnh hưởng quan trọng đối với hiệu quả của các chu kỳ thụ tinh trong ống nghiệm. Điều chỉnh lối sống và chế độ sinh hoạt hằng ngày nhằm hỗ trợ sự phát triển của hệ vi sinh khoẻ mạnh sẽ góp phần nâng cao sức khoẻ sinh sản.
[1] C. Huttenhower et al., “Structure, function and diversity of the healthy human microbiome,” Nature, vol. 486, no. 7402, pp. 207–214, Jun. 2012, doi: 10.1038/nature11234.
[2] “The vaginal microbiome and preterm birth | Nature Medicine.” Accessed: Feb. 24, 2026. [Online]. Available: https://www.nature.com/articles/s41591-019-0450-2
[3] V. Günther et al., “Vaginal Microbiome in Reproductive Medicine,” Diagnostics, vol. 12, no. 8, p. 1948, Aug. 2022, doi: 10.3390/diagnostics12081948.
[4] D. E. O’Hanlon, T. R. Moench, and R. A. Cone, “Vaginal pH and Microbicidal Lactic Acid When Lactobacilli Dominate the Microbiota,” PLOS ONE, vol. 8, no. 11, p. e80074, thg 11 2013, doi: 10.1371/journal.pone.0080074.
[5] P. B. Heczko, M. Giemza, W. Ponikiewska, and M. Strus, “Importance of Lactobacilli for Human Health,” Microorganisms, vol. 12, no. 12, p. 2382, Nov. 2024, doi: 10.3390/microorganisms12122382.
[6] I. Moreno et al., “Endometrial microbiota composition is associated with reproductive outcome in infertile patients,” Microbiome, vol. 10, p. 1, Jan. 2022, doi: 10.1186/s40168-021-01184-w.
[7] K. Kyono, T. Hashimoto, S. Kikuchi, Y. Nagai, and Y. Sakuraba, “A pilot study and case reports on endometrial microbiota and pregnancy outcome: An analysis using 16S rRNA gene sequencing among IVF patients, and trial therapeutic intervention for dysbiotic endometrium,” Reprod. Med. Biol., vol. 18, no. 1, pp. 72–82, Jan. 2019, doi: 10.1002/rmb2.12250.
[8] B. Toson, C. Simon, and I. Moreno, “The Endometrial Microbiome and Its Impact on Human Conception,” Int. J. Mol. Sci., vol. 23, no. 1, p. 485, Jan. 2022, doi: 10.3390/ijms23010485.
[9] J. M. Baker, L. Al-Nakkash, and M. M. Herbst-Kralovetz, “Estrogen–gut microbiome axis: Physiological and clinical implications,” Maturitas, vol. 103, pp. 45–53, Sep. 2017, doi: 10.1016/j.maturitas.2017.06.025.
[10] A. H. Larnder, A. R. Manges, and R. A. Murphy, “The estrobolome: Estrogen‐metabolizing pathways of the gut microbiome and their relation to breast cancer,” Int. J. Cancer, vol. 157, no. 4, pp. 599–613, Aug. 2025, doi: 10.1002/ijc.35427.
[11] Y. Liang et al., “Gut microbiome and reproductive endocrine diseases: a Mendelian randomization study,” Front. Endocrinol., vol. 14, p. 1164186, Aug. 2023, doi: 10.3389/fendo.2023.1164186.
[12] P. Escorcia Mora, D. Valbuena, and A. Diez-Juan, “The Role of the Gut Microbiota in Female Reproductive and Gynecological Health: Insights into Endometrial Signaling Pathways,” Life, vol. 15, no. 5, p. 762, May 2025, doi: 10.3390/life15050762.
[13] G. Kından, “The Impact of Vaginal Microbiota on IVF Success,” Reprod. Biomed. Online, vol. 51, p. 105329, Nov. 2025, doi: 10.1016/j.rbmo.2025.105329.
[14] B. Balla et al., “The Role of the Vaginal and Endometrial Microbiomes in Infertility and Their Impact on Pregnancy Outcomes in Light of Recent Literature,” Int. J. Mol. Sci., vol. 25, no. 23, p. 13227, Dec. 2024, doi: 10.3390/ijms252313227.
[15] A. Oliver et al., “High-Fiber, Whole-Food Dietary Intervention Alters the Human Gut Microbiome but Not Fecal Short-Chain Fatty Acids,” mSystems, vol. 6, no. 2, pp. e00115-21, doi: 10.1128/mSystems.00115-21.
[16] X. Han, Y. Ma, S. Ding, J. Fang, and G. Liu, “Regulation of dietary fiber on intestinal microorganisms and its effects on animal health,” Anim. Nutr., vol. 14, pp. 356–369, Jun. 2023, doi: 10.1016/j.aninu.2023.06.004.
[17] B. L. Tan and M. E. Norhaizan, “Effect of High-Fat Diets on Oxidative Stress, Cellular Inflammatory Response and Cognitive Function,” Nutrients, vol. 11, no. 11, p. 2579, Oct. 2019, doi: 10.3390/nu11112579.
[18] J. A. Foster, L. Rinaman, and J. F. Cryan, “Stress & the gut-brain axis: Regulation by the microbiome,” Neurobiol. Stress, vol. 7, pp. 124–136, Mar. 2017, doi: 10.1016/j.ynstr.2017.03.001.
[19] J. Sun, D. Fang, Z. Wang, and Y. Liu, “Sleep Deprivation and Gut Microbiota Dysbiosis: Current Understandings and Implications,” Int. J. Mol. Sci., vol. 24, no. 11, p. 9603, May 2023, doi: 10.3390/ijms24119603.
[20] M. U. Sohail, H. M. Yassine, A. Sohail, and A. A. Al Thani, “Impact of Physical Exercise on Gut Microbiome, Inflammation, and the Pathobiology of Metabolic Disorders,” Rev. Diabet. Stud. RDS, vol. 15, pp. 35–48, 2019, doi: 10.1900/RDS.2019.15.35.
[21] Y. Meng, J. Sun, and G. Zhang, “Vaginal microbiota transplantation is a truly opulent and promising edge: fully grasp its potential,” Front. Cell. Infect. Microbiol., vol. 14, p. 1280636, Mar. 2024, doi: 10.3389/fcimb.2024.1280636.
[22] V. D. Valeriano, E. Lahtinen, I.-C. Hwang, Y. Zhang, J. Du, and I. Schuppe-Koistinen, “Vaginal dysbiosis and the potential of vaginal microbiome-directed therapeutics,” Front. Microbiomes, vol. 3, Oct. 2024, doi: 10.3389/frmbi.2024.1363089.