CNSH. Lê Thị Quỳnh – IVFMD SIH – Bệnh viện Phụ sản Quốc tế Sài Gòn
-
Mở đầu
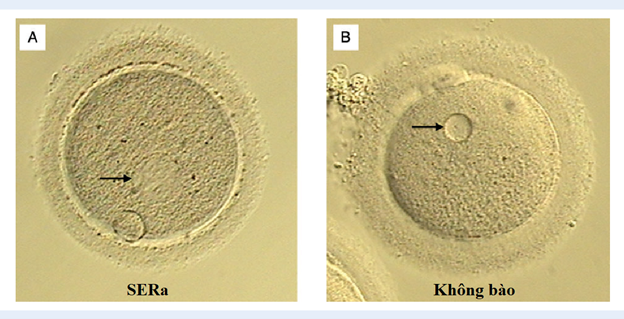
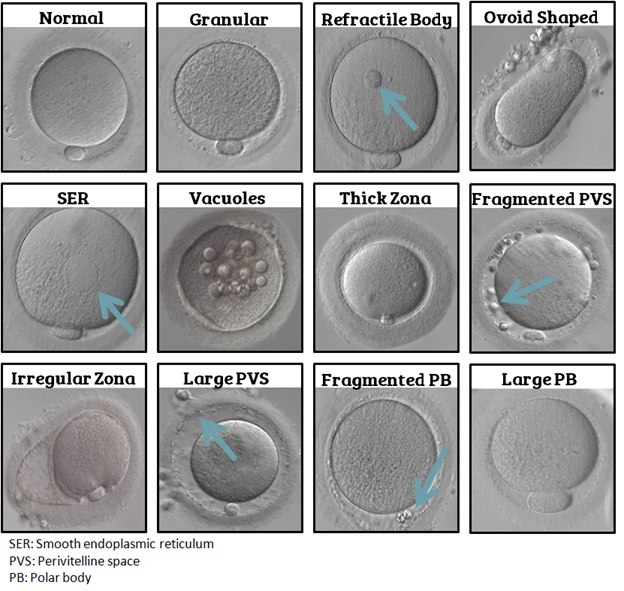
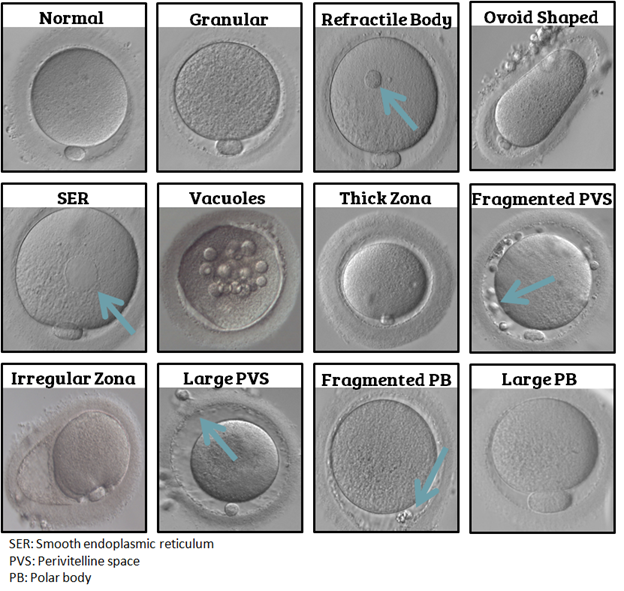
Trong lĩnh vực phôi học lâm sàng và hỗ trợ sinh sản (HTSS), việc đánh giá hình thái noãn là một bước quan trọng để dự đoán tiềm năng phát triển của phôi. Trong số các bất thường hình thái tế bào chất, cụm lưới nội chất trơn (Smooth Endoplasmic Reticulum aggregates – SERa) hay còn gọi là đĩa SER đã thu hút sự chú ý của giới chuyên môn trong suốt hơn hai thập kỷ qua[1]. Dưới kính hiển vi quang học, SERa thường xuất hiện như một hoặc nhiều cấu trúc dạng đĩa, mờ, có thể làm thay đổi sự khúc xạ ánh sáng bên trong bào tương của noãn trưởng thành (Metaphase II - MII)[2].
Lịch sử quan điểm về noãn có chứa SERa đã trải qua những biến động lớn, phản ánh sự phát triển của y học thực chứng. Vào năm 2011, Đồng thuận Istanbul do Hiệp hội Sinh sản và Phôi học Châu Âu (ESHRE) và tổ chức Alpha Scientists in Reproductive Medicine (gọi tắt là Alpha) ban hành đã xếp SERa vào nhóm “noãn bệnh lý”[1]. Dựa trên một số báo cáo ca bệnh về hội chứng đa dị tật bẩm sinh hoặc hội chứng Beckwith-Wiedemann ở trẻ sinh ra từ noãn có SERa, đồng thuận này khuyến cáo mạnh mẽ việc loại bỏ và không thực hiện ICSI trên các noãn SERa(+)[1, 3]. Hệ quả là hàng ngàn noãn có tiềm năng đã bị hủy bỏ trên toàn cầu, gây thiệt thòi lớn cho bệnh nhân, đặc biệt là nhóm đáp ứng buồng trứng kém[3].
Tuy nhiên, sự tiến bộ của khoa học đã khiến các chuyên gia phải đánh giá lại. Những thay đổi trong Đồng thuận Vienna (2017) và gần đây nhất là bản Cập nhật Đồng thuận ESHRE/Alpha 2024-2025 đã tạo ra một bước ngoặt lịch sử[4]. Với sự tích lũy của các dữ liệu lâm sàng mới chứng minh khả năng sinh ra những đứa trẻ khỏe mạnh từ noãn SERa(+), ESHRE 2024-2025 đã chính thức gỡ bỏ lệnh cấm tuyệt đối, chuyển SERa từ phân loại “đỏ” (hủy bỏ) sang đánh giá “case-by-case” (tùy từng trường hợp cụ thể)[4, 5].
Vấn đề đặt ra hiện nay không còn là việc có nên vứt bỏ noãn SERa(+) hay không, mà là làm thế nào để hiểu rõ nguồn gốc sinh học của các noãn này, từ đó tối ưu hóa chiến lược điều trị tại labo IVF và cung cấp các tư vấn di truyền chính xác nhất cho bệnh nhân[6, 7].
-
Bản chất và vai trò của SERa
Về mặt sinh học tế bào, SER là một hệ thống màng bao gồm các ống và túi không có ribosome bám trên bề mặt, đóng vai trò trung tâm trong quá trình tổng hợp lipid, chuyển hóa carbohydrate và đặc biệt là kho lưu trữ Canxi (Ca2+) nội bào[7, 8]. Phân tích bằng kính hiển vi điện tử truyền qua (TEM) của Sá và cộng sự (2011) đã cho thấy bản chất thực sự của SERa[8]. Khác với các túi SER phân tán đơn lẻ trong noãn bình thường, SERa là sự kết tụ bất thường của mạng lưới các ống lưới nội chất trơn dạng hình ống, đan xen chặt chẽ với nhau tạo thành một khối có kích thước lớn[8].
Về mặt vật lý, do chứa mật độ cao màng lipid kép và các protein xuyên màng, khối kết tụ này tạo ra sự thay đổi về chiết suất ánh sáng nội bào. Đây là lý do tại sao dưới hệ thống quang học Hoffman, các cụm SERa hiện lên như những “đĩa” hoặc không bào mờ đục có thể dễ dàng nhận diện bằng mắt thường của chuyên viên phôi học[2].
Trong không gian 3D của bào tương, các cụm SERa thường được bao quanh bởi một vòng các ty thể[9]. Mối quan hệ không gian này phản ánh sự tương tác sinh hóa cường độ cao giữa việc cung cấp năng lượng (ATP) và giải phóng tín hiệu Canxi[7, 9]. Nghiên cứu phân tích cấu hình biểu hiện gen của Stigliani và cộng sự (2018) đã so sánh noãn SERa(+) và SERa(-), nhóm tác giả phát hiện ra sự rối loạn điều hòa của nhiều gen mã hóa các protein liên kết Canxi và các kênh vận chuyển ion trên màng[10].
Quá trình thụ tinh bình thường cần phải có sự giải phóng các đợt sóng Canxi từ kho dự trữ lưới nội chất để hoạt hóa noãn ngăn chặn hiện tượng đa thụ tinh. Bên cạnh đó, kích hoạt sự tiếp tục của quá trình giảm phân II[9, 10]. Sự kết tụ thành các đĩa SERa lớn sẽ làm giảm khả năng phân phối đồng đều Canxi trong tế bào chất[7, 8]. Sự gián đoạn này là nguyên nhân chính giải thích vì sao noãn SERa(+) thường có tỷ lệ thụ tinh bất thường hoặc nguy cơ thoái hoá cao hơn khi có các tác động cơ học như ICSI[10].
-
Nguồn gốc và cơ chế hình thành SERa
Nghiên cứu quy mô lớn năm 2025 của Gashti và cộng sự đã làm sáng tỏ mối liên hệ giữa nguyên nhân vô sinh nữ và sự hiện diện của SERa[11]. Các dữ liệu lâm sàng chỉ ra rằng tỷ lệ xuất hiện chu kỳ có noãn SERa(+) tăng lên đáng kể ở các nhóm bệnh nhân mắc hội chứng buồng trứng đa nang, lạc nội mạc tử cung và giảm dự trữ buồng trứng[11]. Điều này gợi ý rằng một môi trường vi nang noãn (follicular microenvironment) chứa nhiều yếu tố viêm hoặc stress oxy hóa nội bào có thể là tác nhân kích hoạt sự hình thành SERa[7, 11].
Một giả thuyết được chấp nhận rộng rãi là SERa là hệ quả trực tiếp của phác đồ kích thích buồng trứng (KTBT) cường độ cao. Từ những quan sát đầu tiên, Otsuki và cộng sự (2004) đã ghi nhận sự tương quan thuận giữa nồng độ Estradiol (E2) đỉnh vào ngày tiêm hCG và tỷ lệ xuất hiện noãn SERa[2]. Quá trình KTBT bằng nồng độ FSH ngoại sinh cao buộc các tế bào hạt và noãn phải tăng tốc độ chuyển hóa[12]. Tốc độ sinh tổng hợp màng lipid diễn ra ồ ạt, vượt quá khả năng tổ chức không gian của hệ thống khung xương tế bào. Hệ quả là thay vì phân tán đều khắp tế bào chất, các ống lưới nội chất bị cuộn lại thành SERa[7, 12].
Tuy nhiên, các nghiên cứu so sánh giữa phác đồ Progestin-primed ovarian stimulation (PPOS) và phác đồ GnRH antagonist không cho thấy sự khác biệt có ý nghĩa thống kê về tỷ lệ hình thành SERa, khẳng định rằng chính cường độ đáp ứng nội tiết của từng cá thể chứ mới là yếu tố quyết định đến tỷ lệ hình thành SERa[11].
-
Tác động của SERa đến động học phôi và di truyền
Đa số các nghiên cứu hồi cứu, bao gồm cả báo cáo của Zhang và cộng sự (2023) đều đồng thuận rằng noãn SERa(+) có xu hướng giảm nhẹ tỷ lệ thụ tinh bình thường (2PN) so với noãn SERa(-) [6, 13]. Điều này hoàn toàn phù hợp với bản chất sinh học đã phân tích: do rối loạn kho chứa Canxi, sóng Ca2+ không đủ biên độ để hoạt hóa noãn hoàn toàn[10].
Một nghiên cứu đột phá của Li và cộng sự (2025) đã phân tích các chu kỳ chia đôi noãn để làm cả IVF cổ điển (cIVF) và ICSI ở bệnh nhân có SERa[14]. Kết quả cho thấy, đối với noãn SERa(+), việc sử dụng cIVF có thể mang lại tỷ lệ tạo phôi phân chia chất lượng cao tốt hơn so với ICSI[14]. Điều này được lý giải bằng việc cIVF cho phép tinh trùng tự xâm nhập và kích hoạt noãn một cách sinh lý, tránh được việc đâm kim vi tiêm có nguy cơ phá vỡ cấu trúc cơ học của đĩa SER vốn đã mong manh[14]. Mặc dù vậy, theo một phân tích gộp của Yuan và cộng sự (2026), sự hiện diện của SERa nhìn chung không làm giảm tỷ lệ hình thành phôi nang nếu noãn đã thụ tinh thành công[13].
Tính an toàn di truyền của phôi có nguồn gốc từ noãn SERa là mối bận tâm lớn nhất dẫn đến khuyến cáo loại bỏ của Istanbul 2011[1, 15]. Tuy nhiên, các phân tích PGT-A hiện đại đã mang lại những góc nhìn trái chiều. Nghiên cứu đoàn hệ hồi cứu của Kong và cộng sự (2024) phân tích các phôi nang có nguồn gốc từ noãn SERa và báo cáo rằng tỷ lệ phôi nguyên bội giảm đáng kể[15]. Sự xáo trộn chức năng của ty thể và màng lưới nội chất có thể ảnh hưởng đến quá trình lắp ráp thoi vô sắc dẫn đến các lỗi phân ly nhiễm sắc thể[15, 16]. Trái ngược hoàn toàn, công trình nghiên cứu của Xu và cộng sự (2022)[17] và nhiều báo cáo khác[13] lại chứng minh rằng noãn chứa SERa hoàn toàn không tác động tiêu cực đến tỷ lệ phôi nguyên bội. Phôi nang phát triển thành công từ noãn SERa(+) có cơ hội mang bộ nhiễm sắc thể bình thường tương đương với phôi từ noãn SERa(-)[17]. Sự mâu thuẫn này cho thấy SERa có thể chỉ là một chỉ điểm hình thái của stress tế bào và phôi có cơ chế “tự sửa chữa” trong quá trình phát triển kéo dài đến giai đoạn phôi nang.
-
Các kết quả lâm sàng
Phân tích gộp mới nhất của Yuan và cộng sự (2026) bao gồm 17.001 chu kỳ SERa(-) và 2.336 chu kỳ SERa(+) đã cung cấp bằng chứng mạnh mẽ nhất hiện nay[13]. Phân tích này khẳng định không có sự khác biệt có ý nghĩa thống kê về tỷ lệ thai lâm sàng, tỷ lệ sảy thai và tỷ lệ trẻ sinh sống (Live birth rate – LBR) giữa hai nhóm[13]. Đáng chú ý, một nghiên cứu chi tiết tại Việt Nam của Nguyen Thanh và cộng sự (2024)[18] cho thấy LBR ở nhóm bệnh nhân có noãn SERa thậm chí còn cao hơn có ý nghĩa thống kê so với nhóm không có SERa (57,7% vs 43,9%, p=0,045). Mặc dù các phôi được chuyển đa phần đến từ noãn SERa(-) trong cùng một chu kỳ (sibling oocytes), kết quả này nhấn mạnh rằng sự hiện diện của SERa ở một hoặc một vài noãn không đồng nghĩa với một “chu kỳ hỏng” hay làm giảm chất lượng của toàn bộ buồng trứng[5, 18].
Mặc dù LBR rất khả quan, các rủi ro dài hạn ở trẻ sơ sinh cũng không thể bỏ qua. Một phân tích gộp quan trọng của Long và cộng sự (2024) đã tập trung đánh giá về rủi ro dị tật bẩm sinh[19]. Nghiên cứu chỉ ra rằng nguy cơ mắc các dị tật bẩm sinh nghiêm trọng ở trẻ sinh ra từ các chu kỳ có noãn SERa cao hơn đáng kể (RR = 2,17 cho toàn bộ chu kỳ và RR = 3,53 cho riêng phôi từ noãn SERa+) so với nhóm chứng[19].
Về mặt sinh học, nguyên nhân có thể do sự bất thường trong môi trường nội bào hoặc các rối loạn dấu ấn sinh học như hội chứng Beckwith-Wiedemann[19]. Điều này cho thấy, mặc dù tỷ lệ làm tổ bình thường, sự bất thường của màng SER trong giai đoạn hình thành hợp tử có thể để lại “vết sẹo” biểu sinh (epigenetic scars) bộc lộ ở giai đoạn thai nhi. Bằng chứng này chính là lý do ESHRE 2025 vẫn giữ mã “màu vàng” thận trọng đối với SERa[4].
-
Cập nhật đồng thuận ESHRE/Alpha 2024-2025 và chiến lược xử trí tại labo IVF
Sau một thập kỷ tranh cãi, cập nhật đồng thuận ESHRE/Alpha 2024-2025 đã chính thức ban hành các hướng dẫn thay thế[4]. Thay vì quy định loại bỏ của năm 2011, đồng thuận mới tuyên bố: “Các noãn biểu hiện SERa có thể được sử dụng lâm sàng, dựa trên việc đánh giá từng trường hợp cụ thể (case-by-case)”[4]. Phôi có nguồn gốc từ noãn SERa được xếp vào nhóm ưu tiên thấp hơn trong việc lựa chọn chuyển phôi so với phôi từ noãn bình thường[4, 16].
Để tối đa hóa cơ hội cho bệnh nhân nhưng vẫn kiểm soát rủi ro, các labo IVF hiện đại nên áp dụng các chiến lược phù hợp. Khi bắt buộc phải làm ICSI trên noãn SERa(+), chuyên viên phôi học nên tránh đặt kim tiêm hoặc hút bào tương trực tiếp vào khu vực đĩa SERa. Sự phá vỡ cơ học cấu trúc này sẽ kích hoạt việc xả Canxi ồ ạt, dẫn đến thoái hoá noãn ngay lập tức[3, 7]. Các báo cáo gần đây chỉ ra tầm quan trọng của hệ thống nuôi cấy liên tục (Time-lapse Technology - TLT) kết hợp với trí tuệ nhân tạo (AI) trong việc theo dõi động học phân chia của phôi[20]. Thay vì chỉ quan sát hình thái tĩnh, TLT giúp labo theo dõi được cả các phôi có hiện tượng phân chia hỗn loạn từ sớm, vốn rất dễ xảy ra ở noãn có cấu trúc tế bào chất bất ổn[4, 20]. Ở các bệnh nhân có cả noãn SERa(+) và SERa(-), luôn ưu tiên thụ tinh và chuyển phôi từ noãn SERa(-) trước[4]. Ở những chu kỳ có nhiều noãn SERa(+), chiến lược chia đôi phác đồ IVF-ICSI có thể được cân nhắc theo khuyến cáo của Li và cộng sự (2025) để giảm thiểu áp lực cơ học lên tế bào[14].
-
Kết luận
Sự tồn tại của SERa trong noãn là một hiện tượng phản ánh tình trạng stress nội bào do sự tăng sinh màng lipid quá mức dưới tác động của phác đồ kích thích buồng trứng và môi trường vi nang noãn bất lợi[11, 12]. Từ việc bị coi là một “án tử” buộc phải vứt bỏ theo Đồng thuận 2011[1], y học thực chứng đã trả lại giá trị thực sự cho noãn SERa. Các dữ liệu lâm sàng mới nhất và Đồng thuận ESHRE/Alpha 2024-2025 khẳng định rằng phôi có nguồn gốc từ noãn SERa hoàn toàn có khả năng phát triển thành những em bé khỏe mạnh với tỷ lệ sinh sống tương đương[4].
Tuy nhiên, SERa không hoàn toàn vô hại. Sự suy giảm tỷ lệ thụ tinh, nguy cơ thoái hoá khi ICSI, và đặc biệt là sự gia tăng rủi ro dị tật bẩm sinh (theo Long và cộng sự, 2024) đòi hỏi phải luôn xếp các phôi từ noãn SERa ở mức độ ưu tiên thấp và tư vấn kỹ lưỡng cho bệnh nhân.
Tài liệu tham khảo:
[1] Alpha Scientists in Reproductive Medicine and ESHRE SIG of Embryology. The Istanbul consensus workshop on embryo assessment: proceedings of an expert meeting. Hum Reprod. 2011;26(6):1270-1283.
[2] Otsuki J, Okada A, Morimoto K, et al. The relationship between pregnancy outcome and smooth endoplasmic reticulum clusters in MII human oocytes. Hum Reprod. 2004;19(7):1591-1597.
[3] Restelli L, Delle Noci S, Mangiarini A, et al. The impact of Alpha/ESHRE consensus regarding oocytes with aggregates of smooth endoplasmic reticulum (SERa) on in vitro fertilization outcome. J Assist Reprod Genet. 2015;32(11):1629-1635.
[4] Coticchio G, Ahlström A, Arroyo G, et al. The Istanbul Consensus update: a revised ESHRE/ALPHA consensus on oocyte and embryo static and dynamic morphological assessment. Hum Reprod. 2025;00(0):1-47.
[5] Hattori H, Nakamura Y, Nakajo Y, et al. Deliveries of babies with normal health derived from oocytes with smooth endoplasmic reticulum clusters. J Assist Reprod Genet. 2014;31(11):1461-1467.
[6] Zhang Z, Liu XN, Wang Y, et al. Real value of the oocytes with smooth endoplasmic reticulum aggregates in in vitro fertilization/intracytoplasmic sperm injection cycle: a retrospective cohort study. Reprod Dev Med. 2023;7(3):142-148.
[7] Patro P, Bhadora V. Oocyte Abnormalities and Smooth Endoplasmic Reticulum Aggregates: A Comprehensive Review. Naturalista Campano. 2024;28(1).
[8] Sá R, Cunha M, Silva J, et al. Ultrastructure of tubular smooth endoplasmic reticulum aggregates in human metaphase II oocytes and clinical implications. Fertil Steril. 2011;96(1):143-149.
[9] Van Blerkom J. Mitochondrial function in the human oocyte and embryo and their role in developmental competence. Mitochondrion. 2011;11:797-813.
[10] Stigliani S, Moretti S, Casciano I, et al. Presence of aggregates of smooth endoplasmic reticulum in MII oocytes affects oocyte competence: Molecular-based evidence. Mol Hum Reprod. 2018;24(6):362-370.
[11] Gashti NG, Hosseini SZ, Qasemi M, et al. Smooth endoplasmic reticulum aggregates in human oocytes are related to female infertility etiology and diminished reproductive outcomes. Sci Rep. 2025;15(1):7160.
[12] Clark ZL, Ruebel M, Schall PZ, et al. Follicular Hyperstimulation Dysgenesis: New Explanation for Adverse Effects of Excessive FSH in Ovarian Stimulation. Endocrinology. 2022;163(9):bqac100.
[13] Yuan B, Wang J, Mao J. Impact of smooth endoplasmic reticulum aggregates in oocytes on embryo development and clinical outcomes in ICSI cycles: a meta-analysis. 2026.
[14] Li Y, Hu J, Lu H, et al. Oocytes with aggregates of smooth endoplasmic reticulum may not affect reproductive outcomes in split IVF-ICSI insemination: a retrospective study. Front Endocrinol. 2025;16:1567066.
[15] Kong X, Pan J, Liang S, et al. Blastocysts originated from oocytes with smooth endoplasmic reticulum aggregates have a reduced euploidy rate: a retrospective cohort study. Front Endocrinol. 2024;15:1425578
[16] Bartolacci A, Intra G, Coticchio G, et al. Does morphological assessment predict oocyte developmental competence? A systematic review and proposed score. J Assist Reprod Genet. 2022;39:3-17.
[17] Xu J, Yang L, Chen ZH, et al. Oocytes With Smooth Endoplasmic Reticulum Aggregates May Not Impact Blastocyst Euploidy Rate. Front Endocrinol. 2022;13:851370.
[18] Nguyen Thanh T, Nguyen DM, Dinh Le T, et al. The Relationship Between Smooth Endoplasmic Reticulum Clusters in Metaphase II Oocytes and Embryological and Birth Outcomes in Infertile Couples. J Assist Reprod Genet. 2024
[19] Long R, Wang M, Yang Q, et al. Smooth endoplasmic reticulum aggregates in oocytes associated with increased risk of neonatal birth defects: A meta-analysis. Acta Obstet Gynecol Scand. 2024;103:2163-2170.
[20] Chavez-Badiola A, Mendizabal-Ruiz G, Flores-Saiffe Farias A, et al. Automated oocyte retrieval, denudation, sperm preparation, and ICSI in the IVF laboratory: a proof-of-concept study and report of the first live births. Hum Reprod. 2026;41(2):214-230.