Nội dung chính
Hiện nay trong lĩnh vực hỗ trợ sinh sản (HTSS), trong khi việc kiểm tra và phân loại phôi (embryo grading) đã được tiêu chuẩn hóa thông qua các tiêu chí quốc tế, thì việc đánh giá chất lượng noãn (oocyte morphology grading) lại mang tính chủ quan và chưa được chuẩn hóa đồng bộ[1]. Các chuyên viên phôi học hiện đại nhận ra rằng việc quan sát hình thái noãn dưới kính hiển vi đảo ngược là một công cụ tiên lượng vô cùng giá trị. Phương pháp này sở hữu những ưu điểm vượt trội: chi phí thấp, hoàn toàn không xâm lấn, không làm tổn thương giao tử và dễ dàng tích hợp vào quy trình làm việc thường quy của phòng labo[2].
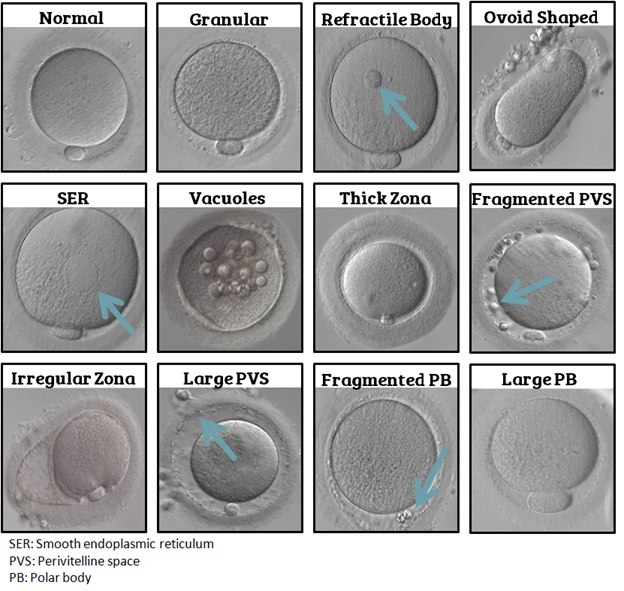
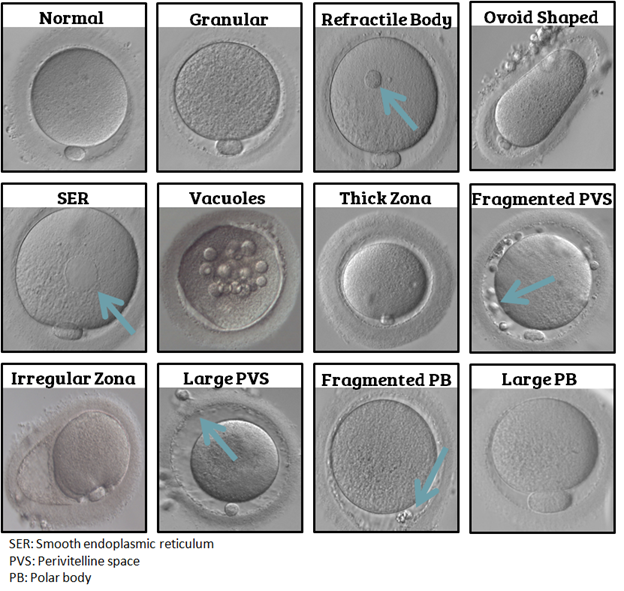
Một noãn trưởng thành đạt chuẩn lý tưởng (ở kỳ giữa giảm phân II - Metaphase II) được mô tả là phải có khối bào tương đồng nhất, thể cực thứ nhất (PB1) nguyên vẹn, màng trong suốt (ZP) có độ dày thích hợp và khoang quanh noãn (PVS) hẹp[1, 3]. Tuy nhiên trong thực tiễn lâm sàng, các biến đổi hình thái bất thường xuất hiện vô cùng phổ biến trong các chu kỳ kích thích buồng trứng[1]. Các tổ chức uy tín (như Alpha Scientists và ESHRE) đã phân loại những bất thường này thành hai nhóm chính: các bất thường ngoại bào (như biến đổi ở PB1, PVS, ZP) thường phản ánh sự lão hóa của noãn hoặc tác động của môi trường nuôi cấy in-vitro; và các bất thường nội bào (như sự xuất hiện của cụm lưới nội chất trơn SER hay không bào) có thể ảnh hưởng đến sự phát triển của phôi[4].
-
- Phức hợp noãn - tế bào hạt (Cumulus Oocyte Complex - COC)
Khối tế bào hạt (Cumulus cells) bao quanh noãn đóng vai trò cung cấp năng lượng, trao đổi chất và tạo hàng rào bảo vệ noãn khỏi các gốc oxy tự do (Reactive Oxygen Species - ROS). Các tế bào hạt tiết ra axit hyaluronic làm cho khối tế bào hạt giãn nở, đặc trưng ở những noãn đã trưởng thành hoàn toàn (MII)[3].
Nghiên cứu của Zhou và cộng sự (2014) trên mô hình noãn giai đoạn GV (Germinal Vesicle) đã chứng minh độ dày của lớp tế bào hạt có mối tương quan tuyến tính với khả năng phát triển của noãn. Những noãn có lớp tế bào hạt dày ( ≥ 50 μm) đạt tỷ lệ trưởng thành nhân lên tới 100%, tỷ lệ thụ tinh là 71,88% và khả năng phát triển thành phôi nang đạt 64,35%[5]. Ngược lại, khi lớp tế bào hạt mỏng (< 30 μm), tỷ lệ thụ tinh giảm mạnh chỉ còn 22,22% và không có phôi nào phát triển được tới giai đoạn phôi nang. Việc cố tình dùng lực cơ học để loại bỏ bớt lớp tế bào hạt cũng làm giảm đáng kể khả năng thụ tinh và phát triển phôi[5]. Điều này khẳng định lớp tế bào hạt kiểm soát trực tiếp sự trưởng thành của bào tương (cytoplasmic maturation) – yếu tố cốt lõi để phôi phân chia sau này[1, 5].
-
- Màng trong suốt (Zona Pellucida - ZP)
Màng ZP cấu tạo từ các glycoprotein, được tiết ra từ cả noãn và các tế bào hạt. Ở người, độ dày bình thường của ZP dao động từ 15 đến 20 μm, trung bình khoảng 17-18 μm[3]. Màng ZP đóng vai trò kiểm soát sự xâm nhập của tinh trùng và ngăn chặn hiện tượng đa thụ tinh.
Độ dày của ZP ảnh hưởng trực tiếp đến khả năng tinh trùng đâm xuyên. Những noãn có ZP mỏng (dưới 18,6 μm) thường cho tỷ lệ thụ tinh tốt nhất[1]. Tuy nhiên, nếu ZP quá dày ( ≥ 22 μm đến 25 μm), tinh trùng sẽ gặp khó khăn rất lớn khi đâm xuyên, do đó thường cần chỉ định kỹ thuật ICSI kết hợp hỗ trợ thoát màng bằng laser[1, 3]. Bên cạnh đó, hiện tượng màng ZP tách lớp (zona splitting) hoặc có bề mặt sần sùi, gồ ghề thường liên quan đến những chu kỳ điều trị thất bại. Bản chất của các bất thường này có thể do tổn thương cơ học trong quá trình thao tác hoặc do sự gián đoạn trong việc tổng hợp các protein khuôn mẫu cấu trúc trong giai đoạn noãn phát triển[1].
-
- Khoang quanh noãn (Perivitelline Space - PVS)
Khoang quanh noãn là khoảng không gian nằm giữa màng bào tương và màng ZP. Trong điều kiện sinh lý bình thường, PVS chỉ đủ rộng để chứa thể cực thứ nhất. Tuy nhiên, sự gia tăng kích thước khoang này (Large PVS - LPVS) là một biomarker phản ánh sự thay đổi bên trong cấu trúc noãn[6].
Sự mở rộng của PVS là kết quả của hiện tượng co rút bào tương (cytoplasmic retraction). Khi noãn bị lão hóa hoặc chịu áp lực stress từ môi trường, mạng lưới khung xương tế bào (đặc biệt là mạng lưới sợi actin vỏ) bị thoái hóa, đứt gãy khiến màng bào tương mất khả năng bám chặt vào lớp ZP[6, 7]. Đồng thời, sự suy giảm chức năng ty thể làm sụt giảm năng lượng ATP, khiến các bơm ion trên màng hoạt động kém làm bào tương mất đi áp suất trương dẫn đến mất nước và co lại[6]. Để phản ứng lại stress, noãn còn tăng tiết axit hyaluronic (HA) vào PVS. Bản chất hút nước mạnh của HA kéo nước từ bên ngoài vào, càng làm khoang này giãn nở bất thường[6].
Hệ quả lâm sàng của LPVS rất nghiêm trọng. Màng bào tương lỏng lẻo làm cho việc đâm kim khi ICSI trở nên khó kiểm soát, dễ làm vỡ màng noãn. Thêm vào đó, PVS rộng làm mất đi sự neo giữ cơ học đối với thoi vô sắc, khiến thoi vô sắc bị lệch vị trí, dẫn đến lỗi phân bào và tăng nguy cơ phôi lệch bội (aneuploidy). Nếu PVS rộng đi kèm với sự xuất hiện của các hạt mảnh vỡ (debris), đó là tiên lượng rất xấu cho sự phát triển của phôi[6].
-
- Thể cực thứ nhất (First Polar Body - PB1)
Sự hiện diện của thể cực thứ nhất xác nhận noãn đã hoàn thành giảm phân 1 và đạt đến giai đoạn MII. Một PB1 lý tưởng có hình tròn hoặc ovoid, bề mặt nhẵn và chiếm khoảng 5% thể tích tế bào noãn[1, 3].
Các bất thường ở thể cực bao gồm PB1 khổng lồ (Giant PB1) hoặc PB1 phân mảnh. Thể cực khổng lồ thường xuất phát từ sự sai lệch vị trí của thoi vô sắc, khiến noãn bị mất đi một lượng lớn bào tương trong quá trình đẩy thể cực[1]. Về PB1 phân mảnh, mặc dù từng bị đánh giá là làm giảm chất lượng phôi, các dữ liệu mới hơn cho thấy hình thái PB1 thay đổi rất nhanh chóng theo thời gian nuôi cấy in-vitro. Do đó, một PB1 phân mảnh có thể chỉ đơn thuần phản ánh sự lão hóa sau phóng noãn (post-ovulatory aging) do thời gian chờ ICSI kéo dài, chứ không hoàn toàn đại diện cho những sai hỏng di truyền nội tại của noãn[1, 8].
Đường kính tiêu chuẩn của một noãn tiền phóng noãn (bao gồm cả màng ZP và PVS) khoảng 150 μm. Sự sai lệch về kích thước noãn có ý nghĩa lâm sàng. Noãn khổng lồ (Giant oocytes) có kích thước lớn gấp đôi bình thường, phát sinh do lỗi trong quá trình phân chia bào tương. Những noãn này chứa bộ nhiễm sắc thể tứ bội (tetraploid) và nếu thụ tinh sẽ tạo ra phôi tam bội (digynic triploidy), không có khả năng phát triển thành thai nhi bình thường và thường bị loại bỏ[1].
Noãn dính liền (Conjoined oocytes) là hiện tượng hai noãn chia sẻ chung một lớp màng ZP. Rất hiếm khi cả hai noãn này cùng thụ tinh bình thường và y văn chưa ghi nhận ca mang thai thành công nào từ dạng noãn này[1].
Noãn hình bầu dục (Ovoid oocytes) dù hình dạng méo mó, những noãn này vẫn có khả năng thụ tinh và sinh ra em bé khỏe mạnh. Tuy nhiên, màng ZP hình bầu dục có thể ép các phôi bào phân chia theo một trục phẳng, làm giảm diện tích tiếp xúc giữa các tế bào dẫn đến chậm quá trình hình thành khoang phôi nang[1].
Bên trong màng bào tương là một hệ thống bào quan phức tạp. Các bất thường nội bào được tổ chức Alpha Scientists và ESHRE đánh giá là nghiêm trọng hơn rất nhiều so với ngoại bào vì phản ánh trực tiếp khả năng chuyển hóa và năng lượng của noãn.
-
- Độ hạt của bào tương
Hiện tượng xuất hiện các hạt tập trung ở trung tâm bào tương (Centrally Located Cytoplasmic Granulation - CLCG) là một biến đổi hình thái rất phổ biến sau quá trình kích thích buồng trứng[1, 10]. Một số nghiên cứu cho rằng hiện tượng này chỉ là phản ứng sinh lý đối với nồng độ gonadotropin cao, hoàn toàn không ảnh hưởng đến tỷ lệ thụ tinh, tốc độ phân chia hay tỷ lệ hình thành phôi nang[1, 10]. Các phân tích gộp cũng chỉ ra rằng noãn có chứa hạt bào tương nhìn chung vẫn đạt tỷ lệ thụ tinh cao hơn những noãn hoàn toàn không có bất kỳ hạt nào[11]. Tuy nhiên, noãn CLCG có thể dẫn đến sự hình thành tiền nhân bất thường và gia tăng tỷ lệ phôi phân mảnh[1, 11].
-
- Không bào
Không bào là những túi chứa dịch xuất hiện trong bào tương, được hình thành do sự dung hợp của các túi vận chuyển từ bộ máy Golgi và lưới nội chất trơn và xuất hiện ở 5 – 12% số noãn[1]. Sự hiện diện của không bào làm suy giảm đáng kể khả năng phát triển của phôi[1, 3]. Đặc biệt, những không bào có đường kính lớn (hơn 14 μm) có thể chiếm không gian quá lớn trong bào tương, gây chèn ép cơ học thoi vô sắc và ảnh hưởng đến quá trình thụ tinh[1].
-
- Lưới nội chất trơn dạng cụm (Smooth Endoplasmic Reticulum Clusters - SERc)
Lưới nội chất trơn dạng cụm được xem là một trong những bất thường hình thái nghiêm trọng nhất. Dưới kính hiển vi, cụm SER có hình dạng như những đĩa phẳng, hình elip mờ và không chứa dịch bên trong[1]. Lưới nội chất trơn đóng vai trò là “kho dự trữ canxi” của tế bào. Quá trình thụ tinh đòi hỏi tinh trùng phải kích hoạt các “dao động canxi” (calcium oscillations) để noãn hoàn tất giảm phân. Sự vón cục của lưới nội chất trơn làm phá vỡ cơ chế giải phóng canxi này[1].
Lo ngại những rủi ro về kết quả sản khoa kém, tài liệu đồng thuận The Istanbul consensus (ESHRE, 2011) từng khuyến cáo tuyệt đối không nên thực hiện ICSI trên noãn có chứa cụm SER[9]. Tuy nhiên, các nghiên cứu gần đây đã ghi nhận một số trường hợp em bé khỏe mạnh được sinh ra từ noãn có cụm SER. Khuyến cáo tuyệt đối trên tuy đã được nới lỏng, nhưng các noãn mang SERc vẫn cần được theo dõi một cách cẩn trọng[1, 12].
Theo lý thuyết, sự hiện diện của thể cực thứ nhất được xem là dấu hiệu noãn đã trưởng thành. Tuy nhiên, các nghiên cứu sâu hơn đã chỉ ra rằng sự tồn tại và vị trí của thoi vô sắc mới là tiêu chuẩn xác thực độ trưởng thành chính xác nhất[14, 15].
Việc sử dụng kính hiển vi ánh sáng phân cực (polarized light microscopy - PolScope) cho phép quan sát trực tiếp thoi vô sắc ở noãn mà không làm tổn thương tế bào[14]. Một phân tích gộp (meta-analysis) của Petersen và cộng sự (2009) trên 10 thử nghiệm lâm sàng với hàng ngàn noãn đã chứng minh tầm quan trọng của cấu trúc này[14]. Kết quả cho thấy tỷ lệ thụ tinh ở nhóm noãn quan sát được thoi vô sắc cao hơn hẳn nhóm không thấy thoi vô sắc (75,6% so với 61,5%, P < 0,0001). Bên cạnh đó, tỷ lệ phôi phân chia (63,1% so với 43,9%, P < 0,0001), số lượng phôi chất lượng tốt ngày 3 (37,3% so với 28%, P = 0,003) và đặc biệt khả năng phát triển thành phôi nang ở ngày 5 (50,7% so với 28,6%, P < 0,0001) đều vượt trội hoàn toàn khi thoi vô sắc hiện diện rõ ràng[14].
Bên cạnh đó, góc lệch giữa thoi vô sắc và PB1 đóng vai trò quyết định. Thông thường thoi vô sắc và PB1 nằm sát nhau (góc 0-5 độ). Tuy nhiên, nếu góc lệch này lớn hơn 90 độ, tỷ lệ thụ tinh bình thường sẽ giảm nghiêm trọng và làm tăng nguy cơ hình thành phôi bất thường có 3 tiền nhân (tripronucleated zygotes) do thoi vô sắc bị tổn thương khi chuyên viên phôi học đâm kim ICSI một cách “mù”[1].
Việc đánh giá chất lượng noãn thông qua các tiêu chuẩn hình thái ngoại bào, nội bào và cấu trúc thoi vô sắc đóng vai trò như một lăng kính phản chiếu sức khỏe sinh sản vi mô của bệnh nhân. Trong khi các khiếm khuyết ngoại bào có thể là kết quả của sự lão hóa in-vitro, các khiếm khuyết nội bào nghiêm trọng (như cụm SER, không bào khổng lồ, co rút bào tương gây LPVS) lại trực tiếp ảnh hưởng đến tiềm năng phân chia nhiễm sắc thể và sự phát triển của phôi. Việc chuẩn hóa và xây dựng hệ thống chấm điểm noãn sẽ giúp bác sĩ lâm sàng cá nhân hóa phác đồ điều trị, tối ưu hóa cơ hội làm mẹ cho bệnh nhân.
[1] Sy EC. A Case for the Oocyte: Why Grading of Oocyte Morphology Should Be Implemented in the IVF Laboratory and How. Philipp J Reprod Endocrinol Infertil. 2024;21(2):59-71.
[2] Zhou HX, Ma YZ, Liu YL, Chen Y, Zhou CJ, Wu SN, et al. Assessment of Mouse Germinal Vesicle Stage Oocyte Quality by Evaluating the Cumulus Layer, Zona Pellucida, and Perivitelline Space. PLoS One. 2014;9(8):e105812.
[3] Hassa H, Aydin Y, Taplamacioglu F. The role of perivitelline space abnormalities of oocytes in the developmental potential of embryos. J Turk Ger Gynecol Assoc. 2014;15(3):161-3.
[4] Reviva IVF. Oocyte Grading: Understanding Egg Quality for IVF Success.
[5] Petersen CG, Oliveira JBA, Mauri AL, Massaro FC, Baruffi RLR, Pontes A, et al. Relationship between visualization of meiotic spindle in human oocytes and ICSI outcomes: a meta-analysis. Reprod Biomed Online. 2009;18(2):235-43.
[6] Delimitreva S, Chakarova I. How Cytoskeletal Disorders Contribute to Errors in the Chromosomal Segregation of Oocytes and Cleavage Stage Embryos. J Dev Biol. 2025;13(4):43.
[7] Voros C, Sapantzoglou I, Athanasiou D, Varthaliti A, Mavrogianni D, Bananis K, et al. Molecular Guardians of Oocyte Maturation: A Systematic Review on TUBB8, KIF11, and CKAP5 in IVF Outcomes. Int J Mol Sci. 2025;26(13):6390.
[8] Rienzi L, Vajta G, Ubaldi F. Predictive value of oocyte morphology in human IVF: a systematic review of the literature. Hum Reprod Update. 2010;17(1):34-45.
[9] Alpha Scientists in Reproductive Medicine and ESHRE Special Interest Group of Embryology. The Istanbul consensus workshop on embryo assessment: proceedings of an expert meeting. Hum Reprod. 2011;26(6):1270-83.
[10] Rienzi L, Ubaldi FM, Iacobelli M, Minasi MG, Romano S, Ferrero S, et al. Significance of metaphase II human oocyte morphology on ICSI outcome. Fertil Steril. 2008;90(5):1692-700.
[11] Ebner T, Moser M, Shebl O, Sommerguber M, Tews G. Prognosis of oocytes showing aggregation of smooth endoplasmic reticulum. Reprod Biomed Online. 2008;16(1):113-18.
[12] Fancsovits P, Tóthné ZG, Murber Á, Rigó J Jr, Urbancsek J. Importance of cytoplasmic granularity of human oocytes in in vitro fertilization treatments. Acta Biol Hung. 2012;63:189-201.
[13] Ten J, Mendiola J, Vioque J, de Juan J, Bernabeu R. Donor oocyte dysmorphisms and their influence on fertilization and embryo quality. Reprod Biomed Online. 2007;14(1):40-8.
[14] Figueira R, Braga D, Semiao-Francisco L, Madaschi C, Iaconelli A Jr, Borges E Jr. Metaphase II human oocyte morphology: contributing factors and effects on fertilization potential and embryo developmental ability in ICSI cycles. Fertil Steril. 2010;94(3):1115-7.
[15] Otsuki J, Nagai Y, Chiba K. Lipofuscin bodies in human oocytes as an indicator of oocyte quality. J Assist Reprod Genet. 2007;24:263-70.