CNSH. Lê Thị Quỳnh, ThS. Trương Thị Thanh Bình, ThS. BS. Dương Công Bằng
Bệnh viện Phụ sản Quốc tế Sài Gòn
1. Mở đầu
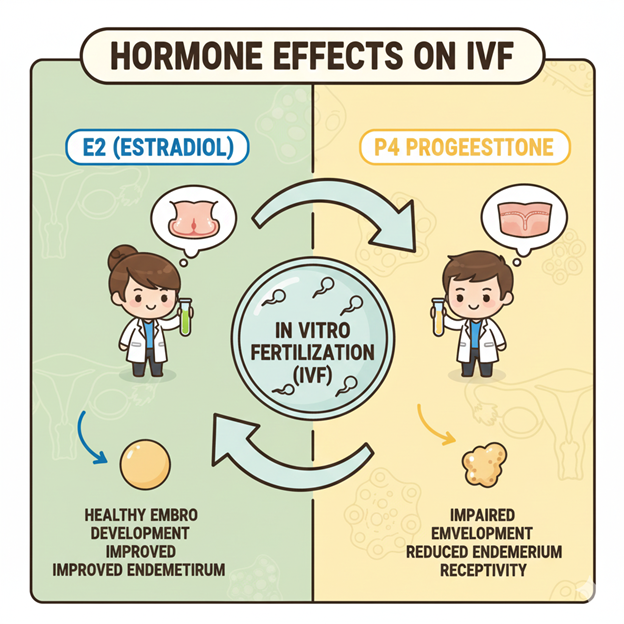
Kết quả điều trị Thụ tinh trong ống nghiệm (TTTON) thành công dựa trên sự kết hợp phức tạp giữa quá trình điều hòa nội tiết trên lâm sàng (in vivo) và môi trường nuôi cấy trong phòng thí nghiệm (lab) (in vitro). Mặc dù chuyên viên phôi học (CVPH) không can thiệp trực tiếp vào quá trình điều chỉnh nồng độ nội tiết tố của bệnh nhân, tuy nhiên việc am hiểu cơ chế tác động của các hormone steroid - chủ yếu là Estradiol (E2) và Progesterone (P4) - là nền tảng để tối ưu hóa môi trường nuôi cấy nhằm đảm bảo khả năng phát triển và tiềm năng làm tổ của phôi sau đó.
Môi trường nuôi cấy thương mại được thiết kế để mô phỏng chức năng sinh lý của dịch nang noãn và dịch ống dẫn trứng. Do đó, việc kiểm soát nghiêm ngặt các yếu tố như nhiệt độ, pH, áp suất thẩm thấu[1] trong phòng lab là nhiệm vụ rất quan trọng của CVPH nhằm giảm thiểu stress cho phôi. Noãn thu nhận được từ môi trường in vivo có thể đã chịu ảnh hưởng của hormone nội tiết[2] (ví dụ: tăng P4 sớm), do đó sự ổn định của môi trường lab sẽ hỗ trợ tối đa khả năng phục hồi và phát triển của noãn/phôi.
Mục tiêu chính của bài viết này là cung cấp một góc nhìn từ phía CVPH về vai trò gián tiếp nhưng quan trọng của hormone steroid đối với chất lượng noãn và phôi trong điều trị TTTON. Bài viết sẽ phân tích các cơ chế phân tử mà E2 và P4 tác động lên khả năng thụ tinh của noãn và sự tiếp nhận của nội mạc tử cung (NMTC). Từ đó, đề xuất các chiến lược cho CVPH để đánh giá noãn dựa trên chỉ dấu gián tiếp của môi trường nội tiết và kiểm soát các yếu tố ngoại sinh (như EDCs/VOCs) nhằm tạo ra một môi trường vi mô lý tưởng, để góp phần tối ưu hóa hơn nữa kết quả điều trị TTTON.
2. Tác động của hormone lên noãn và phôi
2.1. Tác động lên noãn và môi trường nang noãn
Vai trò của Estradiol – E2
E2 là hormone steroid chính được tổng hợp bởi tế bào hạt của nang noãn. Khi nồng độ E2 đạt đỉnh, nó kích hoạt phản hồi dương lên trục Hạ đồi - Tuyến yên - Buồng trứng, dẫn đến đỉnh LH[3]. Đỉnh LH là tín hiệu khởi phát cho quá trình tái khởi động giảm phân của noãn thông qua việc giảm nồng độ cAMP nội bào[3].
E2 cũng thúc đẩy sự tăng sinh của tế bào cumulus, hình thành phức hợp noãn-cumulus (Cumulus Oocytes Complex - COC). Tính toàn vẹn hình thái học của COC là một dấu hiệu gián tiếp phản ánh nồng độ E2 và các yếu tố tăng trưởng trong môi trường nang noãn.
Vai trò của Progesterone – P4
P4 được tế bào cumulus sản xuất mạnh mẽ sau khi nhận tín hiệu trigger[4]. Sự gia tăng nồng độ P4 là điều kiện thiết yếu cho quá trình trưởng thành noãn bào, hay khả năng chuyển từ giảm phân I sang giảm phân II - trạng thái noãn có khả năng thụ tinh. Cơ chế hoạt động của P4 gián tiếp thông qua thụ thể progesterone màng (membrane Progesterone Receptor - mPR). Tín hiệu này được xem là một cơ chế non-genomic (không qua điều hòa gen), dẫn đến sự hoạt hóa yếu tố thúc đẩy trưởng thành (Maturation Promoting Factor - MPF) - một phức hợp enzyme kinase chính kích hoạt noãn chuyển sang pha giữa của quá trình giảm phân I. Hơn nữa, sự hiện diện của các thụ thể P4 trong tế bào cumulus cũng được cho là ảnh hưởng đến sự trưởng thành noãn và phát triển phôi về sau.
Đối với sinh lý của tinh trùng, P4 là một chất hóa hướng động (chemoattractant) mạnh, kích thích hoạt hóa, khả năng di chuyển và phản ứng cực đầu của tinh trùng[4].
Androgen và tác động lên noãn
Androgen là tiền chất cần thiết cho quá trình tổng hợp E2. Tuy nhiên, tăng androgen, đặc trưng ở bệnh nhân mắc hội chứng buồng trứng đa nang (Polycystic Ovary Syndrome - PCOS), có liên quan đến không phóng noãn và chất lượng noãn kém[5]. Các nghiên cứu trên mô hình động vật đã chỉ ra rằng việc điều trị androgen có tác động bất lợi, làm giảm tỷ lệ noãn trưởng thành và tỷ lệ thụ tinh[6] [7].
Mặt khác, ở phụ nữ có dự trữ buồng trứng giảm (Diminished Ovarian Reserve - DOR), một số bằng chứng cho thấy việc bổ sung DHEA có thể cải thiện môi trường buồng trứng, thậm chí làm giảm tỷ lệ lệch bội trong noãn[6]. Điều này cho thấy quá trình giảm phân và chất lượng tế bào noãn cực kỳ nhạy cảm với sự điều hòa về liều lượng và thời điểm của hormone steroid[8].
2.2. Tác động lên phôi
Ảnh hưởng trực tiếp
Phôi người ở giai đoạn tiền làm tổ có biểu hiện thụ thể progesterone. Các nghiên cứu đang tiếp tục làm rõ cách P4 có thể ảnh hưởng trực tiếp đến chuyển hóa và biểu hiện gen của phôi[9]. Tuy nhiên, bằng chứng về ảnh hưởng trực tiếp này hiện vẫn còn hạn chế.
Ảnh hưởng gián tiếp
Ảnh hưởng gián tiếp là cơ chế tác động mạnh mẽ nhất của hormone steroid lên kết cục điều trị TTTON. Nồng độ P4 tăng cao sớm (Premature Progesterone Elevation - PPE) trong huyết thanh đã được chứng minh là gây ra sự không đồng bộ giữa phôi và NMTC[9].
P4 cao tác động chủ yếu bằng cách thay đổi biểu hiện gen trong NMTC, làm thay đổi thành phần dịch tiết nội mạc. Sự thay đổi này khiến cửa sổ làm tổ (CSLT) bị đóng sớm[8] [10], ảnh hưởng đến sự làm tổ của phôi.
Khi có bằng chứng lâm sàng về PPE (ví dụ: P4 vượt ngưỡng 1,5–1,75 ng/ml ), CVPH cần phối hợp chặt chẽ với lâm sàng để chuyển sang chiến lược trữ phôi toàn bộ nhằm tách biệt quá trình phát triển phôi khỏi môi trường NMTC bị rối loạn nội tiết, gián tiếp tối ưu hóa kết quả IVF[8].
Sự liên quan giữa các phác đồ kích thích buồng trứng đến chất lượng noãn/phôi
Mức độ hormone steroid mà noãn và phôi tiếp xúc phụ thuộc đáng kể vào phác đồ kích thích buồng trứng (KTBT) và loại trigger được lựa chọn. Phác đồ sử dụng chất đồng vận GnRH (GnRHa trigger) thường được áp dụng nhằm ngăn ngừa hội chứng quá kích buồng trứng ở nhóm bệnh nhân nguy cơ cao (như PCOS)[7]. Phác đồ này tạo ra đỉnh LH ngắn và kéo theo sự suy giảm nhanh chóng của E2/P4 sau đó. Môi trường nội tiết này có thể liên quan đến tỷ lệ PPE thấp hơn so với phác đồ sử dụng chất đối vận GnRH, nhưng cũng có thể dẫn đến tình trạng môi trường nội tiết bên trong cơ thể thấp hơn so với sinh lý, đòi hỏi CVPH phải tối ưu hóa môi trường nuôi cấy in vitro ở mức độ cao hơn để bù đắp cho sự thiếu hụt các yếu tố tăng trưởng thường có.
Ngược lại, nghiên cứu của Levy R. và cộng sự (2002) đã chỉ ra rằng nồng độ hormone quá mức sinh lý của E2 trong các chu kỳ hiến noãn không được chứng minh là ảnh hưởng tiêu cực đến chất lượng noãn và phôi. Điều này cho thấy rằng noãn có chất lượng tốt có khả năng thích ứng cao hơn với những thay đổi E2 ngoại sinh. Việc hiểu rõ các biến động nội tiết cụ thể theo từng phác đồ KTBT giúp CVPH nhận thức được mức độ stress tiềm ẩn của noãn và chủ động điều chỉnh các điều kiện nuôi cấy, từ đó nâng cao chất lượng phôi và kết quả lâm sàng.
Tác động lên NMTC và khả năng làm tổ của phôi
Vai trò của hormone steroid không chỉ dừng lại ở chất lượng noãn và phôi mà còn là yếu tố quyết định sự tiếp nhận của NMTC - một điều kiện tiên quyết cho sự làm tổ thành công.
E2 đóng vai trò chính trong việc làm dày NMTC trong pha tăng sinh. Sau đó, E2 tác động phối hợp với P4 để điều chỉnh trạng thái tiếp nhận của NMTC. Các nghiên cứu, đặc biệt trên mô hình động vật, cho thấy nồng độ E2 nằm trong một phạm vi rất hẹp sẽ quyết định thời gian mở của CSLT. Nồng độ E2 quá cao có thể khiến NMTC nhanh chóng chuyển sang trạng thái không tiếp nhận sau CSLT, làm giảm khả năng làm tổ của phôi[11].
Trong các chu kỳ chuyển phôi đông lạnh sử dụng chu kỳ nhân tạo, việc bổ sung P4 ngoại sinh là bắt buộc để đồng bộ hóa NMTC và phôi. Ngưỡng P4 tối ưu trên ngày chuyển phôi là chủ đề nghiên cứu tích cực. Các nghiên cứu gần đây thường sử dụng ngưỡng từ 8,8 đến 9,2 ng/mL làm mức dưới để đảm bảo kết quả thai lâm sàng tốt. Việc duy trì sự đồng bộ phân tử giữa NMTC và phôi là yếu tố thiết yếu để làm tổ thành công[11].
3. Vai trò của chuyên viên phôi học
CVPH đóng vai trò quan trọng trong việc thiết lập môi trường lab tối ưu, kiểm soát các yếu tố gây nhiễu và chọn lọc phôi có khả năng phát triển cao nhất.
3.1. Đánh giá và phân loại noãn
CVPH với nhiều năm kinh nghiệm có thể đánh giá chất lượng và tiên lượng khả năng phát triển của phôi dựa trên phản ứng của tế bào cumulus của noãn với hormone in vivo.
Sự khác biệt giữa COC là rất quan trọng, mặc dù cả hai loại COC Compact và COC Expanded đều phản ánh nang noãn khỏe mạnh. Noãn được bao phủ bởi COC Compact - với lớp tế bào dày và chất nền ngoại bào (extracellular matrix) chặt chẽ - thường là dấu hiệu của nồng độ E2 tối ưu trong giai đoạn tiền trigger, cho thấy noãn được bảo vệ và nuôi dưỡng tốt. Những noãn này thường đạt tỷ lệ trưởng thành MII cao và có tiềm năng phát triển phôi chất lượng cao. Tuy nhiên, trạng thái tối ưu nhất thể hiện quá trình hoàn thiện noãn bào đã được kích hoạt là COC Expanded. COC Expanded, nơi các tế bào cumulus đã rời rạc và chất nền ngoại bào không chặt chẽ, phản ánh phản ứng hoàn hảo với tín hiệu trigger (LH hoặc P4) và là dấu hiệu cho thấy quá trình tiếp tục giảm phân đang diễn ra một cách thuận lợi, noãn đã chuẩn bị sẵn sàng cho quá trình thụ tinh. Nhóm này thường mang lại khả năng phát triển phôi tối ưu nhất. Tuy nhiên, COC bất thường (Irregular) - với số lượng tế bào cumulus ít và hình dạng không đều - gián tiếp cảnh báo về một môi trường nang noãn bất lợi, có thể do thiếu hụt E2 hoặc các yếu tố tăng trưởng khác trong quá trình phát triển nang noãn. Những noãn này có nguy cơ cho tỷ lệ trưởng thành và chất lượng phôi kém hơn[6].
Trong bối cảnh hiện nay, việc đánh giá hình thái COC đang được bổ sung thêm bằng các nghiên cứu về dấu ấn sinh học di truyền. Các gen như HAS2, VCAN, GDF-9, và PTGS2, được điều hòa bởi tín hiệu nội tiết, đang được phân tích trong tế bào cumulus để cung cấp các tiêu chí khách quan hơn trong việc dự đoán tiềm năng làm tổ và tỷ lệ thai lâm sàng. Phương pháp này hứa hẹn sẽ vượt qua những hạn chế của đánh giá hình thái truyền thống, cung cấp cơ sở dữ liệu vững chắc hơn cho quá trình chọn lọc phôi[12].
3.2. Tối ưu hoá môi trường nuôi cấy
Môi trường nuôi cấy thương mại được xây dựng để cung cấp đầy đủ các dưỡng chất cần thiết cho phôi, bao gồm axit amin, vitamin, và chất chống oxy hóa[5]. Tuy nhiên, các môi trường này thường được thiết kế ở dạng không chứa hormone steroid ngoại sinh để tránh bất kỳ sự can thiệp hoặc tác động khó lường nào lên thụ thể hormone của phôi[6].
Bên cạnh đó, CVPH phải đảm bảo nhiệt độ, pH, và áp suất thẩm thấu được kiểm soát liên tục theo nguyên tắc "Tip-to-Tip" (từ kim chọc hút đến catheter chuyển phôi). Việc duy trì nhiệt độ chính xác 37°C trong môi trường nuôi cấy là tối quan trọng để tránh stress nhiệt cho phôi gây rối loạn chuyển hóa[2].
Đồng thời, thiết kế lab và chất lượng không khí là yếu tố then chốt. Phòng lab cần áp dụng công nghệ phòng sạch, sử dụng vật liệu phát thải thấp, và tuân thủ các tiêu chuẩn nghiêm ngặt về kiểm soát chất lượng không khí[2].
3.3. Lựa chọn phôi chuyển/trữ
Việc lựa chọn phôi được thực hiện bằng cách sử dụng phân loại hình thái tiêu chuẩn hoặc hệ thống nuôi cấy time-lapse. Phôi có động học phát triển bình thường và hình thành phôi nang chất lượng cao là minh chứng cho khả năng vượt qua stress chuyển hóa từ môi trường nang noãn. CVPH cần nhận thức rằng sự bất thường về chất lượng phôi (ví dụ: tốc độ phân chia chậm, phân chia nhanh, tỷ lệ phân mảnh cao) có thể là kết quả trực tiếp của những thay đổi vi mô trong môi trường nội tiết tố của bệnh nhân.
4. Các vấn đề và hướng nghiên cứu liên quan
4.1. Thử nghiệm bổ sung hormone vào môi trường nuôi cấy
Việc bổ sung hormone ngoại sinh vào môi trường nuôi cấy vẫn là một lĩnh vực đang được nghiên cứu[4]. Tuy nhiên, các bằng chứng hiện tại chưa đủ mạnh để trở thành tiêu chuẩn lâm sàng. Ví dụ, việc hỗ trợ pha hoàng thể bằng P4 trong các chu kỳ chuyển phôi trữ bằng phác đồ chu kỳ tự nhiên không cho thấy sự khác biệt đáng kể về tỷ lệ thai lâm sàng[13]. Do đó, CVPH cần thận trọng, tránh can thiệp hormone steroid ngoại sinh vào môi trường nuôi cấy phôi, vì điều này có thể gây rối loạn các thụ thể steroid trên phôi một cách không mong muốn.
4.2. Ảnh hưởng của các chất gây rối loạn nội tiết (EDCs)
Mối đe dọa lớn nhất đối với tính toàn vẹn của môi trường lab là hóa chất gây rối loạn nội tiết (Endocrine-Disrupting Chemicals - EDCs), bao gồm hợp chất hữu cơ bay hơi (Volatile Organic Compounds - VOCs). EDCs can thiệp vào hoạt động của hormone steroid theo hai cơ chế chính.
Thứ nhất, EDCs kích hoạt các phản ứng giống với hormone sinh dục (đặc biệt là estrogen) khi liên kết với thụ thể steroid và kích hoạt phản ứng nội bào. Thứ hai, EDCs có thể tác động ức chế bằng cách ngăn chặn hormone sinh dục tự nhiên liên kết với thụ thể của chúng, dẫn đến rối loạn cân bằng nội tiết. Sự can thiệp kép này làm rối loạn trục Hạ đồi - Tuyến yên - Buồng trứng và các quá trình sinh lý quan trọng khác[10].
Tác động của VOCs lên hình thái phôi
VOCs, một nhóm EDCs phổ biến trong lab (phát thải từ vật tư tiêu hao làm bằng nhựa, keo dán), được xem là tác nhân gây ô nhiễm môi trường. Nghiên cứu chỉ ra rằng ngay cả khi tổng nồng độ VOCs thấp hơn khuyến nghị của Đồng thuận Cairo, nồng độ VOCs được giám sát theo thời gian thực vẫn liên quan tuyến tính đến các thông số phôi học bất lợi[1].
Sự gia tăng nồng độ VOCs trong thời gian nuôi cấy phôi liên quan đến việc giảm tỷ lệ phân chia sớm, giảm khả năng nén chặt của phôi Ngày 3 và tăng tỷ lệ tế bào lá nuôi phôi loại C (Grade C Trophectoderm). Sự tăng tỷ lệ phôi loại C còn đáng lo ngại hơn, vì nó chỉ ra sự rối loạn biệt hóa của lớp tế bào sẽ hình thành nhau thai, trực tiếp làm giảm tiềm năng làm tổ[1].
Chiến lược kiểm soát chất lượng
Để bảo vệ phôi khỏi các EDCs, CVPH phải triển khai các chiến lược kiểm soát chất lượng (Quality Control - QC) chủ động. Điều này bao gồm việc duy trì áp suất khí dương trong hệ thống HVAC (Heating, Ventilation, and Air Conditioning) và sử dụng kết hợp bộ lọc HEPA (lọc hạt) và than hoạt tính (lọc VOCs)[2]. Đồng thời, việc kiểm soát nguồn gốc EDCs là tối quan trọng: chỉ sử dụng vật tư được đánh giá cấp độ dùng trong y tế (Medical-grade plasticware) và tuân thủ các quy định nghiêm ngặt về vệ sinh cá nhân, cấm tuyệt đối mỹ phẩm, nước hoa chứa EDCs trong khu vực lab. Thiết lập hệ thống giám sát VOCs liên tục theo thời gian thực giúp phát hiện các đỉnh ô nhiễm để điều chỉnh quy trình làm việc kịp thời[1].
5. Kết luận
Hormone steroid đóng vai trò nền tảng trong việc điều hòa sinh lý, tạo ra noãn có tiềm năng phát triển thành phôi chất lượng cao. Vai trò của CVPH, mặc dù gián tiếp, nhưng lại là trọng tâm trong việc thiết lập một môi trường in vitro ổn định, có khả năng bù đắp và bảo vệ phôi khỏi những biến động nội tiết in vivo và EDCs/VOCs in vitro.
Để tối ưu hóa hiệu suất lab, cần tập trung vào ba chiến lược then chốt: Thứ nhất, phải có sự phối hợp lâm sàng - phôi học chặt chẽ, đặc biệt trong việc xử lý các trường hợp PPE, nơi chiến lược trữ phôi toàn bộ là cần thiết để tránh tình trạng bất đồng bộ phôi với NMTC. Thứ hai, phải thực hiện kiểm soát chủ động EDCs/VOCs - đây là biện pháp mạnh mẽ nhất để bảo vệ phôi khỏi các chất gây ô nhiễm giống với hormone sinh dục, từ đó duy trì động học phát triển tối ưu[9] [11]. Việc này đòi hỏi duy trì hệ thống HVAC chuyên dụng và sử dụng vật tư không phát thải. Cuối cùng, đánh giá noãn toàn diện thông qua hình thái COC như một chỉ số không xâm lấn để liên kết với tình trạng nội tiết của bệnh nhân là cần thiết để đưa ra quyết định nuôi cấy và chọn lọc phôi có tiềm năng làm tổ tốt nhất[12].
Từ khoá: hormone steroid, môi trường nuôi cấy, HVAC, hoá chất gây rối loạn nội tiết, chọn lọc phôi
Tài liệu tham khảo:
[1] PhytoTechnology Laboratories, Inc. (2003). Components of Tissue Culture Media (Product Information Sheet). Retrieved from https://phytotechlab.com/media/documents/TechnicalLiterature/ComponentsOfTissueCultureMedia.pdf
[2] Olofsson et al (2013). Quality management systems for your in vitro fertilization clinic's laboratory: Why bother?. Journal of Human Reproductive Sciences, 6(1), 3-8.
[3] He, M., Zhang et al (2021). Mechanisms of oocyte maturation and related epigenetic regulation. Frontiers in cell and developmental biology, 9, 654028.
[4] Kotarska et al (2015). Increased progesterone production in cumulus–oocyte complexes of female mice sired by males with the Y-chromosome long arm deletion and its potential influence on fertilization efficiency. Reproductive Sciences, 22(2), 242-249.
[5] Gleicher et al (2011). The role of androgens in follicle maturation and ovulation induction: friend or foe of infertility treatment?. Reproductive Biology and Endocrinology, 9(1), 116.
[6] Kamijo et al (1994). In vitro fertilization of androgen sterilized mice. Life sciences, 55(7), 527-531.
[7] Cleveland Clinic. (2023). Ovarian hyperstimulation syndrome (OHSS). Retrieved from https://my.clevelandclinic.org/health/diseases/17972-ovarian-hyperstimulation-syndrome-ohss
[8] Carter et al (2010). Effect of elevated circulating progesterone concentration on bovine blastocyst development and global transcriptome following endoscopic transfer of in vitro produced embryos to the bovine oviduct. Biology of reproduction, 83(5), 707-719.
[9] Cai et al (2025). Real-time monitoring reveals the effects of low concentrations of volatile organic compounds in the embryology laboratory. Human Reproduction, 40(4), 601-611.
[10] Darbre, P. D. (2018). Overview of air pollution and endocrine disorders. International journal of general medicine, 191-207.
[11] Shahine, L. (2024). How air quality affects your fertility and what you can do about it. Dr. Lora Shahine. https://drlorashahine.com/blog/how-air-quality-affects-your-fertility-and-what-you-can-do-about-it
[12] Massoud et al (2024). Biomarkers assessing the role of cumulus cells on IVF outcomes: a systematic review. Journal of assisted reproduction and genetics, 41(2), 253-275.
[13] Eftekhar et al (2013). Effect of progesterone supplementation on natural frozen-thawed embryo transfer cycles: a randomized controlled trial. International Journal of Fertility & Sterility, 7(1), 13.