CNSH. Trần Hồ Khánh Duyên
CNSH. Nguyễn Quỳnh Như
Bệnh viện Đại Học Y Dược Buôn Ma Thuột
GIỚI THIỆU
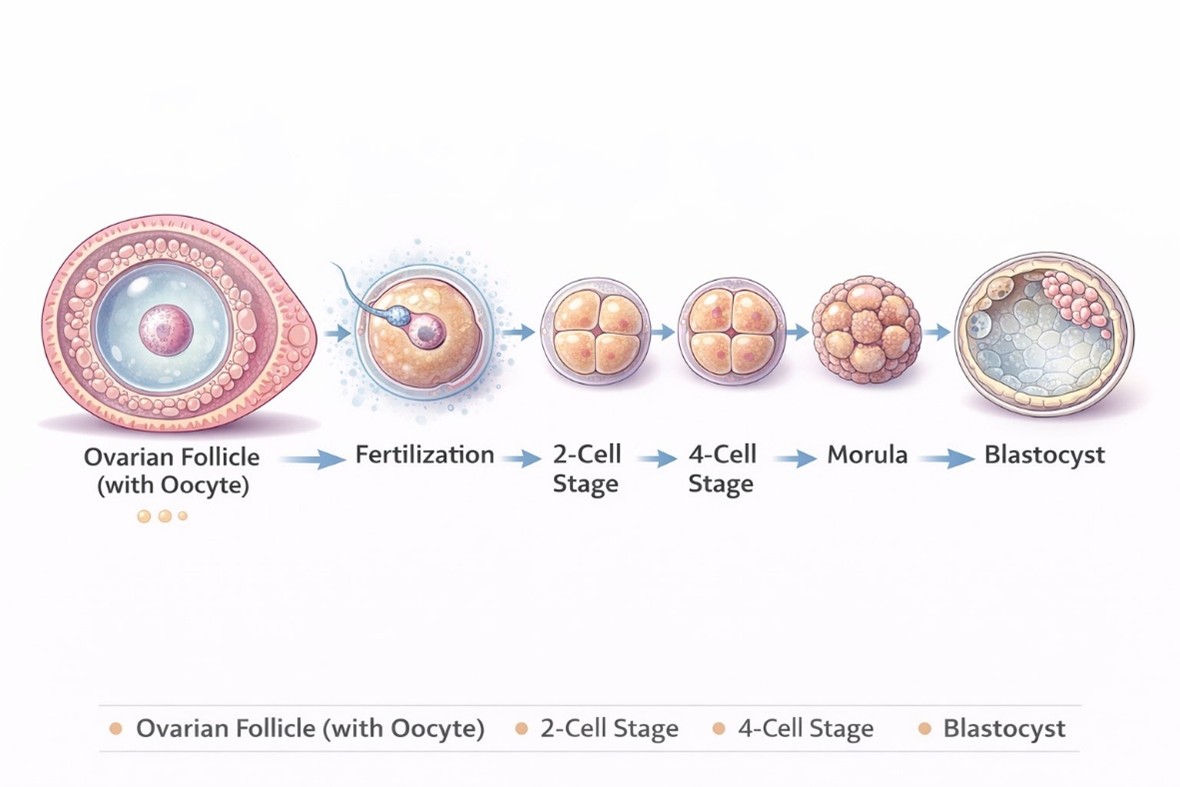
Thụ tinh trong ống nghiệm (In Vitro Fertilization - IVF) và tiêm tinh trùng vào bào tương noãn (Intracytoplasmic Sperm Injection - ICSI) đã trở thành những kỹ thuật cốt lõi trong hỗ trợ sinh sản hiện đại, mang lại cơ hội làm cha mẹ cho hàng triệu cặp vợ chồng vô sinh, hiếm muộn trên toàn thế giới. IVF cho phép kết hợp noãn và tinh trùng ngoài cơ thể, trong khi ICSI mở rộng khả năng điều trị cho các trường hợp tinh trùng chất lượng kém hoặc thất bại thụ tinh trước đó. Tuy nhiên, thành công của một chu kỳ IVF vẫn phụ thuộc vào nhiều yếu tố, trong đó, việc lựa chọn phôi tối ưu để chuyển đóng một vai trò quyết định. Trong nhiều năm, đánh giá hình thái phôi vẫn là tiêu chuẩn vàng trong lâm sàng, dù vẫn tồn tại những hạn chế nhất định về độ chính xác. Do đó, nhu cầu tìm kiếm các dấu chỉ sinh học bổ sung, khách quan hơn để nâng cao khả năng tiên lượng kết quả là một hướng nghiên cứu cấp thiết. Dịch nang noãn (Follicular fluid – FF), được hình thành từ dịch thấm huyết tương và dịch tiết của tế bào hạt, đóng vai trò quan trọng trong việc nuôi dưỡng và trưởng thành noãn. Thành phần của FF phản ánh năng lực phát triển của noãn cũng như khả năng sống của phôi. Các nghiên cứu bước đầu cho thấy, nồng độ hormone steroid trong dịch nang noãn có thể phản ánh tình trạng chức năng của noãn bào, từ đó tiết lộ tiềm năng phát triển của phôi.
Hormone steroid là nhóm hormone có cấu trúc nền từ cholesterol, giữ vai trò thiết yếu trong điều hòa sinh lý sinh sản nữ giới. Chúng tham gia kiểm soát quá trình phát triển nang noãn, trưởng thành noãn, rụng trứng và chuẩn bị nội mạc tử cung cho sự làm tổ. Trong buồng trứng, các hormone steroid như estrogen, progesterone và androgen không chỉ điều hòa cục bộ sự phát triển của noãn mà còn phản ánh tình trạng hoạt động nội tiết của nang noãn. Do đó, việc nghiên cứu nồng độ hormone steroid trong dịch nang noãn đang được quan tâm như một dấu ấn sinh học tiềm năng để đánh giá chất lượng noãn và tiên lượng kết quả thụ tinh trong ống nghiệm [1]. Bài viết này sẽ thảo luận về tiềm năng của các hormone steroid như estradiol, progesterone và một số chất chuyển hóa khác trong dịch nang noãn với tư cách là một dấu ấn sinh học đầy hứa hẹn, hỗ trợ đắc lực cho việc tiên lượng kết quả IVF và bổ trợ cho quy trình lựa chọn phôi dựa trên hình thái truyền thống [2], [3].
NỒNG ĐỘ HORMONE STEROID TRONG DỊCH NANG NOÃN VÀ TIỀM NĂNG TIÊN LƯỢNG KẾT QUẢ THỤ TINH TRONG ỐNG NGHIỆM
Progesterone trong dịch nang và năng lực noãn bào
Progesterone đóng vai trò thiết yếu trong nhiều giai đoạn sinh sản, bao gồm việc tiếp tục sự giảm phân của noãn, thụ tinh, phát triển phôi, làm tổ và duy trì thai kỳ [4],[5]. Trong quá trình trưởng thành của noãn, progesterone (P4) được tổng hợp trong các tế bào hạt. Sự tổng hợp này xảy ra do sự kích thích của hormone kích thích nang noãn (FSH). Hơn nữa, quá trình sản xuất P4 tiếp tục tăng lên trong các nang noãn tiền rụng trứng do sự biệt hóa của các thụ thể Hormone Luteinizing (LH), tương ứng với sự gia tăng LH đột ngột. Các nghiên cứu đã chứng minh rằng việc phân tích nồng độ P4 trong dịch nang, có thể cung cấp các dấu ấn sinh học tiềm năng cho khả năng phát triển của noãn. Mục tiêu chính của một số nghiên cứu là điều tra tính hữu ích của P4 trong dịch nang như một dấu ấn sinh học để dự đoán sự phát triển thành công của noãn đã thụ tinh đến giai đoạn phôi nang.
Nghiên cứu của O'Brien và cộng sự, 2019 khi phân tích nồng độ hormone Anti-Müllerian hormone (AMH) và P4 trong dịch nang noãn (Follicular fluid - FF) và sự tương quan với năng lực noãn bào, cho thấy mức FF-P4 cao hơn đáng kể (p = 0,013) ở nhóm noãn phát triển thành phôi nang (59,76 ± 54,38 mg/ml) so với nhóm noãn chỉ thụ tinh nhưng không phát triển được đến giai đoạn phôi nang (29,25 ± 22,4 mg/ml). Nồng độ FF-P4 cao tương quan với sự phát triển thành phôi nang. Cụ thể, trong số các mẫu dịch nang được kiểm tra, 11 mẫu có nồng độ P4 > 60 mg/ml, trong đó 10 mẫu liên quan đến noãn phát triển đến giai đoạn phôi nang. Mức P4 này cung cấp giá trị dự đoán dương tính là 90,99% cho khả năng phát triển thành phôi nang. Khi kết hợp cả hai dấu ấn sinh học, 6 mẫu có mức P4 > 60 mg/ml và AMH > 15 pmol/L, trong đó 100% các noãn tương ứng đã phát triển thành phôi nang, với giá trị dự đoán dương tính là 96,83%. Điều này cho thấy nồng độ P4 cao trong dịch nang có thể được sử dụng như một xét nghiệm dự đoán chính xác, không xâm lấn và tiết kiệm chi phí về tiềm năng phát triển của noãn trong môi trường lâm sàng. Ngược lại, giảm tiết FF-P4 trong quá trình trưởng thành của noãn có thể gây ra tác động bất lợi đến chất lượng noãn, được định nghĩa bằng sự phát triển phôi, đặc biệt ở giai đoạn phôi nang [4]. Nồng độ P4 trong dịch nang tiền rụng trứng cũng được ghi nhận có sự tương quan với sự thụ tinh thành công và sự phân chia của phôi [6].
Các nghiên cứu trước đây đã chỉ ra rằng nồng độ P4 cao trong FF là yếu tố dự đoán khả năng làm tổ [7, 8, 9]. Tóm lại, P4 trong dịch nang đóng vai trò là một dấu ấn sinh học không xâm lấn và chính xác để đánh giá tiềm năng phát triển của noãn, đặc biệt là khả năng phát triển thành phôi nang, và liên quan tích cực đến các kết quả thai lâm sàng [4].
Estradiol trong dịch nang tương quan với chất lượng noãn và kết quả lâm sàng
Estradiol (E2) là một trong những hormone estrogen hoạt động mạnh. Trong cơ thể phụ nữ tiền mãn kinh, buồng trứng là nơi tổng hợp estrogen chủ yếu. E2 được tổng hợp tại buồng trứng thông qua một quá trình phức tạp. Hormone kích thích nang trứng (FSH) điều chỉnh sự tổng hợp estrogen thông qua enzyme aromatase nằm trong các tế bào hạt của buồng trứng. Aromatase có vai trò thiết yếu trong quá trình sinh tổng hợp estrogen, chuyển đổi Testosterone thành E2 và Androstenedione thành Estrone (E1). Sau đó, enzyme 17β-Hydroxysteroid dehydrogenase (HSD17β) tiếp tục chuyển E1 thành E2, hoàn tất quá trình tổng hợp estrogen trong nang noãn. E2 đóng vai trò quan trọng trong sự phát triển nang noãn, thúc đẩy sự tăng sinh các tế bào hạt của các nang nhỏ. E2 còn làm tăng cường độ nhạy của các tế bào hạt với FSH, có tác dụng bảo tồn trong các nang sớm bằng cách ức chế quá trình chết tế bào theo chương trình [1].
Estradiol trong dịch nang (FF-E2) được xem là một dấu ấn sinh học tiềm năng cho chất lượng noãn bào và kết quả điều trị hỗ trợ sinh sản. Thông thường, nồng độ E2 trong FF luôn ở mức cao. Nghiên cứu của Yan và cộng sự, 2020 nhằm đánh giá FF-E2 như một yếu tố dự đoán kết quả thụ tinh trong ống nghiệm và chuyển phôi tươi. Cho thấy nồng độ E2 trong dịch nang ở nhóm bệnh nhân có thai lâm sàng là 526,419 ± 289,944 pg/ml, thấp hơn đáng kể so với nhóm không có thai là 736,085 ± 261,885 pg/ml. Kết quả này cho thấy nồng độ E2 cao trong dịch nang có tác động tiêu cực đến kết quả mang thai. Nồng độ E2 cao bất thường này có thể ảnh hưởng đến tiềm năng phát triển của các noãn bào lân cận thông qua các con đường tín hiệu tự tiết và cận tiết. Nghiên cứu này cho thấy FF-E2 được xem là yếu tố dự đoán tốt hơn cho kết quả thụ tinh trong ống nghiệm và chuyển phôi so với nồng độ AMH trong cùng môi trường. Tuy nhiên, trong mô hình đường cong ROC, mức E2 có giá trị dự đoán thấp cho kết quả mang thai (AUC < 0,5)[10].
Một số nghiên cứu chỉ ra rằng estradiol và progesterone trong dịch nang là những dấu ấn sinh học cho chất lượng noãn bào tiền rụng trứng [4]. Tuy nhiên, khi chia các trường hợp thành nhóm E2 thấp và E2 cao dựa trên mức trung vị FF-E2 (676,610 pg/ml), nghiên cứu của Yan Lv và cộng sự, 2020 cho thấy không có sự khác biệt đáng kể về số lượng noãn thu được, tỉ lệ thụ tinh (81,99% so với 80,74%, p=0,691), và tỉ lệ phôi chất lượng tốt (70,89% so với 65,78%, p=0,238) giữa hai nhóm. Sự tương quan giữa nồng độ E2 trong dịch nang với tỉ lệ thụ tinh và số lượng phôi nang hữu dụng cũng không có ý nghĩa thống kê [10]. Điều này được giải thích rằng FF-E2 cao có liên quan đến tổn thương ty thể của noãn, thể hiện qua giảm điện thế màng ty thể và tăng stress oxy hóa, từ đó làm suy giảm chức năng và chất lượng noãn [10]. Những rối loạn ở mức ty thể và biểu sinh này có thể không biểu hiện trên hình thái phôi sớm, nhưng lại làm giảm khả năng làm tổ và phát triển phôi sau đó, do sự sai lệch trong biểu hiện của các gen điều hòa phát triển sớm của phôi [11].
Tóm lại, trong khi E2 đóng vai trò quan trọng trong vi môi trường nang noãn, các nghiên cứu gần đây cho thấy nồng độ E2 trong dịch nang của nang lớn nhất có tương quan nghịch với kết quả mang thai lâm sàng nhưng không có mối liên hệ rõ ràng với tỉ lệ thụ tinh hay tỉ lệ phôi chất lượng tốt.
Cortisone trong dịch nang và vai trò của Glucocorticoid đối với tiềm năng phôi
Cortisone là một steroid nội nang thuộc nhóm Glucocorticoid. Về mặt sinh học, Cortisone được coi là dạng không hoạt động vì nó có ái lực thấp với thụ thể Glucocorticoid. Trong môi trường dịch nang, Cortisone tồn tại trong một hệ thống cân bằng phức tạp với Cortisol, dạng hoạt động của Glucocorticoid. Sự chuyển đổi qua lại giữa Cortisol (hoạt động) và Cortisone (không hoạt động) được xúc tác bởi enzyme 11β-Hydroxysteroid Dehydrogenase (11β-HSD). HSD11β1 chủ yếu chuyển đổi Cortisone thành Cortisol. Sau khi tiêm hCG, biểu hiện của enzyme HSD11β1 tăng lên, làm tăng sản xuất Cortisol. HSD11β2 thực hiện quá trình ngược lại, chuyển đổi Cortisol thành Cortisone. Hoạt động của HSD11β2 giảm sau khi tiêm hCG. Các enzyme này được tìm thấy trong tất cả các khoang của nang noãn, bao gồm noãn bào, tế bào cumulus, tế bào hạt và tế bào vỏ.
Chức năng sinh học chủ yếu của hệ thống này là thông qua thụ thể Glucocorticoid có mặt trong noãn bào và các tế bào soma xung quanh, thực hiện chuyển vị trí từ bào tương vào nhân sau khi gắn kết với Cortisol. Sự truyền tín hiệu qua thụ thể Glucocorticoid trong noãn bào được cho là gián tiếp điều chỉnh chức năng của tế bào cumulus, bao gồm sự nở rộng của tế bào cumulus, một quá trình quan trọng cho sự trưởng thành của noãn [5], [12].
Nồng độ Cortisone trong dịch nang được nghiên cứu như một dấu ấn sinh học tiềm năng dự đoán chất lượng phôi nang. Mức cortisone trong FF thấp hơn đã được quan sát thấy trong các nang noãn chứa noãn bào phát triển thành phôi nang chất lượng cao (12,20 ± 0,82 ng/ml) so với nhóm không thụ tinh (15,37 ± 0,87 ng/ml) [5].
Các nghiên cứu lâm sàng còn chỉ ra rằng tỷ lệ Cortisol/Cortisone cao hơn trong dịch nang và huyết thanh có thể là yếu tố quan trọng đối với sự trưởng thành của noãn bào và sự làm tổ của phôi. Sự giảm Cortisone và tăng Cortisol sau kích thích rụng trứng tạo ra tỷ lệ Cortisol/Cortisone cao hơn, điều này cho thấy một môi trường nang noãn tối ưu cho sự phát triển phôi. Các nghiên cứu trên người cho thấy nồng độ Cortisone trong FF thấp hơn đáng kể trong các mẫu thu được từ bệnh nhân có thai lâm sàng so với chu kỳ không có thai [5], [12].
Tóm lại, nồng độ Cortisone thấp trong dịch nang (và do đó, tỷ lệ Cortisol/Cortisone cao) là một yếu tố dự đoán tích cực, cho thấy hệ thống enzyme trong nang noãn đang chuyển hóa Cortisone (không hoạt động) thành Cortisol (hoạt động) một cách hiệu quả, tạo ra vi môi trường thuận lợi cho tiềm năng phát triển của phôi.
Testosterone trong dịch nang và tiềm năng phát triển phôi
Testosterone là một androgen quan trọng, chủ yếu được tổng hợp trong các tế bào vỏ của buồng trứng. Testosterone có vai trò trong việc điều chỉnh sự tăng sinh và ngăn chặn quá trình chết tế bào theo chương trình trong các tế bào hạt, qua đó tác động đến sự phát triển nang noãn. Trong con đường chuyển hóa steroid nội nang, Testosterone là dạng hoạt động có thể được chuyển hóa thành Dihydrotestosterone (DHT), một androgen mạnh hơn [1].
Nồng độ Testosterone trong dịch nang (FF-T) đã được nghiên cứu như một dấu ấn sinh học phản ánh chất lượng noãn bào và tiềm năng phát triển phôi. Nồng độ Testosterone được ghi nhận là thấp hơn trong các noãn bào phát triển tốt. Cụ thể, nồng độ FF-T thấp hơn đáng kể ở nhóm noãn phát triển thành phôi nang chất lượng cao (0,49 ± 0,21 ng/ml) so với nhóm noãn không thụ tinh (1,69 ± 0,52 ng/ml). Tương tự, nồng độ FF-T trong toàn bộ nhóm noãn thụ tinh cũng thấp hơn nhóm noãn không thụ tinh. Kết quả này cho thấy mức FF-T cao có thể liên quan đến thất bại trong quá trình thụ tinh. Tuy nhiên, khi so sánh trực tiếp nồng độ FF-T giữa nhóm noãn đã thụ tinh nhưng không phát triển đến giai đoạn phôi nang và nhóm tạo ra phôi nang chất lượng cao, không có sự khác biệt có ý nghĩa thống kê về nồng độ Testosterone được tìm thấy [5].
Tóm lại, nồng độ Testosterone thấp trong dịch nang có vẻ là điều kiện thuận lợi, có khả năng dự đoán thành công quá trình thụ tinh và sự phát triển thành phôi nang chất lượng cao khi so sánh với thất bại thụ tinh. Mức Testosterone cao hơn có thể báo hiệu một môi trường nang không tối ưu dẫn đến thất bại thụ tinh.
KẾT LUẬN:
Các nghiên cứu gần đây cho thấy một số hormone steroid trong dịch nang noãn, đặc biệt là cortisone, estradiol, progesterone và testosterone có liên quan đến tiềm năng phát triển của phôi và kết quả IVF. Nồng độ cortisone cao trong dịch nang là yếu tố dự báo tiêu cực cho khả năng mang thai lâm sàng, trong khi progesterone cao hơn liên quan đến phôi phát triển tốt hơn. Tuy nhiên, vai trò dự báo của các hormone steroid khác như estradiol và testosterone còn chưa nhất quán và cần thêm nghiên cứu xác nhận.
Tài liệu tham khảo
-
Beevors LI, Sundar S, Foster PA. Steroid metabolism and hormonal dynamics in normal and malignant ovaries. Essays Biochem. 2024 Dec 4;68(4):491-507. doi: 10.1042/EBC20240028. PMID: 38994724; PMCID: PMC11625866.
-
Influence of follicular fluid and cumulus cells on oocyte quality: clinical implications. M. G. Da Broi, el al Journal of Assisted Reproduction Genetics volume 35, pages735–751 (2018)
-
Zhang, Y., He, C., He, Y. et al. Follicular Fluid Metabolomics: Tool for Predicting IVF Outcomes of Different Infertility Causes. Reprod. Sci. 32, 921–934 (2025). https://doi.org/10.1007/s43032-024-01664-y
-
O'Brien Y, Wingfield M, O'Shea LC. Anti-Müllerian hormone and progesterone levels in human follicular fluid are predictors of embryonic development. Reprod Biol Endocrinol. 2019 Jun 19; 17(1):47. doi: 10.1186/s12958-019-0492-9. PMID: 31217014; PMCID: PMC6585091.
-
Yu L, Liu M, Xu S, Wang Z, Liu T, Zhou J, Zhang D, Dong X, Pan B, Wang B, Liu S, Guo W. Follicular fluid steroid and gonadotropic hormone levels and mitochondrial function from exosomes predict embryonic development. Front Endocrinol (Lausanne). 2022 Nov 9;13:1025523. doi: 10.3389/fendo.2022.1025523. PMID: 36440207; PMCID: PMC9682035.
-
Kobayashi T, Oda T, Yoshimura Y, Takehara Y, Natori M, Nozawa S. Androstenedione and progesterone concentrations in preovulatory follicular fluid correlate with successful fertilization and cleavage of human oocytes in vitro. Fertil Steril. 1991;56(2):301–5.
-
Basuray R, Rawlins RG, Radwanska E, Henig I, Sachdeva S, Tummon I, et al. High progesterone/estradiol ratio in follicular fluid at oocyte aspiration for in vitro fertilization as a predictor of possible pregnancy. Fertil Steril. 1988;49(6):1007–11.Vanluchene E, Hinting A, Dhont M, De Sutter P, Van Maele G, Vandekerckhove D. Follicular fluid steroid levels in relation to oocyte maturity and in vitro fertilization. J Steroid Biochem Mol Biol. 1991;38(1):83–7.
-
Enien WM, el Sahwy S, Harris CP, Seif MW, Elstein M. Human chorionic gonadotrophin and steroid concentrations in follicular fluid: the relationship to oocyte maturity and fertilization rates in stimulated and natural in-vitro fertilization cycles. Hum Reprod. 1995;10(11):2840–4.
-
Lv, Y., Du, S., Huang, X., & Hao, C. (2020). Follicular fluid estradiol is an improved predictor of in vitro fertilization/intracytoplasmic sperm injection and embryo transfer outcomes. Experimental and Therapeutic Medicine, 20. https://doi.org/10.3892/etm.2020.9256.
-
Voros, C.; Varthaliti, A.; Mavrogianni, D.; Athanasiou, D.; Athanasiou, A.; Athanasiou, A.; Papahliou, A.-M.; Zografos, C.G.; Topalis, V.; Kondili, P.; et al. Epigenetic Alterations in Ovarian Function and Their Impact on Assisted Reproductive Technologies: A Systematic Review. Biomedicines 2025, 13, 730. https://doi.org/10.3390/biomedicines13030730.
-
Ravisankar S, Hanna CB, Brooks KE, Murphy MJ, Redmayne N, Ryu J, Kinchen JM, Chavez SL, Hennebold JD. Metabolomics analysis of follicular fluid coupled with oocyte aspiration reveals importance of glucocorticoids in primate periovulatory follicle competency. Sci Rep. 2021 Mar 22;11(1):6506. doi: 10.1038/s41598-021-85704-6. Erratum in: Sci Rep. 2021 Aug 16;11(1):16968. doi: 10.1038/s41598-021-96473-7. PMID: 33753762; PMCID: