ThS. Hồ Lan Trâm – Bệnh viện Mỹ Đức
- Đặt vấn đề
Tiêm tinh trùng vào bào tương noãn (Intracytoplasmic sperm injection – ICSI) hiện nay đã trở thành kỹ thuật hỗ trợ sinh sản phổ biến nhất, được áp dụng cho nhiều chỉ định vô sinh khác nhau. Mặc dù tỷ lệ thụ tinh bình thường ước tính đạt khoảng 70%, hiện tượng thất bại thụ tinh hoàn toàn (Total fertilization failure – TFF) vẫn xảy ra ở khoảng 3–5% tổng số chu kỳ ICSI [1]. Trong đó, sự thất bại trong quá trình hoạt hóa noãn (Oocyte activation deficiency - OAD) được xem là nguyên nhân chính, có thể liên quan đến yếu tố từ tinh trùng hoặc từ noãn [2]. Hoạt hóa noãn được khởi phát bởi các dao động Ca2+ nội bào, trong đó phospholipase C zeta (PLCζ) có nguồn gốc từ tinh trùng đóng vai trò then chốt. Sự thiếu hụt hoặc rối loạn chức năng PLCζ dẫn đến thất bại trong việc tạo ra tín hiệu Ca2+ thích hợp, gây OAD và TFF sau ICSI. Trên cơ sở đó, kỹ thuật hỗ trợ hoạt hóa noãn nhân tạo (Assisted oocyte activation – AOA) đã được phát triển nhằm tạo ra sự gia tăng Ca2+ nội bào, thông qua các phương pháp cơ học, điện hoặc hóa học. Trong bài viết này, chúng tôi tổng quan cơ sở sinh học của quá trình hoạt hóa noãn, các phương pháp hỗ trợ hoạt hóa noãn nhân tạo hiện nay và những chỉ định lâm sàng đang được áp dụng, nhằm làm rõ vai trò thực tế của AOA trong điều trị thất bại thụ tinh sau ICSI.
- Cơ sở sinh học của các phương pháp hỗ trợ hoạt hoá noãn nhân tạo
Trong quá trình thụ tinh ở động vật hữu nhũ, sau khi tinh trùng và noãn dung hợp noãn bào, noãn bào biểu hiện những đợt tăng lặp đi lặp lại của nồng độ ion canxi nội bào, hay được gọi là dao động Ca2+ (Ca2+ oscillations).
Tinh trùng thụ tinh khởi phát tín hiệu Ca2+ thông qua việc đưa PLCζ đến màng noãn trong hoặc ngay sau khi xảy ra sự dung hợp màng giữa tinh trùng và noãn. PLCζ tương tác với một hoặc nhiều yếu tố có nguồn gốc từ noãn hiện vẫn chưa được xác định, từ đó thúc đẩy quá trình thủy phân Phosphatidylinositol 4,5-bisphosphate (PIP[TL2] ₂) thành Diacylglycerol (DAG) và Inositol 1,4,5-trisphosphate (InsP₃). InsP₃ sau đó kích hoạt sự phóng thích Ca2+ từ các kho dự trữ nội bào [3] (Hình 1).
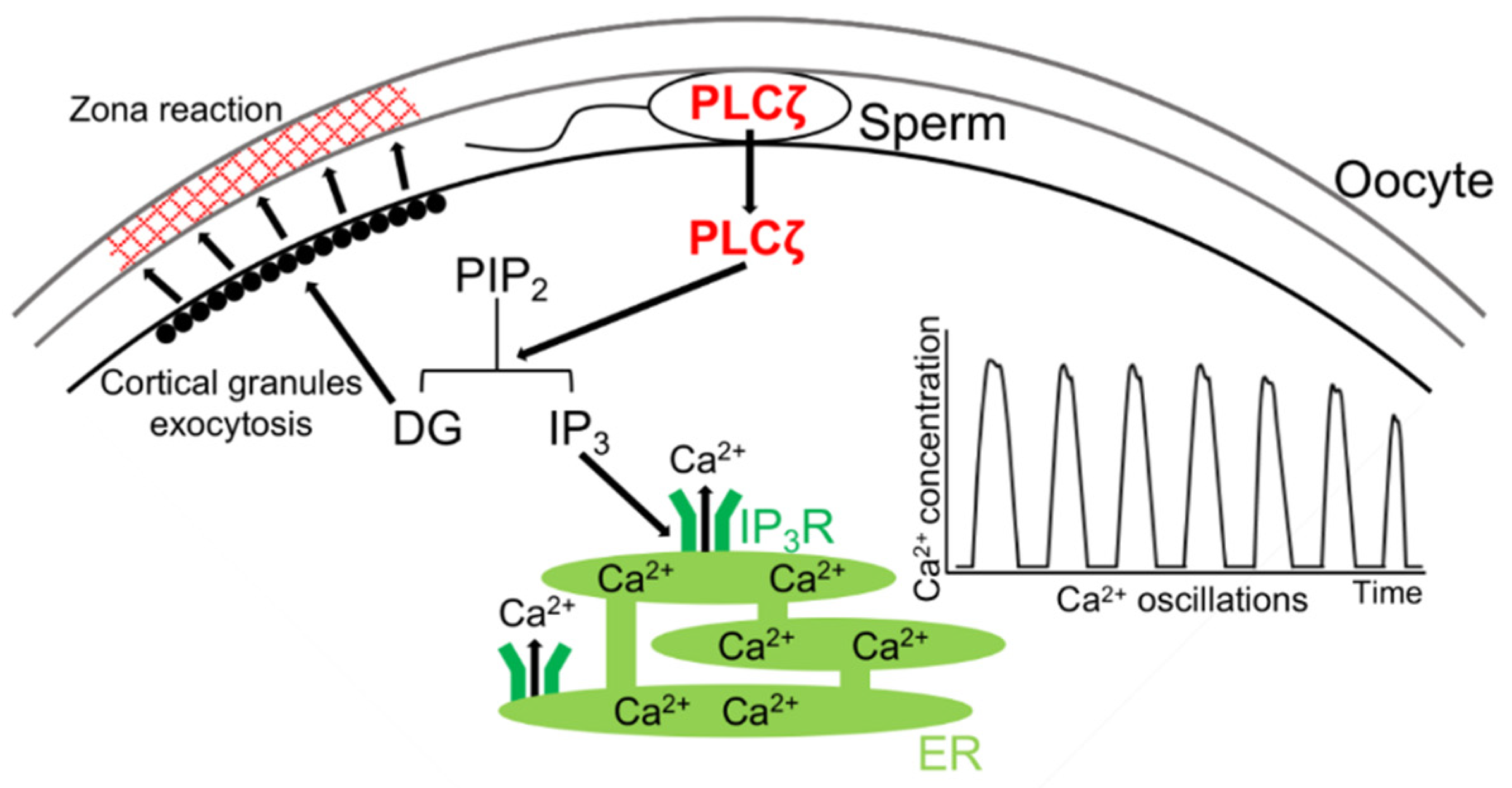 |
Hình 1: Cơ chế hoạt động của PLCζ ở tinh trùng [3]
Làn sóng này khởi phát từ vị trí hợp nhất giữa tinh trùng và noãn, sau đó di chuyển sang phía đối diện của noãn. Kiểu dao động này có sự khác biệt giữa các loài về thời gian kéo dài, biên độ và tần suất [4]. Ở chuột, thời gian để làn sóng Ca2+ ban đầu lan truyền trong các noãn này vào khoảng 5–10 giây. Ở các pha tăng Ca2+ tiếp theo, các làn sóng trở nên ngày càng nhanh hơn; sau khoảng 15 phút, làn sóng Ca2+ có thể lan truyền xuyên qua noãn chỉ trong khoảng ~1 giây [5]. Nồng độ Ca2+ điển hình vào khoảng 100 nM, đạt đỉnh gần 1000 nM, với mỗi đợt tăng kéo dài khoảng 0,5 phút [5]. Các dao động Ca2+ này duy trì trong khoảng 4–5 giờ và chấm dứt vào thời điểm hình thành tiền nhân [7], [8].
Dao động Ca2+ đóng vai trò then chốt trong việc hoạt hóa noãn và phát triển phôi, tái khởi động giảm phân II ở noãn. Cơ chế được đề xuất này dẫn đến sự xuất bào của các hạt vỏ (cortical granules), bất hoạt [TL3] Mitogen-activated protein kinase (MAPK) và tiếp theo là sự hình thành tiền nhân, đồng thời hoạt hóa Protein kinase II phụ thuộc Ca²⁺/calmodulin (Ca2+/calmodulin-dependent protein kinase II- (CaMKII)[TL4] . CaMKII ức chế yếu tố duy trì trạng thái tĩnh bào (CSF; Emi2[TL5] ) và giải phóng phức hợp xúc tiến kỳ sau (Anaphase-promoting complex-APC[TL6] ). Quá trình này làm giảm nồng độ Cyclin B1 trong phức hợp yếu tố thúc đẩy trưởng thành (Maturation-promoting factor – MPF), bao gồm Cyclin-dependent kinase 1 (CDK1) [TL7] và Cyclin B1, dẫn đến bất hoạt yếu tố thúc đẩy trưởng thành (Maturation-promoting factor – MPF) và giải phóng noãn khỏi trạng thái ngừng giảm phân II. Cả tinh trùng và noãn đều đóng vai trò quan trọng trong quá trình hoạt hoá noãn, bao gồm tinh trùng cung cấp yếu tố PLCζ có chức năng, trong khi noãn trưởng thành phải có khả năng tiếp nhận PLCζ và tạo ra kiểu dao động Ca2+ phù hợp.
- Các phương pháp hỗ trợ hoạt hoá noãn nhân tạo
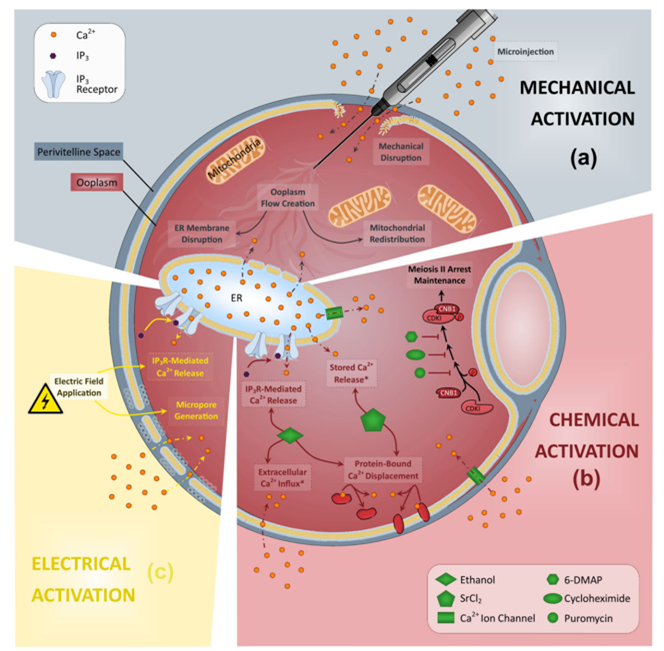
Việc sử dụng ICSI kết hợp với AOA đã ngày càng phổ biến trong hơn hai thập kỷ qua. AOA nhằm mục tiêu tạo ra sự phóng thích Ca2+ nội bào đầy đủ, từ đó cho phép noãn được hoạt hóa và thụ tinh thành công. Nhiều phương pháp AOA đã được sử dụng, bao gồm: phương pháp cơ học, bổ sung Ca2+ ngoại sinh và kích thích xung điện.
Phương pháp cơ học
Hỗ trợ hoạt hoá noãn nhân tạo bằng cơ học được thực hiện bằng việc hút mạnh tế bào chất của noãn từ 2-3 lần bằng kim ICSI, với lượng bào tương noãn khoảng 0,1 pL/lần. Cơ sở sinh học của phương pháp này là thao tác hút cơ học có thể mô phỏng sự dịch chuyển bào quan từ trung tâm noãn ra ngoại vi, tạo ra dòng Ca2+ và giải phóng Ca2+ dự trữ trong bào quan. Một giả thuyết khác cho rằng việc hút tế bào chất giúp ty thể có tính phân cực cao di chuyển về trung tâm noãn, cung cấp thêm năng lượng cho quá trình hoạt hóa sau tiêm tinh trùng [6].
Phương pháp này được nhiều nghiên cứu sau đó ghi nhận kết quả không đồng nhất, với tỷ lệ thụ tinh thấp và tỷ lệ thai lâm sàng kém khi không kết hợp thêm phương pháp AOA khác. Nguyên nhân là do dao động Ca2+ thu được nhỏ và không hình thành được các đỉnh Ca2+ dao động đặc trưng như trong quá trình thụ tinh tự nhiên [7].
Phương pháp kích thích xung điện
Hoạt hóa bằng kích thích xung điện thường liên quan đến việc tác động trực tiếp một dòng điện, gây ra sự di chuyển của các protein mang điện trong lớp đôi lipid và hình thành các lỗ trên màng, từ đó cho phép Ca2+ ngoại bào đi vào màng. Tuy nhiên, các công nghệ này cho đến nay vẫn chưa được sử dụng rộng rãi trên người. Hiệu quả tổng thể của kích thích xung điện phụ thuộc vào nhiều yếu tố, bao gồm kích thước lỗ màng được hình thành và thành phần ion của môi trường xung quanh.
Phương pháp này đã được áp dụng thành công trên noãn bò và noãn người [8]. Theo quy trình được thực hiện bởi tác giả Tanaka, noãn được đặt trong dung dịch Mannitol 295 mM có bổ sung 0,1 mM CaCl₂ và 0,05 mM MgCl₂, được kích thích bằng dòng điện xoay chiều 5 V/cm ở tần số 1 MHz trong 10 giây, tiếp theo là một xung điện một chiều 1,2 kV/cm kéo dài 99 ms bằng máy phát xung điện hợp bào [9]. Ông đã sử dụng kỹ thuật này khi thực hiện tiêm tinh tử tròn vào bào tương noãn, với luận điểm rằng xung điện mang lại dao động Ca2+ tương tự như sinh lý tự nhiên [10]. Tuy nhiên, quan điểm khác cho rằng quy trình kích thích xung điện có thể gây hình thành các gốc oxy hóa phản ứng (reactive oxygen species – ROS) trong noãn [10]. Ngoài ra, sự gia tăng Ca2+ chỉ mang tính thoáng qua, với nồng độ Ca2+ nhanh chóng trở về mức nền mà không tạo ra các dao động Ca2+ đặc trưng [11].
Phương pháp bổ sung Ca2+ ngoại sinh
Các phác đồ AOA hóa học sử dụng những hợp chất có khả năng tạo ra các đợt tăng Ca2+ nội bào tại màng noãn, chủ yếu thông qua dòng Ca2+ đi vào từ ngoại bào. Các tác nhân này thường là những hợp chất tan trong lipid, có khả năng vận chuyển Ca2+ qua màng tế bào bằng cách làm tăng tính thấm Ca2+ và thúc đẩy dòng Ca2+ ngoại bào vào trong noãn. Ngoài ra, một số hợp chất, chẳng hạn như InsP₃ còn tác động trực tiếp lên các kho dự trữ Ca2+ nội bào [12].
Các tác nhân hoạt hóa hóa học thường được sử dụng bao gồm A23187 và ionomycin. Trong đó, phổ biến nhất trong lâm sàng hiện nay là A23187 (còn được gọi là calcimycin) là một kháng sinh nhóm carboxylic, có khả năng gắn với các cation hóa trị hai như Mn2+, Ca2+ và Mg2+, đồng thời vận chuyển tự do các ion này qua tất cả các màng sinh học. Dung dịch A23187 pha sẵn cho thấy tỷ lệ thành công cao [13]. Ionomycin là chất mang ion (ionophore) được sử dụng phổ biến thứ hai trong hoạt hóa noãn. Hợp chất này có khả năng kích hoạt cũng như kích thích biểu hiện gen [14] và dường như có hiệu lực mạnh, tính đặc hiệu cao hơn so với A23187 [12],[15].
Phương pháp AOA mới
Một trong những hướng tiếp cận được quan tâm nhiều nhất là AOA dựa trên PLCζ, bao gồm vi tiêm mRNA PLCζ hoặc protein PLCζ tái tổ hợp vào noãn sau ICSI [16]. Các phương pháp này đã cho thấy khả năng tạo ra dao động Ca2+ dạng sinh lý, tương tự như sau thụ tinh tự nhiên ở mô hình động vật, đồng thời cải thiện tỷ lệ thụ tinh trong các trường hợp thất bại thụ tinh liên tiếp do thiếu hụt PLCζ ở tinh trùng. Tuy nhiên, việc thiếu tiêu chuẩn định lượng PLCζ trong tinh trùng người và những lo ngại về kiểm soát liều lượng, thời gian biểu hiện vẫn đang hạn chế ứng dụng lâm sàng rộng rãi.
- Các hướng dẫn về việc sử dụng AOA
Vào tháng 8 năm 2023, hiệp hội các nhà khoa học sinh sản và lâm sàng (Association of Reproductive and Clinical Scientists – ARCS) phối hợp với Hiệp hội Sinh sản Vương quốc Anh (British Fertility Society – BFS) đã ban hành tài liệu cung cấp các khuyến nghị thực hành lâm sàng đối với AOA. Theo tài liệu này, AOA không nên dùng thường quy với ICSI do tính an toàn lâu dài và kết quả nâng cao tỷ lệ sinh sống chưa được xác định rõ. Có thể xem xét ICSI kết hợp AOA khi hai chu kỳ ICSI trước đó có tỷ lệ thụ tinh <30 % hoặc không thụ tinh hoàn toàn. Bệnh nhân phải được tư vấn rõ ràng về mức độ bằng chứng hạn chế và các rủi ro tiềm ẩn và phải được cung cấp dữ liệu an toàn liên quan đến kỹ thuật AOA được sử dụng [17].
Trong khuyến cáo thực hành tốt mới nhất về các kỹ thuật bổ trợ trong y học sinh sản của Hiệp hội Sinh sản và Phôi người Châu Âu (European Society of Human Reproduction and Embryology - ESHRE [TL8] ), AOA được xếp vào nhóm kỹ thuật bổ trợ (Add-on), chưa đủ bằng chứng để khuyến cáo sử dụng thường quy trong thực hành lâm sàng. Mặc dù một số nghiên cứu cho thấy AOA, đặc biệt là hoạt hoá hoá học bằng ion Ca2+, có thể cải thiện tỷ lệ thụ tinh trong những trường hợp thụ tinh thấp, thất bại thụ tinh và vô sinh nam nặng như globozoospermia, ESHRE nhấn mạnh rằng các bằng chứng hiện có chủ yếu đến từ những nghiên cứu cỡ mẫu nhỏ, thiết kế không đồng nhất, tiêu chí đánh giá khác nhau và thiếu các thử nghiệm ngẫu nhiên có đối chứng đủ mạnh. Đáng chú ý, dữ liệu về tính an toàn lâu dài vẫn còn rất hạn chế [18].
- Kết luận
Hỗ trợ hoạt hoá noãn nhân tạo là phương pháp bổ trợ, chỉ áp dụng có chọn lọc, thận trọng và dựa trên tư vấn đầy đủ cho bệnh nhân chọn lọc. Trong tương lai, các chiến lược AOA mô phỏng tốt hơn tín hiệu hoạt hoá sinh lý và các công cụ đánh giá chức năng PLCζ sẽ đóng vai trò then chốt trong việc tối ưu hoá hiệu quả và độ an toàn của phương pháp này.
TÀI LIỆU THAM KHẢO
1. Bhattacharya, S., A. Maheshwari, and J. Mollison, Factors associated with failed treatment: an analysis of 121,744 women embarking on their first IVF cycles. PLoS One, 2013. 8(12): p. e82249.
2. Vanden Meerschaut, F., et al., Assisted oocyte activation following ICSI fertilization failure. Reprod Biomed Online, 2014. 28(5): p. 560-71.
3. Sugita, H., et al., Molecular Mechanism of Oocyte Activation in Mammals: Past, Present, and Future Directions. Biomolecules, 2024. 14(3): p. 359.
4. Sanders, J.R. and K. Swann, Molecular triggers of egg activation at fertilization in mammals. Reproduction, 2016. 152(2): p. R41-R50.
5. Round spermatid nucleus injection (ROSNI). Fertil Steril, 2006. 86(5 Suppl 1): p. S184-6.
6. Tesarik, J. and M. Sousa, Key elements of a highly efficient intracytoplasmic sperm injection technique: Ca2+ fluxes and oocyte cytoplasmic dislocation. Fertil Steril, 1995. 64(4): p. 770-6.
7. Tao, Y., Oocyte activation during round spermatid injection: state of the art. Reprod Biomed Online, 2022. 45(2): p. 211-218.
8. Yanagida, K., Y. Fujikura, and H. Katayose, The present status of artificial oocyte activation in assisted reproductive technology. Reprod Med Biol, 2008. 7(3): p. 133-142.
9. Tanaka, A., et al., Ninety babies born after round spermatid injection into oocytes: survey of their development from fertilization to 2 years of age. Fertil Steril, 2018. 110(3): p. 443-451.
10. Tanaka, A. and S. Watanabe, How to improve the clinical outcome of round spermatid injection (ROSI) into the oocyte: Correction of epigenetic abnormalities. Reprod Med Biol, 2023. 22(1): p. e12503.
11. Neri, Q.V., et al., Understanding fertilization through intracytoplasmic sperm injection (ICSI). Cell Calcium, 2014. 55(1): p. 24-37.
12. Nikiforaki, D., et al., Effect of two assisted oocyte activation protocols used to overcome fertilization failure on the activation potential and calcium releasing pattern. Fertil Steril, 2016. 105(3): p. 798-806.e2.
13. Ebner, T., et al., Application of a ready-to-use calcium ionophore increases rates of fertilization and pregnancy in severe male factor infertility. Fertil Steril, 2012. 98(6): p. 1432-7.
14. Santella, L. and B. Dale, Assisted yes, but where do we draw the line? Reprod Biomed Online, 2015. 31(4): p. 476-8.
15. Versieren, K., et al., Developmental competence of parthenogenetic mouse and human embryos after chemical or electrical activation. Reprod Biomed Online, 2010. 21(6): p. 769-75.
16. Kaltsas, A., et al., Phospholipase Cζ, the Molecular Spark of Fertilization and Male Infertility: Insights from Bench to Bedside. Medicina (Kaunas), 2025. 61(6).
17. (BFS), A.o.R.a.C.S.A.B.F.S., The Use of ICSI in ART – Joint BFS ARCS Guidelines. 2023.
18. Lundin, K., et al., Good practice recommendations on add-ons in reproductive medicine†. Hum Reprod, 2023. 38(11): p. 2062-2104.