CVPH. Ngô Thị Lan Phương
Đơn vị HTSS IVFMD Family, Bệnh viện Đa Khoa Gia Đình Đà Nẵng
Giới thiệu
Phân mảnh DNA tinh trùng (Sperm DNA fragmentation-SDF) ngày càng được công nhận là một dấu ấn sinh học quan trọng về khả năng sinh sản của nam giới, ảnh hưởng đến kết quả thụ thai tự nhiên và kết quả lâm sàng của các phương pháp hỗ trợ sinh sản. Do đó, xét nghiệm SDF được khuyến cáo là một xét nghiệm có giá trị đối với khả năng sinh sản của nam giới, đặc biệt trong các trường hợp vô sinh không rõ nguyên nhân, vô sinh do yếu tố nam giới, thất bại làm tổ nhiều lần (recurrent implantation failure-RIF) và sảy thai tái phát (recurrent pregnancy loss-RPL).
Không giống như các thông số tinh dịch thông thường, SDF phản ánh trực tiếp tính toàn vẹn của nhiễm sắc thể và tiềm năng di truyền của tinh trùng. Về mặt cơ chế, stress oxy hóa và apoptosis không hoàn chỉnh là những con đường chính dẫn đến tổn thương DNA. Ba cơ chế chính có thể dẫn đến SDF: (1) apoptosis không hoàn chỉnh, trong đó tinh trùng apoptosis không bị loại bỏ và được giải phóng với DNA bị phân mảnh do tác động của endonuclease; (2) quá trình trưởng thành chromatin bị lỗi, trong quá trình nén chromatin tinh trùng bình thường, các hư hỏng DNA không được sửa chữa, dẫn đến dễ bị tổn thương hơn bởi các yếu tố ngoại sinh; và (3) stress oxy hóa, trong đó các loại oxy phản ứng có thể trực tiếp ảnh hưởng DNA trong tinh hoàn hoặc khi tinh trùng di chuyển dọc theo đường sinh sản của nam giới [1]. Các thực hành trong phòng thí nghiệm, chẳng hạn như ly tâm, ủ kéo dài, đông lạnh và tiếp xúc với nhiệt độ hoặc ánh sáng không phù hợp có thể làm tăng các gốc oxy hoạt tính và làm tổn hại đến tính ổn định của DNA. Tương tự, các vật liệu được sử dụng trong phòng thí nghiệm thụ tinh trong ống nghiệm, bao gồm găng tay, chất phụ gia môi trường và hộp đựng, có thể giải phóng các hợp chất độc hại gây hại cho DNA tinh trùng. Trong khi một số thủ thuật phẫu thuật, chẳng hạn như phẫu thuật cắt bỏ giãn tĩnh mạch tinh hoàn, có thể cải thiện chất lượng tinh trùng, thì những thủ thuật khác, bao gồm lấy tinh trùng từ tinh hoàn, lại tiềm ẩn nguy cơ tổn thương oxy hóa. Mục đích của bài đánh giá này là tóm tắt các yếu tố phức tạp và các thực hành phòng thí nghiệm có thể làm tổn hại tính toàn vẹn DNA tinh trùng trong thụ tinh trong ống nghiệm (TTTON) [2].
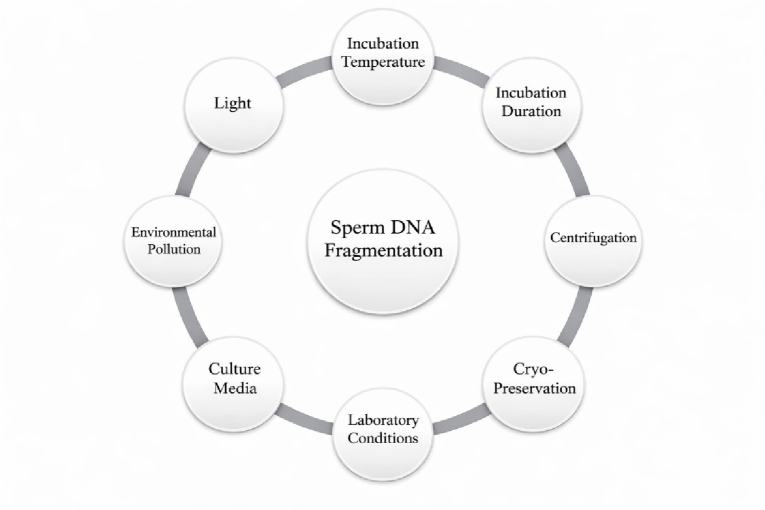
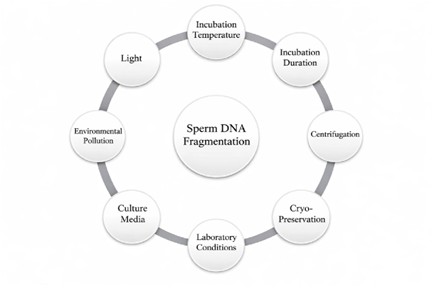
Hình 1. Các yếu tố do can thiệp y khoa góp phần tạo nên SDF khi thực hiện TTTON [2].
Các yếu tố vật lý
-
Nhiệt độ
Nhiệt độ ảnh hưởng đến tính toàn vẹn DNA ở tinh trùng. Ở nhiệt độ cao hơn, quá trình trao đổi chất của tinh trùng và sản sinh ROS (Reactive oxygen species) [DN1] tăng lên, dẫn đến tổn thương DNA nhanh hơn. Một số nghiên cứu cho thấy %DFI (DNA Fragmentation Index - chỉ số phân mảnh DNA tinh trùng) tăng theo thời gian khi ủ ở cả nhiệt độ phòng (room temperature-RT) và ở 37°C trong không khí, nhưng %DFI sau 24 giờ ở RT thấp hơn đáng kể so với ở 37°C (P < 0,05) [3]. Bên cạnh đó, tinh trùng được thao tác ở nhiệt độ phòng duy trì khả năng vận động và hình thái tốt hơn, đồng thời giảm thiểu hiện tượng apoptosis và hoại tử, so với việc ủ ở 35°C [4]. Tóm lại, việc giảm thiểu tiếp xúc với nhiệt độ cao và sử dụng các chiến lược làm mát nhẹ nhàng để bảo quản lâu dài là những biện pháp quan trọng để bảo tồn tính toàn vẹn của DNA trong quá trình xử lý in vitro.
-
Thời gian ủ
Thời gian ủ và bảo quản tinh trùng trong ống nghiệm có ảnh hưởng trực tiếp đến SDF. Sau khi xuất tinh, tinh trùng có thể tích lũy tổn thương DNA nếu thời gian xử lý kéo dài; các nghiên cứu cho thấy SDF tăng đáng kể chỉ sau vài giờ ủ, như sau 2 giờ ở nhiệt độ phòng hoặc 4 giờ ở 37°C [5]. Tinh trùng thu nhận từ tinh hoàn sau đông lạnh – rã đông cũng ghi nhận mức phân mảnh DNA tăng theo thời gian ủ, kèm giảm khả năng di động và bất thường hình thái [6]. Ngoài ra, các đứt gãy DNA vẫn có thể gia tăng trong quá trình ủ kéo dài ngay cả ở tinh trùng đã được chọn lọc. Vì vậy, tinh trùng nên được xử lý và sử dụng càng sớm càng tốt sau khi xuất tinh; trong thực hành lâm sàng thường bắt đầu chuẩn bị trong vòng 30-60 phút để hạn chế stress oxy hóa và hoạt động endonuclease làm tăng SDF [7].
-
Xử lý tinh trùng bằng phương pháp ly tâm
Ly tâm có thể làm tăng stress oxy hóa và gây tổn thương DNA tinh trùng. Do đó, các phòng thí nghiệm thường áp dụng lực ly tâm vừa phải (300-600 × g) trong 5-10 phút để hạn chế tổn thương. Mặc dù phương pháp ly tâm thang nồng độ (density gradient centrifugation -DGC) có thể cải thiện khả năng di động, một số nghiên cứu cho thấy phương pháp này không làm giảm đáng kể phân mảnh DNA do apoptosis [8]. Vì vậy, cần giảm thiểu lực, thời gian và số lần ly tâm nhằm hạn chế gia tăng SDF, đặc biệt khi kết hợp với các quy trình như đông lạnh - rã đông có thể làm tăng tổn thương DNA [9]. Gần đây, các kỹ thuật chọn lọc tinh trùng vi lưu được phát triển nhằm giảm stress cơ học, giúp chọn lọc tinh trùng di động với DNA nguyên vẹn hơn và có thể cải thiện kết quả TTTON [10].
-
Thao tác bằng piptette
Áp lực trong quá trình hút pipet, đặc biệt khi xử lý tinh dịch có độ nhớt cao, có thể làm tổn thương màng tinh trùng và có khả năng ảnh hưởng đến tính toàn vẹn DNA. Việc hút mạnh với đầu pipet có đường kính nhỏ có thể gây gãy đuôi hoặc tổn thương đầu tinh trùng. Do đó, các phòng thí nghiệm thường sử dụng đầu pipet có đường kính lớn hoặc đầu pipet được cắt và thực hiện các thao tác hút-đẩy nhẹ nhàng, ngắn để giảm lực và bảo toàn cấu trúc tế bào. Mặc dù chưa có nghiên cứu định lượng trực tiếp SDF do thao tác pipet, thao tác cơ học quá mức được cho là làm giảm khả năng sống của tinh trùng. Vì vậy, các thực hành như pha loãng tinh dịch nhớt với môi trường nuôi cấy, điều chỉnh áp suất hút tối thiểu trong ICSI và hạn chế số lần hút pipet được khuyến nghị để giảm tổn thương do thao tác kỹ thuật [11].
-
Đông lạnh tinh trùng
Bảo quản lạnh là kỹ thuật phổ biến trong hỗ trợ sinh sản nhưng có thể làm tăng SDF do sốc thẩm thấu, stress oxy hóa và hình thành tinh thể băng trong quá trình đông lạnh - rã đông. Một số nghiên cứu ghi nhận sự gia tăng đứt gãy DNA và hoạt hóa các con đường apoptosis sau rã đông [1]. So với đông lạnh chậm hoặc đông lạnh nhanh, thủy tinh hóa có xu hướng gây ít tổn thương DNA hơn và bảo tồn tốt hơn khả năng vận động, sức sống và tính toàn vẹn nhiễm sắc thể của tinh trùng, đặc biệt khi sử dụng các thiết bị như cryotop [12].
Dụng cụ trữ tinh trùng cũng có thể ảnh hưởng đến chất lượng tinh trùng. Tinh dịch thường được thu thập trong ống polypropylene hoặc thủy tinh vô trùng; một số loại nhựa có thể giải phóng các chất như bisphenol A liên quan đến suy giảm chất lượng tinh trùng và tăng tổn thương DNA [13]. Vì vậy, việc sử dụng vật liệu đạt chuẩn sinh học, không chứa BPA, ống vô trùng mới và niêm phong đúng cách được khuyến nghị để bảo tồn tính toàn vẹn DNA tinh trùng.
Các yếu tố hóa học
-
Môi trường
Thành phần môi trường nuôi cấy trong quá trình xử lý tinh trùng có vai trò quan trọng trong việc duy trì tính toàn vẹn DNA. Nhiều môi trường thương mại chứa các chất chống oxy hóa như taurine, EDTA và citrate nhằm giảm stress oxy hóa, một yếu tố chính gây phân mảnh DNA tinh trùng [14]. Tuy nhiên, môi trường chuẩn bị không phù hợp, nhiễm bẩn, pH hoặc độ thẩm thấu không tối ưu, cũng như tiếp xúc với hóa chất từ kháng sinh hoặc dụng cụ phòng thí nghiệm có thể làm tăng tổn thương DNA. Do đó, các phòng thí nghiệm thường sử dụng môi trường đạt chuẩn và làm việc trong điều kiện vô trùng; trong trường hợp stress oxy hóa cao, việc bổ sung các chất chống oxy hóa như glutathione có thể giúp giảm tổn thương DNA [15].
-
O2
Điều kiện bảo quản, đặc biệt là sự hiện diện của oxy, có ảnh hưởng đáng kể đến tính toàn vẹn DNA tinh trùng. Thiếu oxy có thể thúc đẩy hình thành ROS, gây tổn thương oxy hóa và đứt gãy DNA, bao gồm sự hình thành 8-hydroxy-2′-deoxyguanosine – một dấu ấn của stress oxy hóa, từ đó làm giảm khả năng vận động, sức sống và khả năng thụ tinh của tinh trùng. Ngoài ra, tình trạng thiếu oxy cũng có thể ảnh hưởng bất lợi đến chức năng tinh hoàn và chất lượng tinh trùng thông qua các cơ chế như tăng ROS, apoptosis tế bào mầm, viêm và biến đổi biểu sinh [16]. Tuy nhiên, điều kiện bảo quản tinh trùng hiện vẫn tương tự như đối với noãn và phôi, trong khi các đặc điểm sinh lý khác biệt cho thấy cần có thêm nghiên cứu để tối ưu hóa điều kiện nuôi cấy tinh trùng.
-
PVP (Polyvinylpyrrolidone)
Mặc dù được sử dụng phổ biến trong ICSI, tác động của PVP đối với tính toàn vẹn DNA tinh trùng vẫn chưa được nghiên cứu đầy đủ. PVP có thể gây tổn thương nhiễm sắc thể thông qua stress oxy hóa và thay đổi môi trường vi mô của tế bào, từ đó làm tăng phân mảnh DNA tinh trùng và có thể ảnh hưởng đến sự phát triển phôi. Nghiên cứu cho thấy SDF tăng và khả năng sống của tinh trùng giảm đáng kể chỉ sau 10 phút tiếp xúc với môi trường chứa PVP. Ngoài ra, sử dụng PVP nồng độ thấp (5%) trong ICSI được ghi nhận giúp giảm SDF và cải thiện tỷ lệ thụ tinh cũng như chất lượng phôi so với nồng độ cao hơn (10%) [17]. Vì vậy, cần kiểm soát chặt chẽ nồng độ và thời gian tiếp xúc PVP để hạn chế tổn thương DNA tinh trùng.
Yếu tố môi trường
-
Ánh sáng
Ánh sáng, đặc biệt là tia cực tím (ultraviolet -UV), có thể gây tổn thương DNA tinh trùng thông qua việc tạo ra ROS. Trong phòng thí nghiệm, ánh sáng huỳnh quang hoặc ánh sáng kính hiển vi thường ít gây ảnh hưởng đáng kể nếu mẫu được giữ ẩm, tuy nhiên tiếp xúc với nguồn UV cường độ cao (như đèn UV-C) có thể làm tăng phân mảnh DNA trong một số điều kiện. Vì vậy, các phòng thí nghiệm thường hạn chế chiếu sáng mạnh, giảm thời gian quan sát dưới kính hiển vi và bảo quản mẫu trong ống có nắp hoặc che chắn ánh sáng để giảm stress oxy hóa [18].
Ngược lại, một số nghiên cứu cho thấy ánh sáng laser đỏ 633 nm có thể cải thiện khả năng vận động của tinh trùng mà không làm tăng tổn thương DNA [19]. Tuy nhiên, nhìn chung việc hạn chế tiếp xúc trực tiếp với ánh sáng mạnh, đặc biệt là UV, vẫn được khuyến nghị để bảo vệ tính toàn vẹn DNA tinh trùng.
-
Điều kiện phòng thí nghiệm và môi trường ô nhiễm
Các yếu tố môi trường trong phòng thí nghiệm như chất lượng không khí, nhiệt độ và bảo trì thiết bị có thể ảnh hưởng gián tiếp đến tính toàn vẹn DNA tinh trùng. Phòng thí nghiệm IVF thường duy trì điều kiện kiểm soát (nhiệt độ ổn định, không khí lọc HEPA, nồng độ nội độc tố thấp) nhằm hạn chế ô nhiễm và stress môi trường. Các chất ô nhiễm không khí như các hợp chất hữu cơ bay hơi (Volatile organic compounds – VOC) hoặc hóa chất từ nhựa có thể làm tăng stress oxy hóa và dẫn đến phân mảnh DNA tinh trùng [20].
Sau khi tách khỏi huyết tương tinh dịch, tinh trùng trở nên nhạy cảm hơn với các chất gây ô nhiễm môi trường. Do đó, việc duy trì điều kiện phòng thí nghiệm tối ưu, bao gồm hệ thống lọc không khí HEPA, vật liệu không chứa VOC, môi trường nuôi cấy giàu chất chống oxy hóa và hạn chế tiếp xúc với khí dung là cần thiết để bảo tồn tính toàn vẹn nhiễm sắc thể tinh trùng [21].
-
Vật liệu làm găng tay trong phòng thí nghiệm
Găng tay phòng thí nghiệm là vật dụng thiết yếu trong ART, nhưng một số vật liệu và hóa chất từ găng tay có thể ảnh hưởng đến tính toàn vẹn DNA tinh trùng. Các hợp chất như VOC, hạt bột hoặc cặn hóa chất từ găng tay cao su có thể làm ô nhiễm môi trường nuôi cấy và làm tăng phân mảnh DNA tinh trùng. Mặc dù găng tay nitrile được xem là an toàn hơn, một số sản phẩm vẫn có thể giải phóng hợp chất lưu huỳnh, kẽm hoặc VOC. Trong khi đó, găng tay vinyl có thể giải phóng phthalate, các chất gây rối loạn nội tiết liên quan đến tổn thương nhiễm sắc thể và tăng SDF [20].
Vì vậy, các phòng thí nghiệm ART nên sử dụng găng tay chất lượng cao, không bột, ưu tiên nitrile, đồng thời kiểm tra và thay thế găng tay thường xuyên để giảm nguy cơ nhiễm bẩn hóa học và bảo vệ chất lượng tinh trùng cũng như kết quả TTTON.
Chọn lọc tinh trùng bằng phương pháp Microfluidics
Microfluidic sperm sorting là một kỹ thuật chọn lọc tinh trùng mới trong TTTON nhằm giảm tổn thương DNA so với các phương pháp chuẩn bị tinh trùng truyền thống như ly tâm thang nồng độ (density gradient centrifugation-DGC) và swim-up. Khác với các phương pháp dựa trên ly tâm, microfluidic sử dụng các kênh vi lưu để mô phỏng môi trường sinh lý của đường sinh sản nữ, cho phép tinh trùng di động tự bơi qua các vi kênh và được chọn lọc mà không chịu tác động của lực cơ học mạnh. Nhờ tránh quá trình ly tâm có thể làm tăng sản sinh ROS và stress cơ học – phương pháp này có khả năng thu được quần thể tinh trùng có tính toàn vẹn DNA tốt hơn. Một nghiên cứu so sánh trực tiếp cho thấy tinh trùng được chọn bằng microfluidic có mức phân mảnh DNA gần như không phát hiện được (median DFI ≈ 0%), thấp hơn đáng kể so với mẫu xử lý bằng DGC kết hợp swim-up (median DFI ≈ 6%) và thấp hơn nhiều so với mẫu tinh dịch ban đầu (DFI ≈ 21%) [22]. Ngoài ra, các nghiên cứu gần đây cũng ghi nhận microfluidic tạo ra quần thể tinh trùng có DFI thấp hơn đáng kể so với DGC và swim-up, đồng thời cải thiện khả năng vận động và giảm các dấu hiệu stress oxy hóa trong ty thể [23]. Những kết quả này cho thấy microfluidic là một phương pháp chọn lọc tinh trùng đầy hứa hẹn nhằm giảm SDF và có thể cải thiện chất lượng tinh trùng trước các kỹ thuật hỗ trợ sinh sản.
Kết luận
Tính toàn vẹn DNA tinh trùng là yếu tố quan trọng đối với khả năng sinh sản nam giới và hiệu quả của ART. Các yếu tố trong phòng thí nghiệm như ly tâm quá mức, ủ kéo dài, nhiệt độ hoặc pH không phù hợp và tiếp xúc với ROS có thể làm tăng phân mảnh DNA. Ngoài ra, vật liệu sử dụng như môi trường nuôi cấy, chất bảo quản lạnh, găng tay hoặc dụng cụ nhựa cũng có thể ảnh hưởng đến chất lượng DNA tinh trùng.
Vì vậy, cần áp dụng các quy trình xử lý tinh trùng nhẹ nhàng, sử dụng vật tư an toàn và kiểm soát môi trường phòng thí nghiệm chặt chẽ để giảm stress oxy hóa. Đồng thời, phát triển các phương pháp đánh giá DNA và kỹ thuật chọn lọc tinh trùng mới, như vi dòng chảy, mở ra hướng đi mới giúp cải thiện hiệu quả TTTON.
Tài liệu tham khảo
1. Agarwal, A., Farkouh, A., Parekh, N., Zini, A., Arafa, M., Kandil, H., Tadros, N., Busetto, G. M., Ambar, R., Parekattil, S., Boitrelle, F., Sallam, H., Jindal, S., Ko, E., Simopoulou, M., Park, H. J., Sadighi, M. A., Saleh, R., Ramsay, J., … Shah, R. (2022). Sperm DNA Fragmentation: A Critical Assessment of Clinical Practice Guidelines. The World Journal of Men’s Health, 40(1), 30–37. https://doi.org/10.5534/wjmh.210056
2. Vasiee, M., & Agha-Rahimi, A. (2026). Complex in vitro fertilization laboratory factors affecting sperm DNA integrity: A narrative review. International Journal of Reproductive Biomedicine, 23(12), 971–984. https://doi.org/10.18502/ijrm.v23i12.20710
3. Matsuura, R., Takeuchi, T., & Yoshida, A. (2010). Preparation and incubation conditions affect the DNA integrity of ejaculated human spermatozoa. Asian Journal of Andrology, 12(5), 753–759. https://doi.org/10.1038/aja.2010.46
4. Karimi Zarchi, M., Maleki, B., Dehghani Ashkezari, M., Motamed Zadeh, L., & Agha-Rahimi, A. (2020). The Effects of In Vitro Incubation of Asthenoteratozoospermic Semen after Density Gradient Centrifugation at Room Temperature and 37°C on Sperm Parameters, Chromatin Quality and DNA Fragmentation in a Short Time Period. Journal of Reproduction & Infertility, 21(4), 275–282. https://doi.org/10.18502/jri.v21i4.4332
5. Sabbaghian, M., Hosseinifar, H., Rafaee, A., & Gilani, M. A. S. (2022). Assessment of the Impact Induced by Different Incubation Time, Storage Time, Storage Medium and Thawing Methods on Sperm DNA Fragmentation Assay: A Before–After Study. Journal of Human Reproductive Sciences, 15(4), 377–381. https://doi.org/10.4103/jhrs.jhrs_145_22
6. Beigi, S. A. D., Khalili, M. A., Nabi, A., Hosseini, M., Sarcheshmeh, A. A., & Sabour, M. (2022). Prolonged semen incubation alters the biological characteristics of human spermatozoa. Clinical and Experimental Reproductive Medicine, 49(4), 270–276. https://doi.org/10.5653/cerm.2022.05435
7. Dalzell, L. H., McVicar, C. M., McClure, N., Lutton, D., & Lewis, S. E. M. (2004). Effects of short and long incubations on DNA fragmentation of testicular sperm. Fertility and Sterility, 82(5), 1443–1445. https://doi.org/10.1016/j.fertnstert.2004.04.053
8. Stevanato, J., Bertolla, R. P., Barradas, V., Spaine, D. M., Cedenho, A. P., & Ortiz, V. (2008). Semen processing by density gradient centrifugation does not improve sperm apoptotic deoxyribonucleic acid fragmentation rates. Fertility and Sterility, 90(3), 889–890. https://doi.org/10.1016/j.fertnstert.2007.01.059
9. Marzano, G., Chiriacò, M. S., Primiceri, E., Dell’Aquila, M. E., Ramalho-Santos, J., Zara, V., Ferramosca, A., & Maruccio, G. (2020). Sperm selection in assisted reproduction: A review of established methods and cutting-edge possibilities. Biotechnology Advances, 40, 107498. https://doi.org/10.1016/j.biotechadv.2019.107498
10. Gisbert Iranzo, A., Cano-Extremera, M., Hervás, I., Falquet Guillem, M., Gil Juliá, M., Navarro-Gomezlechon, A., Pacheco-Rendón, R. M., & Garrido, N. (2025). Sperm Selection Using Microfluidic Techniques Significantly Decreases Sperm DNA Fragmentation (SDF), Enhancing Reproductive Outcomes: A Systematic Review and Meta-Analysis. Biology, 14(7), 792. https://doi.org/10.3390/biology14070792
11. Rochdi, C., Allai, L., Bellajdel, I., Taheri, H., Saadi, H., Mimouni, A., & Choukri, M. (2024). Evaluation of Sperm DNA Fragmentation Using Halosperm Technique after the Freezing–Thawing Process in Men: A Study on the Validation of the SCD Protocol. Journal of Reproduction & Infertility, 25(1), 12–19. https://doi.org/10.18502/jri.v25i1.15194
12. Hosseini, A., Khalili, M. A., Talebi, A. R., Agha-Rahimi, A., Ghasemi-Esmailabad, S., Woodward, B., & Yari, N. (2019). Cryopreservation of Low Number of Human Spermatozoa; Which is Better: Vapor Phase or Direct Submerging in Liquid Nitrogen? Human Fertility, 22(2), 126–132. https://doi.org/10.1080/14647273.2018.1456681
13. Sharma, A., Mollier, J., Brocklesby, R. W. K., Caves, C., Jayasena, C. N., & Minhas, S. (2020). Endocrine‐disrupting chemicals and male reproductive health. Reproductive Medicine and Biology, 19(3), 243–253. https://doi.org/10.1002/rmb2.12326
14. Chi, H. J., Kim, J. H., Ryu, C. S., Lee, J. Y., Park, J. S., Chung, D. Y., Choi, S. Y., Kim, M. H., Chun, E. K., & Roh, S. I. (2008). Protective effect of antioxidant supplementation in sperm-preparation medium against oxidative stress in human spermatozoa. Human Reproduction, 23(5), 1023–1028. https://doi.org/10.1093/humrep/den060
15. Agarwal, A., & Said, T. M. (2005). Oxidative stress, DNA damage and apoptosis in male infertility: A clinical approach. BJU International, 95(4), 503–507. https://doi.org/10.1111/j.1464-410X.2005.05328.x
16. Li, Z., Wang, S., Gong, C., Hu, Y., Liu, J., Wang, W., Chen, Y., Liao, Q., He, B., Huang, Y., Luo, Q., Zhao, Y., & Xiao, Y. (2021). Effects of Environmental and Pathological Hypoxia on Male Fertility. Frontiers in Cell and Developmental Biology, 9, 725933. https://doi.org/10.3389/fcell.2021.725933
17. Sabour, M., Agha-Rahimi, A., Dehghani Ashkezari, M., Seifati, S. M., Anbari, F., & Nabi, A. (2022). Prolonged exposure of human spermatozoa in polyvinylpyrrolidone has detrimental effects on sperm biological characteristics. Andrologia, 54(6), e14402. https://doi.org/10.1111/and.14402
18. Catalán, J., Yánez-Ortiz, I., Gacem, S., Papas, M., Bonet, S., Rodríguez-Gil, J. E., Yeste, M., & Miró, J. (2021). The Effects of Red Light on Mammalian Sperm Rely upon the Color of the Straw and the Medium Used. Animals : an Open Access Journal from MDPI, 11(1), 122. https://doi.org/10.3390/ani11010122
19. Preece, D., Chow, K. W., Gomez-Godinez, V., Gustafson, K., Esener, S., Ravida, N., Durrant, B., & Berns, M. W. (2017). Red light improves spermatozoa motility and does not induce oxidative DNA damage. Scientific Reports, 7, 46480. https://doi.org/10.1038/srep46480
20. Agarwal, N., Chattopadhyay, R., Ghosh, S., Bhoumik, A., Goswami, S. K., & Chakravarty, B. (2017). Volatile organic compounds and good laboratory practices in the in vitro fertilization laboratory: The important parameters for successful outcome in extended culture. Journal of Assisted Reproduction and Genetics, 34(8), 999–1006. https://doi.org/10.1007/s10815-017-0947-x
21. Sciorio, R., Greco, P. F., Greco, E., Tramontano, L., Elshaer, F. M., & Fleming, S. (2025). Potential effects of environmental toxicants on sperm quality and potential risk for fertility in humans. Frontiers in Endocrinology, 16, 1545593. https://doi.org/10.3389/fendo.2025.1545593
22. Quinn, M. M., Jalalian, L., Ribeiro, S., Ona, K., Demirci, U., Cedars, M. I., & Rosen, M. P. (2018). Microfluidic sorting selects sperm for clinical use with reduced DNA damage compared to density gradient centrifugation with swim-up in split semen samples. Human Reproduction, 33(8), 1388–1393. https://doi.org/10.1093/humrep/dey239
23. Wen, Z.-N., Duan, L., Chen, Y., Qiu, Q.-H., Liu, G., Luo, N., Li, P.-H., Tian, E.-P., & Ge, R.-S. (2025). Comparative Efficacy of Swim-Up, Density-Gradient Centrifugation, and Microfluidic Sorting in Sperm Preparation, and the Impact on Motility, Morphology, and DNA Integrity. International Journal of General Medicine, 18, 2355–2366. https://doi.org/10.2147/IJGM.S517575