CN. Liên Mỹ Dinh – IVFMD SIH, Bệnh viện Phụ sản Quốc tế Sài Gòn
-
Giới thiệu
Sự trưởng thành noãn in vivo phụ thuộc chặt chẽ vào mạng lưới giao tiếp hai chiều giữa noãn và các tế bào sinh dưỡng hoặc giữa các tế bào sinh dưỡng với nhau thông qua cầu nối liên bào (Gap Junctions – GJs), sợi bào tương xuyên màng (Transzonal Projections – TZP) và các yếu tố tiết từ noãn (Oocyte Secreted Factors – OSFs) như GDF9 và BMP15. Mặc dù đã có những cải tiến về mặt quy trình và môi trường nuôi cấy, hiệu quả của nuôi trưởng thành noãn non trong ống nghiệm (In vitro Maturation – IVM) vẫn thấp hơn so với điều kiện in vivo về tỷ lệ phôi nang và tỷ lệ thai, một phần do chất lượng noãn bị ảnh hưởng bởi môi trường nuôi cấy dưới mức tối ưu, không mô phỏng hoàn toàn được môi trường in vivo. Sự chênh lệch này thúc đẩy các nỗ lực nhằm hiểu rõ hơn về các cơ chế ảnh hưởng đến năng lực noãn nhằm tối ưu hoá điều kiện nuôi cấy (1).
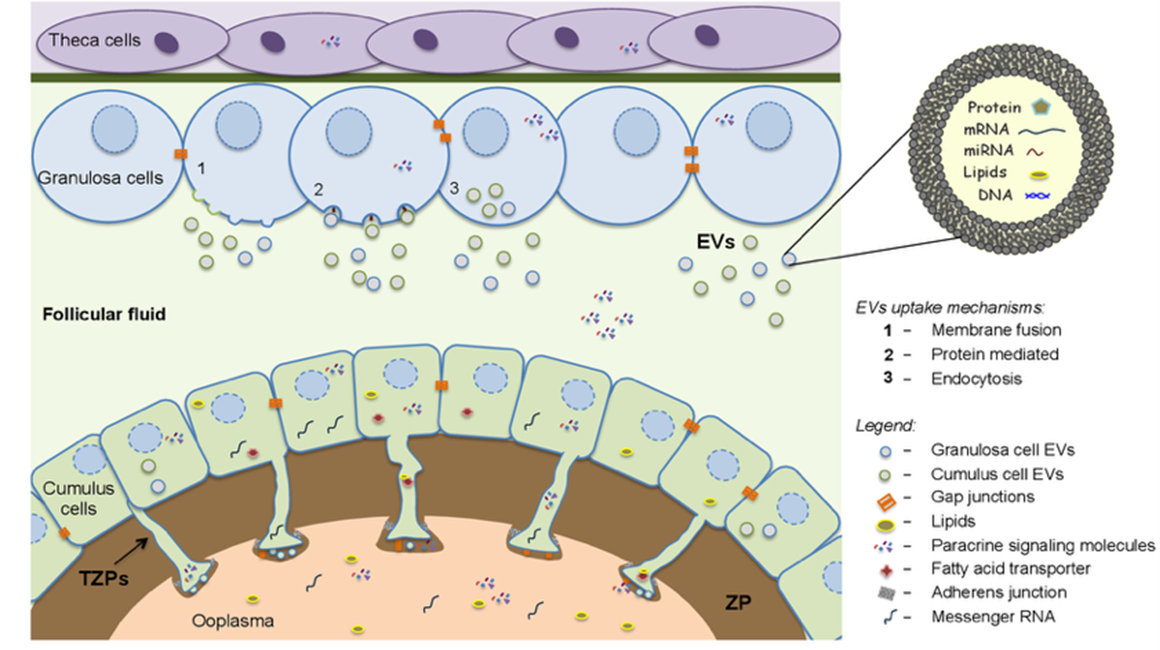
Vi môi trường nang noãn được duy trì thông qua mạng lưới tương tác sinh lý chặt chẽ giữa noãn, tế bào hạt (Granulosa Cells – GCs) và dịch nang (Follicular Fluid – FF). Trong đó, FF cung cấp một nguồn phân tử sinh học dồi dào, bao gồm các chất chuyển hoá, yếu tố tăng trưởng, hormone và đặc biệt là túi ngoại bào (Extracellular Vesicles – EVs). Bên cạnh các cơ chế giao tiếp tế bào đã được nghiên cứu nhiều trước đây như GJs và TZPs, túi ngoại bào dịch nang (ffEVs - follicular fluid Extracellular Vesicles) do các tế bào sinh dưỡng buồng trứng tiết ra đã được xác định là một cơ chế truyền tin tín hiệu phân tử mới, đóng vai trò then chốt trong việc điều hoà sự trưởng thành của noãn và hỗ trợ phát triển phôi giai đoạn sớm (1),(2),(3). Về mặt bản chất, EVs là các hạt nano có cấu trúc màng lipid kép, đảm nhiệm chức năng vận chuyển các phân tử tín hiệu đặc hiệu đến tế bào đích, qua đó tác động trực tiếp đến các tín hiệu cận tiết (paracrine) trong giao tiếp tế bào. Các nghiên cứu tiến hành trên mô hình người, bò và ngựa đã cung cấp bằng chứng rõ ràng rằng ffEVs có khả năng thay đổi hệ phiên mã và hệ protein của tế bào cumulus (Cumulus Cells – CCs) cũng như noãn, từ đó định hình năng lực phát triển của noãn. Nhìn chung, mặc dù các tác động có lợi của ffEVs lên chất lượng noãn đã được ghi nhận rộng rãi, vai trò và cơ chế điều hoà cụ thể của chúng trong mạng lưới chuyển hoá của noãn vẫn là một khía cạnh cần được xác minh thêm trong các nghiên cứu tương lai (2).
Bài viết này cung cấp khái quát về những hiểu biết hiện tại đối với vai trò của EVs trong sự trưởng thành noãn và phát triển phôi.
-
Tổng quan về túi ngoại bào dịch nang
Túi ngoại bào dịch nang là một quần thể hạt nano không đồng nhất, mang các đặc điểm đặc trưng của tế bào mẹ và trạng thái sinh lý của nang noãn. Việc hiểu rõ cấu trúc và nguồn gốc của ffEVs là điều kiện tiên quyết để ứng dụng mở rộng trong nghiên cứu và lâm sàng.
ffEVs đóng vai trò quan trọng trong giao tiếp tế bào giúp vận chuyển các tín hiệu từ các tế bào sinh dưỡng đến noãn. Sự trao đổi này diễn ra thông qua các TZPs, cho phép EVs và các thành phần bên trong chúng xâm nhập vào noãn. EVs vận chuyển các RNA mã hóa và không mã hóa, chẳng hạn như microRNA (miRNAs), và các phân tử sinh học khác như DNA, RNA, lipid, protein giúp kiểm soát sự biểu hiện của các gen trong noãn (4),(5).
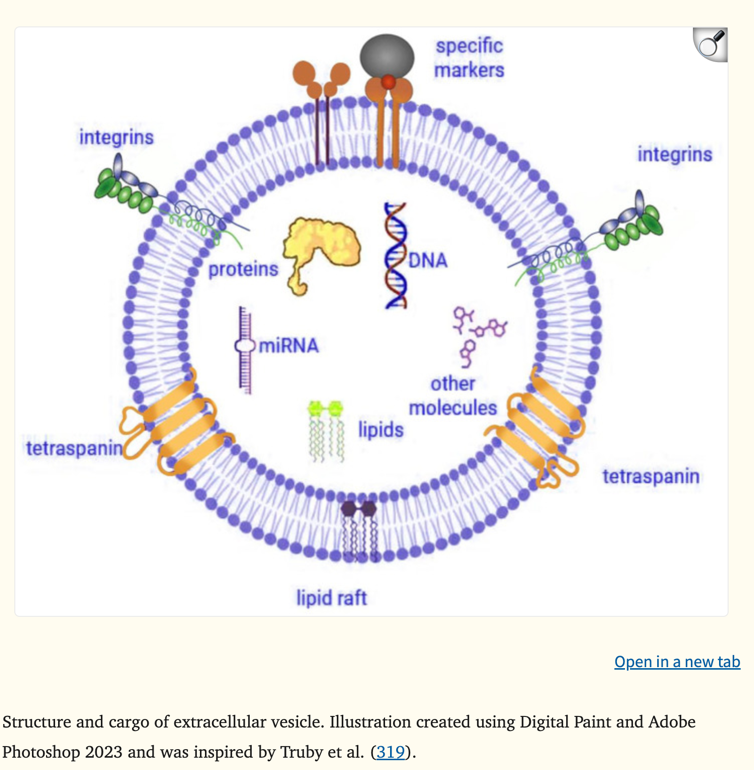
Hình 1: Cấu trúc và cargo của túi ngoại bào (5)
-
Định nghĩa và phân loại theo MISEV 2023
Theo các hướng dẫn mới nhất MISEV 2023 từ Hiệp hội Quốc tế về Túi ngoại bào (International Society for Extracellular Vesicles – ISEV), thuật ngữ túi ngoại bào được sử dụng để chỉ tất cả các hạt có màng lipid kép được giải phóng bởi tế bào và không có khả năng tự sao chép. Việc phân loại dựa trên con đường sinh học (exosome, microvesicles, ectosomes) hiện nay gặp nhiều thách thức do sự chồng chéo về kích thước và thành phần protein, vì vậy MISEV2023 khuyến nghị sử dụng các đặc điểm vật lý (kích thước), thành phần sinh hoá, nguồn gốc tế bào để phân loại (Bảng 1).
Bảng 1: Các phân loại của EVs (5)
|
Phân loại |
Kích thước (nm) |
Nguồn gốc |
Dấu ấn |
Chức năng |
|
EVs nhỏ (sEVs) |
<200nm |
Endosomal (thể đa túi) hoặc không xác định |
CD9, CD63, CD81, TSG101, Alix |
Tham gia vào quá trình giao tiếp liên bào, sự vận động, biệt hoá tăng sinh và sự chết theo chương trình (apoptosis) của tế bào và khả năng miễn dịch |
|
EVs trung bình/lớn (m/lEVs) |
>200nm |
Nảy chồi từ màng sinh chất (plasma membrane budding) |
Annexin A1, Integrins |
Tham gia vào quá trình giao tiếp tế bào, sửa chữa mô, đông máu và các đáp ứng miễn dịch |
|
Apoptotic Bodies |
500-5000 nm |
Được hình thành trong quá trình chết tế bào theo chương trình |
Histones, phân mảnh DNA |
Tạo điều kiện xử lý các tế bào chết (apoptotic cells), có thể ảnh hưởng tới đáp ứng miễn dịch |
Trong dịch nang, sEVs (thường được gọi là exosomes trong các tài liệu cũ) là đối tượng được nghiên cứu nhiều nhất do khả năng mang tải lượng sinh học đa dạng và khả năng xâm nhập vào tế bào đích một cách hiệu quả (5),(6).
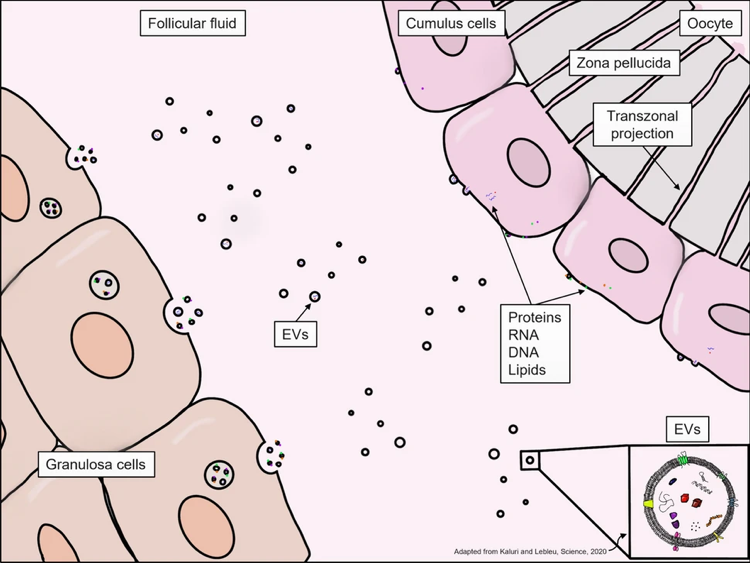
Hình 2: Sơ đồ truyền tín hiệu của túi ngoại bào trong nang noãn (7)
-
Nguồn gốc sinh học trong nang noãn
Mọi loại tế bào đều có khả năng giải phóng các EVs, nhưng thành phần bên trong (cargo) của chúng có thể mang tính đặc hiệu cho từng loại tế bào. Tất cả các tế bào hiện diện trong một nang noãn (chủ yếu là GCs, nhưng cũng bao gồm tế bào vỏ Theca Cells, CCs và noãn) đều có thể giải phóng EVs vào FF. Giả thuyết đặt ra rằng ffEVs có thể bao gồm hỗn hợp các EVs có nguồn gốc khác nhau. Việc phân tích nguồn gốc của ffEvs sẽ cung cấp những thông tin giá trị, xác định tiềm năng của ffEVs trong nang noãn và tác động chức năng của ffEVs đối với noãn (8):
-
Tế bào hạt (GCs): Đây là nguồn cung cấp ffEVs chính. Khi nang noãn phát triển, các tế bào hạt tăng sinh mạnh mẽ và giải phóng một lượng lớn EVs vào dịch nang để giao tiếp với các tế bào vỏ và noãn (8),(9),(10).
-
Tế bào vỏ (Theca Cells – TCs): Đóng góp vào thành phần protein và lipid của dịch nang thông qua việc tiết ffEVs (8).
-
Tế bào cumulus (CCs): Tiết ra các EVs tương tác trực tiếp và được vận chuyển vào noãn trong giai đoạn trưởng thành cuối cùng, đặc biệt là trong quá trình giãn nỡ khối cumulus (9),(11).
-
Sự thay đổi tính chất EVs theo kích thước nang noãn
Nồng độ và thành phần cargo của ffEVs không cố định mà phản ánh chính xác trạng thái của nang noãn. Các nang noãn nhỏ (<3-5mm) chứa các ffEVs giàu các yếu tố thúc đẩy sự tăng sinh tế bào, trong khi các nang noãn lớn (>9mm) hoặc nang tiền rụng trứng lại chứa các ffEVs mang những tín hiệu liên quan đến sự trưởng thành của noãn và đáp ứng với đỉnh LH (12). Nghiên cứu so sánh ffEVs từ các nang lớn và nhỏ ở lợn đã xác định được hàng trăm miRNA và protein biểu hiện khác biệt, điều này chứng minh rằng ffEVs là một hệ thống truyền tin động (dynamic signaling system) (13).
-
RNA không mã hoá (miRNA và lncRNA) trong ffEVs và cơ chế điều hoà
Các RNA không mã hoá, cụ thể là microRNA (miRNA) và long non-coding RNA (lncRNA), là hai loại cargo quan trọng nhất được tìm thấy trong dịch nang (7). Các RNA không mã hoá (miRNA và lncRNA) có thể được giải phóng ra dịch nang và tồn tại ở dạng tự do hoặc được bao bọc lại bởi ffEVs nhằm bảo vệ các phân tử này khỏi sự phân huỷ của enzyme ribonuclease (14).
-
Micro RNA (miRNA)
miRNA là những phân tử RNA nhỏ (khoảng 22 nucleotides) không trực tiếp mã hoá protein, hoạt động bằng cách liên kết bổ trợ với mRNA mục tiêu để ức chế dịch mã hoặc gây phân huỷ mRNA
Bảng 2: Tóm tắt các miRNA biểu hiện khác biệt và các gene đích, con đường tín hiệu và liên quan lâm sàng của chúng (14).
|
microRNA |
Gene đích |
Tác động sinh học |
|
miR-202-5p |
LHCGR |
Thúc đẩy năng lực giảm phân của noãn bằng cách điều hòa tín hiệu thụ thể LH, có nhiều trong các noãn chất lượng cao. |
|
miR-224 |
CYP19A1 (gene SMAD4 trong con đường TGF-beta) |
Tăng cường biểu hiện aromatase và sinh tổng hợp estradiol, thúc đẩy sự tăng sinh tế bào hạt và sự phát triển của nang noãn. |
|
miR-21 |
PDCD4, RECK |
Ngăn chặn apoptosis (anti-apoptosis) và duy trì khả năng sống của tế bào hạt, hỗ trợ sự hình thành mạch trong nang noãn thông qua ức chế tái cấu trúc cơ chất. Kích hoạt con đường PI3K/AKT, điều hoà PTEN |
|
miR-151-3p |
BCL2L1 |
Nhắm mục tiêu vào BCL2L1 nhằm anti-apoptosis trong các tế bào hạt; sự giảm biểu hiện của nó thúc đẩy apoptosis, góp phần gây thoái hóa nang noãn. |
-
Long Non-coding RNA (lncRNA)
lncRNA là các phân tử RNA dài hơn 200 nucleotide, không mã hoá protein nhưng có khả năng tương tác với DNA, RNA và protein. Trong ffEVs, lncRNA đóng vai trò làm thay đổi tính khả dụng của miRNA đối với mRNA mục tiêu. Một ví dụ điển hình là lncRNA LIPE-AS1 được tìm thấy trong exosome dịch nang của bệnh nhân buồng trứng đa nang. LIPE hoạt động thông qua trục LIPE-AS1/miR4306/LHCGR. Cụ thể, trong điều kiện bình thường, miR4306 sẽ ức chế biểu hiện của thụ thể LH (LHCGR). Tuy nhiên, khi LIPE-AS1 tăng cao, sẽ tương tác với miR4306, làm gián đoạn quá trình steroid hoá và gây ra tình trạng dừng trưởng thành của noãn (15).
-
Công nghệ tinh chế ffEVs và các công nghệ tinh chế hiện tại
Để ứng dụng thành công ffEVs vào kỹ thuật IVM, quy trình thu hồi và xác định đặc tính của chúng phải tuân thủ các tiêu chuẩn nghiêm ngặt (như hướng dẫn của MISEV) nhằm đảm bảo độ tinh khiết và chức năng sinh học.
-
Công nghệ tinh chế ffEVs hiện tại
Việc tinh chế ffEVs được thực hiện qua một chuỗi các bước nhằm loại bỏ tạp chất (tế bào, mảnh vụn, protein hoà tan) để thu được các hạt nano tinh khiết. Nghiên cứu mới nhất của Fernanda (2026) đã mô tả các bước tinh chế ffEVs từ dịch nang bò:
-
Ly tâm phân đoạn (Differential Centrifugation): FF được thu thập từ các nang 3-6mm và ly tâm ở 4°C qua 3 giai đoạn: 300g trong 10 phút (loại bỏ tế bào), 2500g trong 10 phút (loại bỏ mảnh vụn tế bào) và 16500g trong 30 phút (loại bỏ các thể apoptotic và các túi lớn).
-
Lọc cơ học: Dịch sau đó được lọc qua màng 0,22mm để đảm bảo chỉ còn các hạt có kích thước nhỏ hơn ngưỡng này.
-
Sắc ký loại trừ kích thước (Size Exclusion Chromatography – SEC): Sử dụng cột Izon qEV1 35 nm Gen 2. Dịch nang được nạp vào cột và rửa bằng PBS để thu nhận các phân đoạn giàu EV (thường là các phân đoạn từ 5-9, tổng cộng khoảng 2,5mL).
-
Siêu ly tâm (Ultracentrifugation – UC): Các phân đoạn giàu EVs được siêu ly tâm ở 100.000g trong 70 phút ở 4°C để thu được tủa (pellet) ffEVs tinh khiết.
-
Đánh giá sau tinh chế
Để xác nhận sản phẩm thu được thực sự là ffEVs và đảm bảo độ tinh khiết, nhóm nghiên cứu sử dụng 3 khía cạnh sau:
-
Phân tích theo dõi hạt (Nanoparticle Tracking Analysis – NTA): Sử dụng hệ thống NanoSight NS300 để xác định nồng độ hạt (trung bình 4,5x1011 hạt/mL) và kích thước (đường kính trung bình khoảng 203nm).
-
Kính hiển vi điện tử truyền qua (Transmission Electron Microscopic – TEM): Xác nhận hình thái đặc trưng của túi ngoại bào là dạng cốc (cup-shaped) với đường kính dưới 200nm.
-
Flow Cytometry:
-
Dấu ấn dương tính: CD81, CD9 (tetraspanins) và Syntenin.
-
Dấu ấn âm tính: Calnexin (một protein của lưới nội chất, dùng để kiểm tra xem có bị nhiễm bẩn tế bào hay không). Kết quả cho thấy Calnexin không được phát hiện, chứng minh độ tinh khiết cao (1).
-
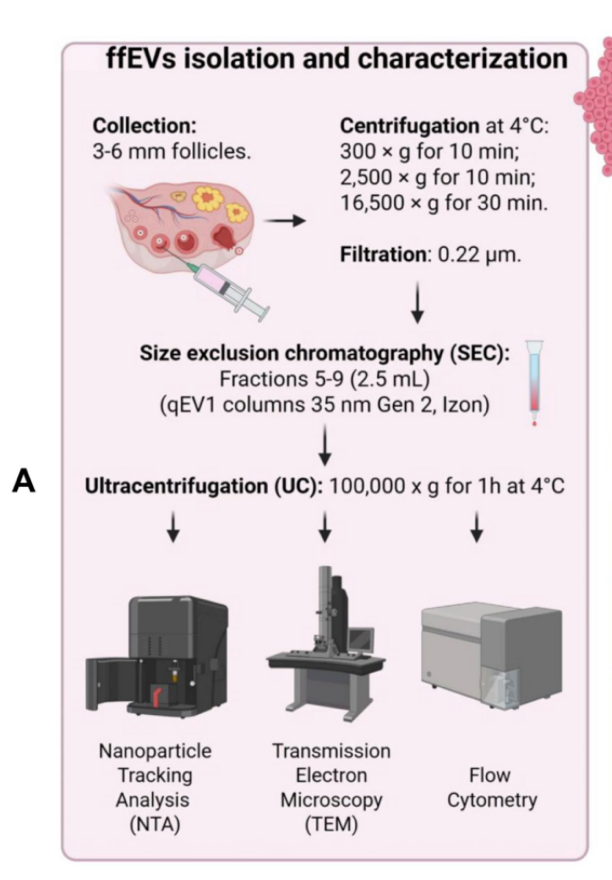
Hình 2: Các bước phân lập ffEVs và đánh giá sau phân lọc (1)
-
Tác động của ffEVs đến quá trình trưởng thành noãn non trong ống nghiệm
Nuôi trưởng thành noãn non trong ống nghiệm thường gặp thách thức về tỷ lệ thai thấp do noãn bị tách khỏi môi trường dịch nang giàu tín hiệu quá sớm. Bổ sung ffEVs vào môi trường IVM đã được chứng minh hiệu quả vượt trội trong việc tái tạo môi trường sinh lý.
-
Các nghiên cứu trên mô hình động vật
-
Thúc đẩy tăng năng lực tế bào chất: Việc bổ sung ffEVs từ các nang noãn khoẻ mạnh vào môi trường IVM bò làm tăng hoạt động của ty thể và giảm mức độ các gốc tự do (Reactive Oxygen Species – ROS) trong noãn. Mặc dù tỷ lệ trưởng thành nhân có thể không thay đổi lớn, nhưng năng lực phát triển của phôi sau thụ tinh (tỷ lệ tạo phôi nang) được cải thiện rõ rệt (1).
-
Điều hoà chuyển hoá lipid: ffEVs thúc đẩy sự tích luỹ các giọt lipid bên trong noãn bò, cung cấp nguồn năng lượng dự trữ thiết yếu cho sự phân chia tế bào sau này. Điều này liên quan đến việc điều hoà các gene chuyển hoá mỡ như CPT1B (16).
-
Mở rộng khối cumulus: ffEVs từ các nang lớn chứa các tín hiệu giúp tế bào cumulus giãn nở tối đa, một chỉ số quan trọng của sự trưởng thành noãn. Các gen như HAS2, TNFAIP6 được kích hoạt mạnh mẽ khi có sự hiện diện của ffEVs (3).
-
Các nghiên cứu và ứng dụng trên người
Trên người, ffEVs đang mở ra hy vọng cho những bệnh nhân có đáp ứng buồng trứng kém hoặc những người có noãn GV cần thực hiện rescue IVM sau chọc hút. Việc bổ sung ffEVs từ nang trưởng thành (MII-ffEVs) vào môi trường nuôi cấy noãn GV người đã làm tăng tỷ lệ trưởng thành thêm 22,8 ± 9,4% so với nhóm chứng. Noãn được xử lý với ffEVs có sự thay đổi đáng kể về proteome, đặc biệt là tăng protein HAS1 (Hyaluronan Synthase 1) (gấp 6,55 lần) – protein đóng vai trò quan trọng trong cấu trúc chất nền ngoại bào (extracellular matrix) của noãn (17).
-
Kết luận
Túi ngoại bào dịch nang là một thành phần không thể thiếu trong mạng lưới giao tiếp hai chiều giữa noãn và tế bào hạt. Với tải lượng cargo phong phú là các miRNA, lncRNA và protein điều hòa, ffEVs đóng vai trò như một bộ điều khiển tinh vi giúp noãn đạt được năng lực phát triển tối ưu. Việc ứng dụng các phương pháp tinh chế hiện đại như SEC và TFF, tuân thủ các hướng dẫn MISEV 2023, cho phép khai thác tiềm năng của ffEVs trong việc cải thiện đáng kể kết quả IVM trên cả động vật và người. Dù vẫn còn những thách thức về tiêu chuẩn hóa và chi phí, ffEVs chắc chắn sẽ là chìa khóa để mở ra kỷ nguyên mới của y học sinh sản cá thể hóa, tăng tỷ lệ thành công cho một chu kỳ thụ tinh trong ống nghiệm.
Từ khoá: túi ngoại bào/trưởng thành noãn non trong ống nghiệm/IVM/túi ngoại bào dịch nang/ffEVs
Tài liệu tham khảo
1. Schneberger F, Bridi A, Ferraz PA, De Oliveira JRQ, Munhoz LC, Sangalli JR, et al. Follicular fluid extracellular vesicles improve bovine oocyte quality via lipid and mitochondrial modulation. Front Vet Sci. 2026 Jan 14;12:1703475. doi:10.3389/fvets.2025.1703475
2. Lipinska P, Smits K, Van Soom A, Pavani KC, Warzych E. Follicular-fluid extracellular vesicles support energy metabolism of bovine oocytes, improving blastocyst development and quality†. Biol Reprod. 2025 Jul 1;113(1):109–26. doi:10.1093/biolre/ioaf096
3. Pakniyat Z, Azari M, Kafi M, Ghaemi M, Hashemipour SMA, Safaie A, et al. The effect of follicular and ampullary fluid extracellular vesicles on bovine oocyte competence and in vitro fertilization rates. PLOS ONE. 2025 Jun 6;20(6):e0325268. doi:10.1371/journal.pone.0325268
4. Esposito R, Piscopo F, Del Prete C, Kosior MA, Benedetti C, Schreiber M, et al. Extracellular vesicles from the follicular fluid of competent oocytes improve blastocyst yields when supplemented during simulated physiological oocyte maturation in cattle. Theriogenology. 2026 Jan 1;249:117629. doi:10.1016/j.theriogenology.2025.117629
5. Pournourali M, Mizban N, Ehsani R, Ebrahimian S, Nadri T, Azari-Dolatabad N. Extracellular vesicles: key mediators in in vitro embryo production. Front Vet Sci. 2025 Aug 20;12:1641966. doi:10.3389/fvets.2025.1641966 PubMed PMID: 40909937; PubMed Central PMCID: PMC12405430.
6. Zhang Y, Lan M, Chen Y. Minimal Information for Studies of Extracellular Vesicles (MISEV): Ten-Year Evolution (2014–2023). Pharmaceutics. 2024 Oct 29;16(11). doi:10.3390/pharmaceutics16111394
7. Duval C, Wyse BA, Tsang BK, Librach CL. Extracellular vesicles and their content in the context of polycystic ovarian syndrome and endometriosis: a review. J Ovarian Res. 2024 Aug 5;17(1):160. doi:10.1186/s13048-024-01480-7
8. Uzbekova S, Almiñana C, Labas V, Teixeira-Gomes AP, Combes-Soia L, Tsikis G, et al. Protein Cargo of Extracellular Vesicles From Bovine Follicular Fluid and Analysis of Their Origin From Different Ovarian Cells. Front Vet Sci. 2020 Nov 4;7. doi:10.3389/fvets.2020.584948
9. Voros C, Athanasiou D, Mavrogianni D, Varthaliti A, Bananis K, Athanasiou A, et al. Exosomal Communication Between Cumulus–Oocyte Complexes and Granulosa Cells: A New Molecular Axis for Oocyte Competence in Human-Assisted Reproduction. Int J Mol Sci. 2025 Jun 3;26(11). doi:10.3390/ijms26115363
10. Pan K, Ju W, Wang Y, Zhang Q, Wang R, Jiang X, et al. Extracellular vesicles in reproductive medicine: from “animal-led” to “plant-enabled.” Front Cell Dev Biol. 2025 Nov 21;13. doi:10.3389/fcell.2025.1718643
11. Hung WT, Hong X, Christenson LK, McGinnis LK. Extracellular Vesicles from Bovine Follicular Fluid Support Cumulus Expansion1. Biol Reprod. 2015 Nov 1;93(5):117, 1–9. doi:10.1095/biolreprod.115.132977
12. Navakanitworakul R, Hung WT, Gunewardena S, Davis JS, Chotigeat W, Christenson LK. Characterization and Small RNA Content of Extracellular Vesicles in Follicular Fluid of Developing Bovine Antral Follicles. Sci Rep. 2016 May 9;6(1):25486. doi:10.1038/srep25486
13. Hu J, Peng S, Deng W, Guo Z, Wu J, Tan X, et al. EV-derived small non-coding RNAs from porcine follicular fluid regulate follicle development using Pandora sequence. Front Vet Sci. 2026 Mar 17;13. doi:10.3389/fvets.2026.1754433
14. Voros C, Varthaliti A, Athanasiou D, Mavrogianni D, Papahliou AM, Bananis K, et al. The Whisper of the Follicle: A Systematic Review of Micro Ribonucleic Acids as Predictors of Oocyte Quality and In Vitro Fertilization Outcomes. Cells. 2025 May 27;14:787. doi:10.3390/cells14110787
15. Yu L, Wang C, Liu M, Xia L, Liu T, Che Q, et al. Follicular fluid-derived exosomal LncRNA LIPE-AS1 modulates steroid metabolism and survival of granulosa cells leading to oocyte maturation arrest in polycystic ovary syndrome. J Assist Reprod Genet. 2024 May 1;41(5):1387–401. doi:10.1007/s10815-024-03092-y
16. Pérez-García F, Muñoz-Acuña E, Valencia C, Aguila L, Felmer R, Arias ME. Effect of Bovine Follicular Fluid Small Extracellular Vesicles Isolated by Ultracentrifugation and Chromatography on In Vitro Oocyte Maturation and Embryo Development. Int J Mol Sci. 2025 Mar 22;26(7). doi:10.3390/ijms26072880
17. Makieva S, Saenz-de-Juano MD, Almiñana C, Bauersachs S, Bernal-Ulloa S, Xie M, et al. Treatment of human oocytes with extracellular vesicles from follicular fluid during rescue in vitro maturation enhances maturation rates and modulates oocyte proteome and ultrastructure [Internet]. Cell Biology; 2025 [cited 2026 Apr 9]. Available from: http://biorxiv.org/lookup/doi/10.1101/2025.02.05.636623 doi:10.1101/2025.02.05.636623