CN. Ngô Thị Lan Phương, BS. Võ Văn Cường
Đơn vị HTSS IVFMD Family, Bệnh viện Đa khoa Gia Đình Đà Nẵng
Giới thiệu
Trong những năm gần đây, sự gia tăng của các bệnh truyền nhiễm do virus đã đặt ra nhiều thách thức mới đối với sức khỏe sinh sản toàn cầu. Từ những đợt bùng phát của đại dịch COVID-19 do SARS-CoV-2 gây ra, đến các bệnh nhiễm trùng mạn tính như viêm gan B (Hepatitis B) hay HIV (Human immunodeficiency virus), ngày càng có nhiều bằng chứng cho thấy virus không chỉ ảnh hưởng đến sức khỏe mà còn tác động trực tiếp và gián tiếp đến khả năng sinh sản, ảnh hưởng đến kết quả thụ tinh trong ống nghiệm (TTTON) và sự phát triển của thai kỳ giai đoạn sớm.
Ở cả hai giới, nhiễm virus có thể gây rối loạn nội tiết, tổn thương mô sinh dục, suy giảm chất lượng giao tử và thay đổi môi trường miễn dịch – những yếu tố then chốt cho thụ tinh và làm tổ. Trong TTTON, tình trạng nhiễm virus có thể ảnh hưởng đến đáp ứng buồng trứng, chất lượng tinh trùng, sự phát triển phôi và tỷ lệ làm tổ. Đặc biệt, giai đoạn đầu thai kỳ rất nhạy cảm; sự xâm nhập của virus có thể làm tăng nguy cơ sảy thai sớm hoặc để lại di chứng bẩm sinh.
Bài viết này nhằm tổng quan các cơ chế sinh học liên quan đến nhiễm virus và chức năng sinh sản, phân tích tác động của virus đến TTTON và làm rõ những nguy cơ tiềm ẩn trong giai đoạn đầu thai kỳ. Từ đó cung cấp cơ sở khoa học, góp phần định hướng thực hành lâm sàng và chiến lược phòng ngừa nhằm bảo vệ sức khỏe sinh sản trong bối cảnh các bệnh truyền nhiễm do virus ngày càng phức tạp.
Cơ chế tác động của virus lên hệ thống sinh sản
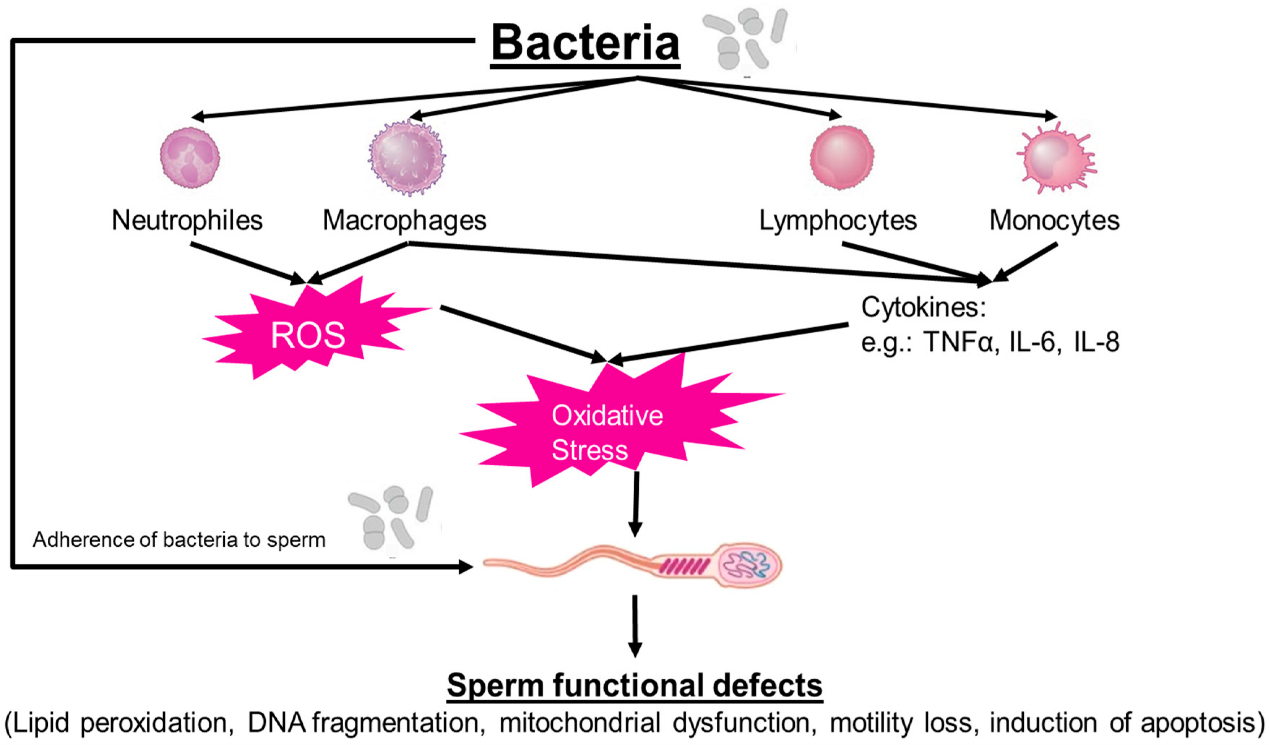
Nhiễm virus có thể tác động lên hệ sinh sản thông qua nhiều cơ chế phức tạp, bao gồm tổn thương mô sinh dục, rối loạn miễn dịch-viêm và mất cân bằng nội tiết. Ở nam giới, nhiều nghiên cứu cho thấy virus có khả năng xâm nhập tinh hoàn, ảnh hưởng đến tế bào Sertoli và Leydig, làm suy giảm quá trình sinh tinh, giảm testosterone và gia tăng stress oxy hóa, từ đó làm tổn thương DNA tinh trùng và giảm chất lượng tinh dịch. Ngoài tổn thương tại chỗ, đáp ứng viêm hệ thống với sự gia tăng các cytokine tiền viêm còn gây rối loạn trục hạ đồi – tuyến yên, làm suy giảm chức năng sinh sản. Ở nữ giới, virus có thể tác động đến buồng trứng và nội mạc tử cung (NMTC), làm thay đổi vi môi trường miễn dịch tại chỗ, ảnh hưởng đến sự phát triển nang noãn, bài tiết progesterone và khả năng tiếp nhận phôi của NMTC. Những cơ chế này không chỉ ảnh hưởng đến khả năng thụ thai tự nhiên mà còn ảnh hưởng kết quả TTTON và quá trình làm tổ ở giai đoạn đầu thai kỳ [1].
- HIV: Virus gây suy giảm miễn dịch ở người
HIV gồm hai loại chính là HIV-1 và HIV-2, là virus RNA thuộc họ retrovirus, trong đó HIV-1 phổ biến toàn cầu và tiến triển nhanh hơn. HIV lây truyền qua quan hệ tình dục, truyền máu và chế phẩm máu, ghép tạng, và lây truyền mẹ con. Nguy cơ lây qua quan hệ tình dục phụ thuộc vào tải lượng virus; trung bình khoảng 0,08% mỗi lần giao hợp khi nam nhiễm HIV và 0,034% khi nữ nhiễm HIV [2]. Lây truyền dọc có tỷ lệ khoảng 15–20%, tăng lên khi bệnh ở mẹ tiến triển nặng [3]. Tỷ lệ tử vong ở trẻ nhiễm HIV theo đường này từng được ghi nhận cao trong những năm đầu đời.
HIV ảnh hưởng đáng kể đến sức khỏe sinh sản. Ở phụ nữ, gần một nửa trường hợp ghi nhận rối loạn kinh nguyệt, có thể liên quan đến suy giảm miễn dịch (giảm CD4), bệnh lý phối hợp (suy thận, suy gan), stress và sụt cân ảnh hưởng đến trục hạ đồi–tuyến yên–buồng trứng. Tình trạng vô kinh, rối loạn chảy máu tử cung bất thường và giảm nồng độ testosterone cũng được ghi nhận [4]. Ngoài ra, HIV và các tình trạng viêm nhiễm kèm theo có thể làm giảm dự trữ buồng trứng và khả năng sinh sản.
Ở nam giới, HIV được phát hiện trong tinh dịch và tế bào sinh tinh, virus xâm nhập vào tế bào CD4 và có thể gắn vào thụ thể GalAAG (galactosylalkacylglycerol) trên màng tinh trùng. Nhiễm HIV và điều trị kháng retrovirus có thể làm suy giảm chất lượng tinh dịch. Bệnh nhân AIDS giai đoạn tiến triển có thể gặp viêm tinh hoàn, thiểu năng sinh dục, thiểu tinh hoặc vô tinh [5].
Trong TTTON, các nghiên cứu so sánh giữa nhóm nhiễm và không nhiễm HIV cho kết quả không đồng nhất: một số nghiên cứu ghi nhận tỷ lệ có thai và tỷ lệ trẻ sinh sống thấp hơn ở bệnh nhân nhiễm HIV, trong khi các nghiên cứu khác không thấy khác biệt hoặc thậm chí ghi nhận kết quả khả quan hơn ở cặp đôi có nam giới nhiễm HIV [6]. Tuy nhiên, dữ liệu gần đây cho thấy xu hướng kết cục kém hơn, đặc biệt ở phụ nữ nhiễm HIV hoặc cả hai vợ chồng đều nhiễm [7]. Cần thêm các nghiên cứu quy mô lớn để làm rõ tác động của HIV đối với kết quả TTTON.
- Virus viêm gan B và C (HBV, HCV)
Virus viêm gan B (HBV) và virus viêm gan C (HCV) là các tác nhân gây bệnh gan mạn tính có khả năng ảnh hưởng đến chức năng sinh sản. HBV thuộc họ Hepadnaviridae, lây truyền chủ yếu qua đường máu, quan hệ tình dục, ghép tạng và từ mẹ sang con; nhiễm HBV có thể liên quan đến chậm thụ thai và rối loạn rụng trứng. HCV thuộc họ Flaviviridae, lây truyền chủ yếu qua tiếp xúc máu, ngoài ra có thể lây truyền dọc, qua quan hệ tình dục và ghép tạng. Nhiễm HCV, đặc biệt ở bệnh nhân xơ gan, có thể gây rối loạn chuyển hóa estrogen và progesterone, làm giảm đáp ứng kích thích buồng trứng và có thể liên quan đến giảm dự trữ buồng trứng [8].
Ở nam giới, HBV có thể tích hợp DNA vào tinh trùng và biểu hiện ở giai đoạn phôi sớm. Nhiễm HBV làm suy giảm chất lượng tinh dịch thông qua rối loạn chức năng ty thể và tăng stress oxy hóa, dẫn đến tăng phân mảnh DNA và apoptosis tinh trùng. Tương tự, HCV cũng làm giảm số lượng, độ di động và hình thái tinh trùng [9].
Bệnh nhân mắc bệnh gan mạn tính (bao gồm HBV/HCV) nhìn chung dung nạp tốt khi thực hiện TTTON, với tỷ lệ làm tổ và tỷ lệ sinh sống không khác biệt đáng kể giữa nhóm có xơ gan, không xơ gan hoặc sau ghép gan. Tuy nhiên, nhóm bệnh nhân này có thể có nguy cơ cao hơn mắc hội chứng quá kích buồng trứng (Ovarian hyperstimulation syndrome-OHSS), do đó cần tư vấn trước mang thai, theo dõi chức năng gan và điều chỉnh điều trị phù hợp trong quá trình TTTON [7].
- HPV (Human papillomavirus)
Ngoài gây tổn thương biểu mô cổ tử cung và ung thư cổ tử cung, HPV còn có thể ảnh hưởng đến biểu mô buồng trứng; mức độ tác động phụ thuộc vào tải lượng virus và tính đặc hiệu mô [5]. Một nghiên cứu đoàn hệ lớn tại Đan Mạch không ghi nhận mối liên quan giữa nhiễm HPV và vô sinh; tuy nhiên, các nghiên cứu gần đây ghi nhận tỷ lệ có thai thấp hơn ở phụ nữ nhiễm HPV [10].
Ở nam giới, HPV được phát hiện trong khoảng 10% trường hợp không triệu chứng. Virus có thể bám vào đầu tinh trùng, ảnh hưởng đến mật độ, hình thái, độ di động và làm tăng phân mảnh DNA tinh trùng; một số trường hợp có thể liên quan đến tinh trùng yếu chưa rõ nguyên nhân. Nhiễm HPV ở nam giới có liên quan đến giảm tỷ lệ thai và tăng nguy cơ sảy thai, kể cả trong TTTON [9].
- SARS-CoV-2
SARS-CoV-2 là một trong những virus RNA có bộ gen lớn nhất, với protein gai đóng vai trò nhận diện thụ thể angiotensin-converting enzyme 2 (ACE2) và thúc đẩy quá trình bám dính – hòa màng tế bào. Quá trình nhiễm virus kích hoạt đáp ứng viêm qua trung gian tế bào T hỗ trợ, interferon-γ, TNF-α và IL-2. Sự xâm nhập tế bào phụ thuộc vào sự hiện diện đồng thời của ACE2 và protease TMPRSS2. Ở nữ, hệ renin–angiotensin–aldosterone và ACE2 tham gia điều hòa sinh nang noãn, sinh steroid, trưởng thành và rụng noãn [1]. Biểu hiện ACE2 tại NMTC tăng trong “cửa sổ làm tổ”, trong khi TMPRSS2/TMPRSS4 tăng dần ở pha chế tiết và mức biểu hiện cao hơn ở phụ nữ lớn tuổi. Tuy nhiên, nhiều nghiên cứu không phát hiện RNA virus trong NMTC, dịch nang noãn hoặc tế bào cumulus ở phụ nữ nhiễm gần thời điểm chọc hút noãn. Bằng chứng lâm sàng hiện tại chưa cho thấy SARS-CoV-2 gây biến chứng lâu dài lên chức năng sinh sản nữ [11].
Ở nam giới, mức độ bệnh có xu hướng nặng hơn, có thể do khác biệt biểu hiện ACE2 và ảnh hưởng của androgen làm tăng TMPRSS2. Các giả thuyết bao gồm rối loạn ACTH–glucocorticoid và giảm angiotensin ảnh hưởng sản xuất testosterone; tuy nhiên, đa số nghiên cứu chưa ghi nhận rối loạn trục hạ đồi–tuyến yên–tinh hoàn rõ rệt. Một số nghiên cứu ghi nhận viêm tinh hoàn và tổn thương tế bào Sertoli; tuy nhiên các ảnh hưởng nếu có thường hồi phục sau một chu kỳ sinh tinh [12].
Những nghiên cứu gần đây cho thấy nhiễm COVID-19 không làm suy giảm dự trữ buồng trứng hay chức năng buồng trứng [13]. Tiền sử nhiễm không triệu chứng hoặc nhẹ ở nữ giới không ảnh hưởng đến kết quả TTTON. Hiện chưa có khuyến cáo rõ ràng về khoảng thời gian tối thiểu cần trì hoãn thực hiện TTTON sau khi mắc COVID-19, đặc biệt ở nam giới. Do đó, quyết định lâm sàng nên dựa trên đánh giá toàn diện về tình trạng nhiễm, mức độ bệnh và các chỉ số sinh sản của từng cặp vợ chồng.
- Virus quai bị
Virus quai bị là virus RNA sợi đơn thuộc họ Paramyxoviridae, có khả năng gây tổn thương đến hệ sinh sản, đặc biệt ở nam giới sau dậy thì. Cơ chế bệnh sinh liên quan đến tổn thương tế bào Leydig và Sertoli, cùng đáp ứng viêm qua trung gian cytokine, dẫn đến giảm sản xuất testosterone và gây chết tế bào mầm. Khoảng 20–30% nam giới mắc quai bị sau dậy thì phát triển viêm tinh hoàn/mào tinh hoàn, trong đó khoảng 15% có thể tiến triển thành teo tinh hoàn hai bên, làm giảm mật độ và độ di động tinh trùng, thậm chí vô tinh [14]. Virus có thể được phát hiện trong tinh dịch đến 14 ngày sau nhiễm.
Ở nữ giới, viêm buồng trứng do quai bị là biến chứng hiếm gặp nhưng có thể dẫn đến tổn thương nhu mô buồng trứng và suy buồng trứng sớm (premature ovarian insufficiency-POI), thậm chí mãn kinh sớm trong một số trường hợp [15]. Do đó, nhiễm quai bị cần được cân nhắc trong chẩn đoán phân biệt các trường hợp POI không rõ nguyên nhân. Tiêm vắc-xin phòng quai bị là biện pháp hiệu quả nhất nhằm bảo vệ chức năng sinh sản lâu dài.
Ngoài các virus kể trên, nhiều virus khác như Cytomegalovirus, Herpes simplex virus, Adenovirus, Zika virus, Rubella virus và Varicella-zoster virus cũng có thể ảnh hưởng đến chức năng sinh sản. Các virus này chủ yếu tác động thông qua cơ chế viêm, stress oxy hóa, tổn thương DNA hoặc ảnh hưởng gián tiếp đến môi trường nội tiết và quá trình làm tổ của phôi. Mặc dù phần lớn bằng chứng hiện nay còn hạn chế và chưa đồng nhất, việc nhận diện và đánh giá nguy cơ nhiễm virus ở các cặp vợ chồng vô sinh có ý nghĩa quan trọng, đặc biệt trước khi thực hiện TTTON.
Sàng lọc trước khi thực hiện thụ tinh trong ống nghiệm
Đối với bệnh nhân đang thực hiện TTTON, việc sàng lọc HIV, HBV, HCV và xác định tình trạng huyết thanh đối với virus rubella được khuyến nghị. Thứ nhất, các bệnh nhiễm virus này có thể không có triệu chứng trong nhiều năm, khiến người mang bệnh không biết mình bị nhiễm. Thứ hai, việc phát hiện các bệnh nhiễm trùng này sẽ thúc đẩy việc điều trị cần thiết để giảm nguy cơ lây truyền cho con cái và bạn tình. Cuối cùng, nhận thức về các bệnh nhiễm trùng tiềm ẩn sẽ thúc đẩy việc thực hiện các biện pháp phòng ngừa, đặc biệt khi xử lý mô và tế bào từ bệnh nhân bị ảnh hưởng. Mẫu thu nhận từ những người nhiễm HIV, HBV hoặc HCV nên được lưu trữ riêng biệt. Ngoài ra, nhiễm trùng rubella nguyên phát trong thai kỳ gây ra những rủi ro đáng kể cho thai nhi, khiến việc tiêm phòng trở nên quan trọng đối với những người thiếu miễn dịch.
Tác động của virus đối với giai đoạn đầu thai kỳ
Nhiễm virus giai đoạn đầu thai kỳ có thể dẫn đến các kết cục bất lợi, bao gồm sảy thai sớm; các nghiên cứu ước tính virus góp phần gây ra khoảng 2,5% trường hợp sảy thai sớm [16]. Cơ chế gây tổn thương phụ thuộc từng loại virus nhưng nhìn chung bao gồm nhiễm trùng lan rộng hoặc nhiễm virus huyết, sau đó xâm nhập mô màng đệm/nhau thai, gây hoại tử biểu mô nhung mao, apoptosis tế bào, ức chế phân bào. Nhóm TORCH-bao gồm Rubella virus, Cytomegalovirus, Herpes simplex virus, Varicella-zoster virus và Parvovirus B19 là các tác nhân thường gặp gây nhiễm trùng bẩm sinh [1].
Với HIV, nguy cơ lây truyền mẹ con khi không can thiệp khoảng 7% và liên quan tải lượng virus, số lượng CD4+. Điều trị kháng retrovirus, mổ lấy thai chủ động và tránh cho con bú giúp giảm nguy cơ xuống <2% [17]. Ở HBV và HCV, dữ liệu cho thấy có thể giảm tỷ lệ làm tổ ở nhóm HbsAg (+), song chưa ghi nhận khác biệt rõ về tỷ lệ thai lâm sàng hay sinh sống; lây truyền mẹ con của HCV trung bình ~8% và tăng theo tải lượng virus/đồng nhiễm [18]. Đối với HPV, được phát hiện trong mô sảy thai và có thể liên quan tăng nguy cơ sảy thai sớm, đặc biệt khi nhiễm ở nam hoặc cả hai vợ chồng.
SARS-CoV-2 có biểu hiện thụ thể ở mô nhau thai, song các nghiên cứu chưa cho thấy tăng nguy cơ sảy thai khi nhiễm 3 tháng đầu thai kỳ. Nhiễm rubella sớm gây nguy cơ lây truyền và dị tật rất cao (~90% nếu nhiễm sớm), giảm đáng kể sau tuần 20 và khoảng 20% nhiễm trong 2 tháng đầu dẫn đến sảy thai [19].
Các virus khác như Coxsackie, Adenovirus và AAV-2 có thể liên quan mất thai sớm qua tổn thương nguyên bào nuôi; Epstein-Barr virus có khả năng tái hoạt ở mô sinh sản; sởi và cúm trong thai kỳ làm tăng nguy cơ biến chứng, dù lây truyền qua nhau thai hiếm [1].
Kết luận
Virus có thể gây ảnh hưởng đáng kể đến khả năng sinh sản và kết quả thai kỳ ở người. Một số bệnh nhiễm virus có liên quan đến vô sinh, sảy thai và các biến chứng trong thai kỳ. Các nghiên cứu trong tương lai cần đi sâu hơn vào việc hiểu rõ cơ chế mà virus ảnh hưởng đến khả năng sinh sản và thai kỳ, cũng như xác định các biện pháp phòng ngừa và chiến lược điều trị tiềm năng. Trong thực hành lâm sàng, cần đặc biệt chú ý đến khả năng nhiễm virus như một nguyên nhân tiềm tàng gây vô sinh và các biến chứng thai kỳ, đảm bảo chẩn đoán, quản lý và hỗ trợ kịp thời cho những bệnh nhân bị ảnh hưởng.
Tài liệu tham khảo
1. Laudański, P., Zyguła, A., Czyżyk, A., Olszak-Wasik, K., Warzecha, D., Wojtyła, C., & Kurzawa, R. (2025). Viral infection and its impact on fertility, medically assisted reproduction and early pregnancy – a narrative review. Reproductive Biology and Endocrinology: RB&E, 23, 68. https://doi.org/10.1186/s12958-025-01392-1
2. Boily, M.-C., Baggaley, R. F., Wang, L., Masse, B., White, R. G., Hayes, R., & Alary, M. (2009). Heterosexual risk of HIV-1 infection per sexual act: A systematic review and meta-analysis of observational studies. The Lancet. Infectious diseases, 9(2), 118–129. https://doi.org/10.1016/S1473-3099(09)70021-0
3. Ochsendorf, F. R. (2008). Sexually transmitted infections: Impact on male fertility. Andrologia, 40(2), 72–75. https://doi.org/10.1111/j.1439-0272.2007.00825.x
4. Cejtin, H. E. (2008). GYNECOLOGIC ISSUES IN THE HIV-INFECTED WOMAN. Infectious disease clinics of North America, 22(4), 709–vii. https://doi.org/10.1016/j.idc.2008.05.006
5. Pellati, D., Mylonakis, I., Bertoloni, G., Fiore, C., Andrisani, A., Ambrosini, G., & Armanini, D. (2008). Genital tract infections and infertility. European Journal of Obstetrics, Gynecology, and Reproductive Biology, 140(1), 3–11. https://doi.org/10.1016/j.ejogrb.2008.03.009
6. Nurudeen, S. K., Grossman, L. C., Bourne, L., Guarnaccia, M. M., Sauer, M. V., & Douglas, N. C. (2013). Reproductive outcomes of HIV seropositive women treated by assisted reproduction. Journal of Women’s Health, 22(3), 243–249. https://doi.org/10.1089/jwh.2012.3855
7. Vianna, C. A., Dupont, C., Selleret, L., Canestri, A., Levy, R., & Hamid, R. H. (2021). Comparison of in vitro fertilization cycles in couples with human immunodeficiency virus type 1 infection versus noninfected couples through a retrospective matched case-control study. F&S Reports, 2(4), 376–385. https://doi.org/10.1016/j.xfre.2021.04.008
8. Englert, Y., Moens, E., Vannin, A.-S., Liesnard, C., Emiliani, S., Delbaere, A., & Devreker, F. (2007). Impaired ovarian stimulation during in vitro fertilization in women who are seropositive for hepatitis C virus and seronegative for human immunodeficiency virus. Fertility and Sterility, 88(3), 607–611. https://doi.org/10.1016/j.fertnstert.2006.11.177
9. Garolla, A., Pizzol, D., Bertoldo, A., Menegazzo, M., Barzon, L., & Foresta, C. (2013). Sperm viral infection and male infertility: Focus on HBV, HCV, HIV, HPV, HSV, HCMV, and AAV. Journal of Reproductive Immunology, 100(1), 20–29. https://doi.org/10.1016/j.jri.2013.03.004
10. Nøhr, B., Kjaer, S. K., Soylu, L., & Jensen, A. (2019). High-risk human papillomavirus infection in female and subsequent risk of infertility: A population-based cohort study. Fertility and Sterility, 111(6), 1236–1242. https://doi.org/10.1016/j.fertnstert.2019.02.001
11. Stanley, K. E., Thomas, E., Leaver, M., & Wells, D. (2020). Coronavirus disease-19 and fertility: Viral host entry protein expression in male and female reproductive tissues. Fertility and Sterility, 114(1), 33–43. https://doi.org/10.1016/j.fertnstert.2020.05.001
12. Patel, D. P., Punjani, N., Guo, J., Alukal, J. P., Li, P. S., & Hotaling, J. M. (2021). The impact of SARS-CoV-2 and COVID-19 on male reproduction and men’s health. Fertility and Sterility, 115(4), 813–823. https://doi.org/10.1016/j.fertnstert.2020.12.033
13. Ata, B., Vermeulen, N., Mocanu, E., Gianaroli, L., Lundin, K., Rautakallio-Hokkanen, S., Tapanainen, J. S., & Veiga, A. (2022). SARS-CoV-2, fertility and assisted reproduction. Human Reproduction Update, 29(2), 177–196. https://doi.org/10.1093/humupd/dmac037
14. Zhang, S., Li, J., Zhou, G., Qin, S., Xin, N., Guo, J., & Xu, Y. (2013). Infertility treatment for azoospermic patients with a history of infectious parotitis (mumps) using combined techniques. Human Fertility, 16(4), 266–268. https://doi.org/10.3109/14647273.2013.840392
15. Ebrahimi, M., & Akbari Asbagh, F. (2011). Pathogenesis and Causes of Premature Ovarian Failure: An Update. International Journal of Fertility & Sterility, 5(2), 54–65.
16. Syridou, G., Skevaki, C., & Kafetzis, D. A. (2005). Intrauterine infection with parvovirus B19 and CMV: Implications in early and late gestation fetal demise. Expert Review of Anti-Infective Therapy, 3(4), 651–661. https://doi.org/10.1586/14787210.3.4.651
17. Agboghoroma, C. O., & Giwa-Osagie, O. F. (2012). Management of infertility in HIV infected couples: A review. African Journal of Reproductive Health, 16(4), 13–20.
18. Wang, L., Li, L., Huang, C., Diao, L., Lian, R., Li, Y., Xiao, S., Hu, X., Mo, M., & Zeng, Y. (2019). Maternal chronic hepatitis B virus infection does not affect pregnancy outcomes in infertile patients receiving first in vitro fertilization treatment. Fertility and Sterility, 112(2), 250-257.e1. https://doi.org/10.1016/j.fertnstert.2019.03.039
19. Pereira, L. (2018). Congenital Viral Infection: Traversing the Uterine-Placental Interface. Annual Review of Virology, 5(1), 273–299. https://doi.org/10.1146/annurev-virology-092917-043236