KS. Nguyễn Thanh Tuyên, ThS. Lê Nhật Quang, BS. Lê Tuấn Quốc Khánh
IVFMD Gia Định - Bệnh viện Đa khoa Gia Định
Mở đầu
Bệnh nhiễm trùng lây truyền qua đường tình dục (sexually transmitted infections – STIs) là một trong những nhóm bệnh lây lan phổ biến nhất trên toàn cầu và có tác động đến sức khỏe sinh sản của cả nam và nữ. Theo báo cáo của Tổ chức Y tế Thế giới (World Health Organization – WHO) năm 2016 và 2018, mỗi ngày có khoảng một triệu ca mắc mới và mỗi năm ghi nhận hơn 376 triệu ca nhiễm mới liên quan đến bốn tác nhân chính bao gồm Chlamydia trachomatis, Neisseria gonorrhoeae, Treponema pallidum và Trichomonas vagis [1].
STIs có thể gây hậu quả nghiêm trọng như viêm vùng chậu (pelvic inflammatory disease – PID), vô sinh do tổn thương/tắc ống dẫn trứng, viêm tinh hoàn – mào tinh, viêm tắc ống dẫn tinh, suy giảm chất lượng tinh trùng, đồng thời làm tăng nguy cơ lây nhiễm HIV [2]. STIs được xem là một trong những nguyên nhân hàng đầu gây vô sinh thứ phát [3]. Đặc biệt, tại các nước đang phát triển, việc quản lý và sàng lọc STIs vẫn còn hạn chế [4].
Hiện nay, vô sinh nam đang là một thách thức y tế toàn cầu, ảnh hưởng đến khoảng 15% các cặp vợ chồng, trong đó yếu tố nam giới đóng góp lên đến khoảng 50% nguyên nhân [2], [5]. Tuy nhiên, bằng chứng về mối liên quan giữa STIs và vô sinh nam vẫn chưa hoàn toàn đồng nhất giữa các tác nhân gây bệnh, cho thấy sự cần thiết của cách tiếp cận tổng hợp dựa trên cơ chế sinh học kết hợp dữ liệu lâm sàng [2], [5]. Do đó, việc hiểu rõ mối liên hệ giữa các tác nhân gây STIs và sức khoẻ sinh sản, đặc biệt là các cơ chế viêm – miễn dịch – nội tiết ở nam giới, có ý nghĩa thiết thực cho việc xây dựng các chiến lược dự phòng và điều trị có hiệu quả.
Tổng quan về STIs
STIs do hơn 30 loại tác nhân khác nhau, bao gồm: vi khuẩn, virus và ký sinh trùng. Con đường lây truyền chủ yếu qua quan hệ tình dục đường âm đạo, hậu môn hoặc miệng [5]. Trong số đó, các tác nhân vi khuẩn thường gặp nhất là Chlamydia trachomatis, Neisseria gonorrhoeae, Mycoplasma và Ureaplasma, có liên quan chặt chẽ đến các biến chứng sinh sản như PID, tắc ống dẫn trứng ở nữ giới và viêm niệu đạo (urethritis), viêm mào tinh hoàn (epididymitis), viêm tuyến tiền liệt (prostatitis), từ đó dẫn đến nguy cơ tắc nghẽn ống dẫn tinh ở nam giới [5].
Nhóm tác nhân virus, bao gồm: herpes simplex virus type 2 (HSV-2), human papillomavirus (HPV) và human immunodeficiency virus (HIV). Các tác nhân này không chỉ gây nhiễm trùng mạn tính mà còn làm gia tăng nguy cơ sảy thai, tổn thương tinh hoàn, rối loạn chức năng sinh tinh và các bệnh lý ác tính của cơ quan sinh dục [2], [5], [6]. Bên cạnh đó, Trichomonas vaginalis là ký sinh trùng phổ biến gây viêm âm đạo và viêm cổ tử cung, có thể ảnh hưởng bất lợi đến môi trường sinh sản và khả năng thụ thai [5].
Đáng lưu ý, phần lớn các STIs diễn tiến không có triệu chứng hoặc biểu hiện không điển hình, dẫn đến việc chẩn đoán muộn, điều trị không đầy đủ và làm gia tăng nguy cơ lây lan cũng như các biến chứng lâu dài đối với sức khỏe sinh sản [2], [5].
Ảnh hưởng đến sức khoẻ sinh sản nam giới
Viêm đường sinh dục nam giới và hệ quả tắc nghẽn
STIs có ảnh hưởng đáng kể đến khả năng sinh sản của nam giới và mối liên quan này đã được WHO ghi nhận chính thức từ năm 2000 [6]. Nhiễm trùng đường sinh dục nam có thể gây tổn thương trực tiếp hoặc gián tiếp đến quá trình sinh tinh và chức năng tinh trùng, thông qua các cơ chế viêm, stress oxy hóa và rối loạn nội tiết, từ đó làm suy giảm chất lượng tinh dịch và khả năng thụ thai [2], [7].
Viêm đường sinh dục nam là một trong những hậu quả thường gặp của STIs, đặc biệt là viêm mào tinh hoàn và viêm tuyến tiền liệt [7]. Viêm mào tinh hoàn do các tác nhân như Chlamydia trachomatis hoặc Neisseria gonorrhoeae có thể tiến triển thành viêm mạn tính, gây xơ hóa và làm tắc nghẽn ống dẫn tinh, từ đó cản trở quá trình di chuyển của tinh trùng [2], [8]. Trong khi đó, viêm tuyến tiền liệt và các tuyến phụ của hệ sinh dục nam có thể làm thay đổi thành phần và môi trường sinh hóa của tinh dịch, ảnh hưởng bất lợi đến khả năng sống, độ di động và chức năng của tinh trùng [2], [8]. Viêm mạn tính không được điều trị triệt để có thể dẫn đến xơ hóa và hình thành sẹo ở các ống dẫn tinh, gây ra vô sinh do tắc nghẽn (obstructive azoospermia), ngay cả khi quá trình sinh tinh tại tinh hoàn vẫn còn hoạt động [2], [5].
Cơ chế miễn dịch – nội tiết
Bên cạnh tổn thương cấu trúc cơ quan sinh dục, STIs còn gây ảnh hưởng nghiêm trọng đến tế bào sinh tinh thông qua các cơ chế viêm và rối loạn nội tiết [7], [8]. Hệ sinh dục nam không chỉ là cơ quan sản xuất, hỗ trợ tinh trùng di chuyển mà còn là một môi trường nội tiết và miễn dịch có tính điều hoà cao. Khi có sự xâm nhập của tác nhân gây bệnh, hệ miễn dịch bẩm sinh sẽ huy động các tế bào thực bào (bạch cầu) đến vị trí nhiễm trùng [2], đồng thời kích hoạt sự giải phóng các cytokine tiền viêm – những phân tử tín hiệu điều biến chuỗi phản ứng sinh học kế tiếp [2], [8].
Nhiễm trùng làm gia tăng bạch cầu và các chất trung gian gây viêm tại đường sinh dục, từ đó can thiệp vào quá trình tổng hợp steroid và sinh tinh [2], [8]. Các nghiên cứu thực nghiệm mô phỏng viêm bằng nội độc tố lipopolysaccharide (LPS) từ vi khuẩn Gram âm cho thấy tình trạng viêm làm giảm đáng kể nồng độ testosterone trong máu [8]. Cơ chế phân tử trung tâm là sự ức chế hoạt động của protein steroidogenic acute regulatory (StAR) bởi các cytokine như TNF-α (tumor necrosis factor-α) và IL-1β (interleukin-1β), làm gián đoạn vận chuyển cholesterol vào ty thể để tổng hợp steroid tại tế bào Leydig [2], [8].
Ngoài ra, IL-1α (interleukin-1α) đóng vai trò quan trọng trong điều hòa động lực học các liên kết giữa tế bào Sertoli và tế bào mầm sinh tinh [8]. Trong trạng thái viêm, IL-1α tăng cao quá mức có thể làm xáo trộn tính toàn vẹn của hàng rào máu – tinh hoàn, làm mất trạng thái “đặc quyền miễn dịch” của ống sinh tinh và tạo điều kiện cho các tế bào miễn dịch tác động trực tiếp lên các tế bào mầm đang phát triển [5], [8]. Hệ quả là tình trạng gián đoạn quá trình sinh tinh, đặc biệt ở giai đoạn tinh bào và tinh tử [8].
Stress oxy hoá và tổn thương cấu trúc tinh trùng
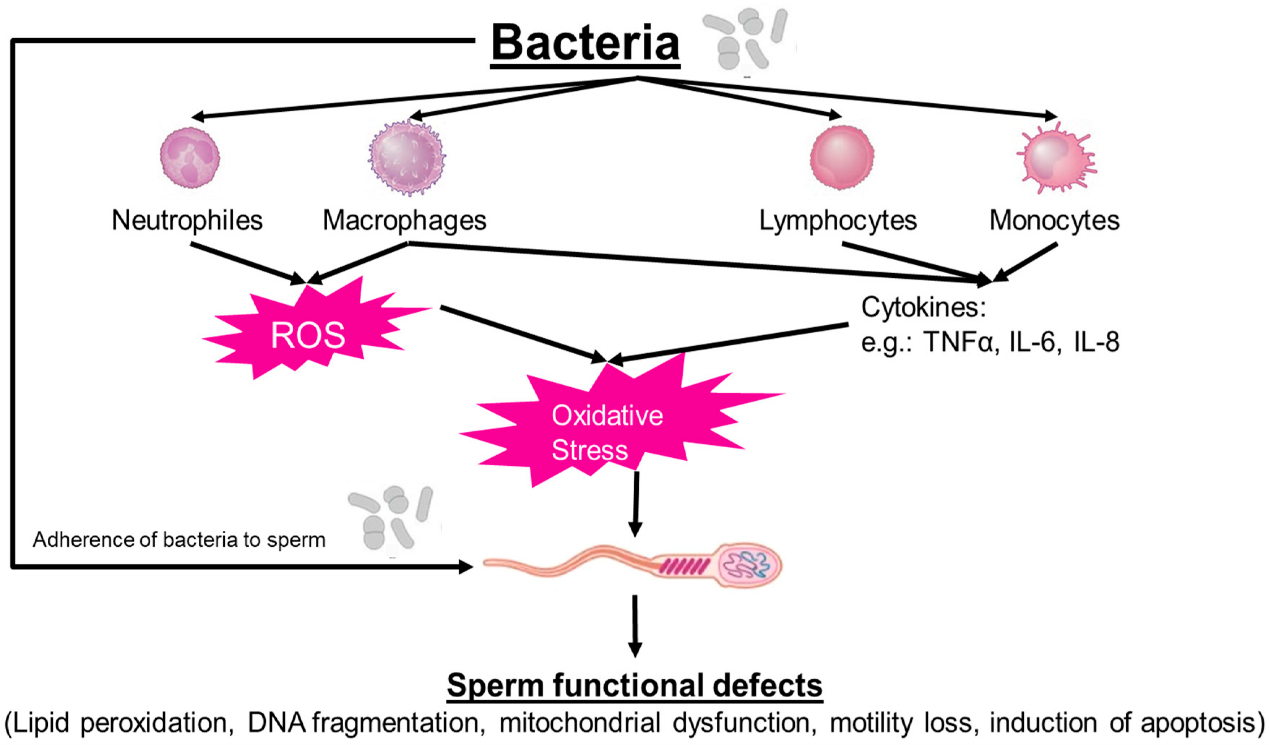
Một trong những cơ chế then chốt liên quan đến mối liên hệ giữa STIs và vô sinh nam là stress oxy hóa [2], [7], [8]. Viêm nhiễm là nguyên nhân trực tiếp dẫn đến mất cân bằng giữa các gốc tự do và hệ thống chống oxy hóa trong tinh dịch, tạo ra trạng thái stress oxy hóa [9]. Quá trình viêm làm gia tăng sản xuất các gốc oxy hóa tự do (reactive oxygen species – ROS) và các cytokine tiền viêm, gây tổn thương màng tinh trùng vốn giàu phospholipid và acid béo không bão hòa đa (PUFAs) [5], [10].
Các thực bào được huy động đến ổ viêm sẽ giải phóng một lượng lớn ROS (như anion superoxide và hydrogen peroxide) nhằm tiêu diệt vi sinh vật; tuy nhiên, do tinh trùng có rất ít tế bào chất – nơi chứa nhiều enzyme chống oxy hoá – nên đặc biệt dễ bị tổn thương bởi ROS [2], [8]. ROS tấn công các acid béo không bão hòa đa trên màng tế bào tinh trùng, gây peroxide hóa lipid, làm giảm tính linh hoạt của màng đuôi, suy giảm khả năng di động và có thể dẫn đến chết tế bào [2], [7], [8].
Không chỉ dừng lại ở tổn thương màng, stress oxy hóa còn là nguyên nhân quan trọng gây đứt gãy DNA (deoxyribonucleic acid) tinh trùng (đứt gãy mạch đơn/mạch kép), làm tăng tỷ lệ phân mảnh DNA tinh trùng (sperm DNA fragmentation – SDF) [2], [5], [7]. Trên lâm sàng, tình trạng tăng bạch cầu trong tinh dịch (leukocytospermia) (nồng độ >1 triệu/mL) thường đi kèm với tỷ lệ SDF cao và suy giảm khả năng thụ tinh [2], [5], [8]. Hệ quả cuối cùng là sự suy giảm toàn diện chất lượng tinh trùng, bao gồm giảm khả năng di động, biến đổi hình thái và tăng SDF [2], [5], [8].
Ảnh hưởng từ điều trị
Ngoài tác động trực tiếp của nhiễm trùng, việc điều trị STIs bằng kháng sinh cũng có thể góp phần làm suy giảm chức năng sinh sản nam giới. Một số kháng sinh được ghi nhận có thể ức chế cạnh tranh các enzyme steroidogenic và ảnh hưởng hormone sinh sản; đồng thời có thể gây suy giảm chức năng tế bào sinh tinh, tế bào Sertoli và làm gián đoạn hàng rào máu – tinh hoàn, khiến chất lượng tinh dịch có thể tiếp tục bị ảnh hưởng ngay cả sau khi nhiễm trùng đã được kiểm soát [2].
Bằng chứng khoa học và hệ quả lâm sàng của STIs
Nhiều nghiên cứu gần đây đã cung cấp bằng chứng cho thấy STIs có liên quan đến sự suy giảm khả năng sinh sản, đặc biệt ở nam giới. Trong số các tác nhân virus, HSV-2 được quan tâm do đặc tính nhiễm trùng mạn tính và khả năng tái hoạt động kéo dài [6], [11]. Các nghiên cứu huyết thanh học ghi nhận tỷ lệ dương tính HSV-2 cao hơn rõ rệt ở nhóm nam giới vô sinh hoặc có bất thường tinh dịch đồ so với nhóm chứng [6].
Đáng chú ý, HSV-2 có thể xâm nhập vào tế bào mầm và liên quan đến thiểu tinh cũng như giảm khả năng di động; trong khi HPV có thể được phát hiện ở tinh trùng và liên quan đến giảm di động tiến tới cũng như gia tăng bất thường hình thái [5], [6]. Sự hiện diện của vi khuẩn trong tinh dịch cũng được chứng minh là yếu tố ảnh hưởng bất lợi đến kết quả sinh sản, đặc biệt trong bối cảnh hỗ trợ sinh sản. Nghiên cứu hồi cứu của Babandi và cộng sự (2023) phân tích trên 242 chu kỳ thụ tinh trong ống nghiệm – chuyển phôi tươi cho thấy nhóm nuôi cấy tinh dịch dương tính có tỷ lệ thụ tinh và phôi chất lượng tốt thấp hơn có ý nghĩa thống kê so với nhóm âm tính, đồng thời tỷ lệ thai lâm sàng cũng giảm đáng kể (p = 0,033) [3]. Theo nghiên cứu của Garolla và cộng sự (2024) trong các chu kỳ hỗ trợ sinh sản, nam giới nhiễm HPV có tỷ lệ thai lâm sàng và trẻ sinh sống thấp hơn, đồng thời nguy cơ sảy thai sớm tăng gấp khoảng hai lần so với nhóm không nhiễm [12].
Ngoài ảnh hưởng trực tiếp lên tinh trùng, vi khuẩn tinh dịch (ví dụ: Staphylococcus aureus) còn có thể gây nhiễm môi trường nuôi cấy, làm phôi thoái hóa và thất bại điều trị [3], [13]. Đáng lưu ý, việc sử dụng tinh trùng có DNA bị tổn thương trong kỹ thuật tiêm tinh trùng vào bào tương noãn (intracytoplasmic sperm injection – ICSI) có thể liên quan đến phôi chất lượng kém và tăng nguy cơ sảy thai sớm; đồng thời đặt ra những quan ngại về hệ quả tiềm tàng cho thế hệ sau [2], [5], [8].
Mặc dù nhiều cơ chế sinh học ủng hộ mối liên quan STIs và vô sinh nam, các tổng quan hệ thống cho thấy các bằng chứng hiện nay vẫn còn mâu thuẫn giữa các tác nhân và giữa các nghiên cứu (khác biệt thiết kế, tiêu chí chẩn đoán, kỹ thuật xét nghiệm và đặc điểm quần thể), nhấn mạnh nhu cầu thực hiện các nghiên cứu tiến cứu, đa trung tâm và được chuẩn hóa nhằm xác định rõ mối quan hệ nhân quả [5].
Chẩn đoán, điều trị và phòng ngừa
Trong bối cảnh nhiều STIs diễn tiến không triệu chứng, việc đánh giá tình trạng viêm và nhiễm khuẩn đường sinh dục nam cần dựa trên thăm khám lâm sàng kết hợp với xét nghiệm [5], [7], [11]. Về thăm khám lâm sàng, STIs ở nam giới có thể biểu hiện bằng các triệu chứng viêm đường tiết niệu dưới như tiểu gắt, tiểu buốt, tiểu mủ hoặc tiểu máu; kèm theo tiết dịch niệu đạo, sưng đỏ hoặc loét dương vật, đau tinh hoàn hay mào tinh hoàn [14]. Tuy nhiên, trong nhiều trường hợp khác nhau, đặc biệt trong nhiễm Chlamydia trachomatis hoặc HPV – diễn tiến không triệu chứng, khiến bệnh dễ bị bỏ sót nếu không được sàng lọc chủ động. Các xét nghiệm thường dùng bao gồm đánh giá bạch cầu trong tinh dịch, nhuộm Gram và nuôi cấy vi khuẩn [3]. Sự hiện diện của leukocytospermia và kháng thể kháng tinh trùng (antisperm antibodies – ASA) có thể gợi ý tình trạng viêm mạn tính và rối loạn hàng rào máu – tinh hoàn [2], [3], [5], [8]. Bên cạnh đó, các xét nghiệm phát hiện tác nhân gây bệnh bằng sinh học phân tử ngày càng được ứng dụng rộng rãi, đặc biệt là kỹ thuật khuếch đại acid nucleic (Nucleic Acid Amplification Test – NAAT) nhằm phát hiện DNA/RNA của vi khuẩn hoặc virus trong nước tiểu hoặc dịch niệu đạo [14]. Các panel xét nghiệm đa tác nhân (ví dụ: xét nghiệm 13 STDs) cho phép sàng lọc đồng thời nhiều mầm bệnh như Chlamydia trachomatis, Neisseria gonorrhoeae, Mycoplasma genitalium, Ureaplasma spp., Trichomonas vaginalis, HSV, HPV,… giúp nâng cao độ nhạy và rút ngắn thời gian chẩn đoán [15]. Ngoài ra, xét nghiệm huyết thanh học nhằm tầm soát các bệnh lây truyền qua đường máu như HIV, giang mai, viêm gan B và C cũng cần được thực hiện để đánh giá toàn diện người bệnh [16]. Do tính chất trên, các dấu ấn sinh học viêm trong tinh dịch như IL-6, IL-8, TNF-α được đề xuất như những chỉ dấu tiềm năng giúp dự báo rối loạn sinh sản liên quan viêm [5], [8]. Ví dụ, nồng độ IL-6 cao thường thấy ở nam giới thiểu tinh, trong khi TNF-α cao liên quan đến tình trạng không có tinh trùng do viêm [5], [8].
Việc điều trị STIs cần tuân thủ nghiêm ngặt các phác đồ chuẩn được khuyến cáo, nhằm đảm bảo hiệu quả điều trị và hạn chế nguy cơ kháng thuốc [5], [17]. Một nguyên tắc quan trọng trong quản lý STIs là điều trị đồng thời cho cả bạn tình, ngay cả khi người này không có triệu chứng lâm sàng, nhằm tránh tình trạng tái nhiễm và lây nhiễm chéo[11], [17]. Bên cạnh kháng sinh (khi có chỉ định), các biện pháp hỗ trợ như bổ sung chất chống oxy hóa (ví dụ kẽm, selen, vitamin C, vitamin E) được đề xuất như một hướng tiếp cận nhằm giảm stress oxy hóa và cải thiện một số chỉ số chức năng tinh trùng trong bối cảnh viêm [2], [8]. Bên cạnh đó, người bệnh cần được theo dõi đáp ứng điều trị và các biến chứng có thể xảy ra, đặc biệt trong các trường hợp nhiễm trùng kéo dài hoặc tái phát, để kịp thời điều chỉnh phác đồ và giảm thiểu tác động tiêu cực đến chức năng sinh sản [5], [17].
Song song với sàng lọc và điều trị, giáo dục hành vi tình dục an toàn là một trong những biện pháp phòng ngừa bền vững và hiệu quả nhất đối với STIs [11]. Việc sử dụng bao cao su đúng cách và thường xuyên trong quan hệ tình dục đã được chứng minh là làm giảm đáng kể nguy cơ lây truyền nhiều tác nhân STIs [11]. Duy trì mối quan hệ tình dục chung thủy với một bạn tình, tránh quan hệ với nhiều bạn tình hoặc quan hệ tình dục không an toàn là biện pháp then chốt giúp giảm nguy cơ nhiễm mới và tái nhiễm. Ngoài ra, tư vấn sức khỏe sinh sản trước kết hôn và trước khi mang thai giúp các cặp đôi nâng cao nhận thức, chủ động sàng lọc STIs và chuẩn bị tốt hơn cho thai kỳ an toàn, từ đó góp phần bảo vệ sức khỏe sinh sản của cá nhân và cộng đồng [5], [17]. Tiêm chủng (đặc biệt vắc-xin HPV) được xem là chiến lược dự phòng hiệu quả nhằm giảm các bệnh lý liên quan HPV và gián tiếp góp phần bảo vệ sức khỏe sinh sản [5], [11].
Kết luận
STIs và viêm nhiễm đường sinh dục nam giới là những quá trình bệnh lý phức tạp, tác động từ mức phân tử (cytokine, StAR, testosterone), mức tế bào (apoptosis, tổn thương màng tinh trùng, phân mảnh DNA) đến hệ quả lâm sàng (giảm chất lượng tinh dịch, vô sinh do tắc nghẽn) và ảnh hưởng lên kết quả hỗ trợ sinh sản (IVF/ICSI) [2], [3], [5], [8]. Vì vậy, chiến lược kiểm soát STIs cần nhấn mạnh phát hiện sớm và sàng lọc định kỳ cho các nhóm nguy cơ theo khuyến cáo của các tổ chức y tế lớn như Trung tâm phòng chống dịch bệnh Hoa Kỳ (Centers for Disease Control – CDC) và WHO, kết hợp điều trị theo phác đồ phù hợp, quản lý bạn tình và can thiệp giảm stress oxy hóa khi có chỉ định, nhằm bảo tồn và phục hồi khả năng sinh sản nam giới [2], [5], [8], [17].
Tài liệu tham khảo
[1] L. Newman et al., “Global Estimates of the Prevalence and Incidence of Four Curable Sexually Transmitted Infections in 2012 Based on Systematic Review and Global Reporting,” PLoS One, vol. 10, no. 12, p. e0143304, Dec. 2015, doi: 10.1371/journal.pone.0143304.
[2] A. Azenabor, A. O. Ekun, and O. Akinloye, “Impact of Inflammation on Male Reproductive Tract.,” J. Reprod. Infertil., vol. 16, no. 3, pp. 123–9, 2015.
[3] R. M. Babandi, R. S. Ibraheem, R. M. Garba, I. M. Liman, A. Ismail-Are, and Y. Samuel, “Does seminal fluid bacterial isolate(s) affect in vitro fertilization — embryo transfer outcome?,” Middle East Fertil. Soc. J., vol. 28, no. 1, p. 8, Apr. 2023, doi: 10.1186/s43043-023-00132-y.
[4] D. G. Tsevat, H. C. Wiesenfeld, C. Parks, and J. F. Peipert, “Sexually transmitted diseases and infertility,” Am. J. Obstet. Gynecol., vol. 216, no. 1, pp. 1–9, Jan. 2017, doi: 10.1016/j.ajog.2016.08.008.
[5] K. Khalafalla et al., “Are sexually transmitted infections associated with male infertility? A systematic review and in-depth evaluation of the evidence and mechanisms of action of 11 pathogens,” Arab J. Urol., vol. 21, no. 4, pp. 216–232, Oct. 2023, doi: 10.1080/2090598X.2023.2218566.
[6] M. J. Mahmodi, S. Shatizadeh Malekshahi, and H. Soltanghoraee, “Seroprevalence of HSV-2 in multiple subgroups of infertile men with abnormal sperm parameters and those seeking sex selection: a case-control study,” BMC Infect. Dis., vol. 25, no. 1, p. 14, Jan. 2025, doi: 10.1186/s12879-024-10421-0.
[7] H. Oghbaei et al., “Effects of bacteria on male fertility: Spermatogenesis and sperm function,” Life Sci., vol. 256, p. 117891, Sep. 2020, doi: 10.1016/j.lfs.2020.117891.
[8] A. Agarwal, “Impact of inflammation on male fertility,” Frontiers in Bioscience, vol. E3, no. 1, p. 223, 2011, doi: 10.2741/e223.
[9] K. Tremellen, “Oxidative stress and male infertility—a clinical perspective,” Hum. Reprod. Update, vol. 14, no. 3, pp. 243–258, May 2008, doi: 10.1093/humupd/dmn004.
[10] A. Agarwal, G. Virk, C. Ong, and S. S. du Plessis, “Effect of Oxidative Stress on Male Reproduction,” World J. Mens Health, vol. 32, no. 1, p. 1, 2014, doi: 10.5534/wjmh.2014.32.1.1.
[11] L. Carmine, M. Castillo, and M. Fisher, “Testing and Treatment for Sexually Transmitted Infections in Adolescents—What’s New?,” J. Pediatr. Adolesc. Gynecol., vol. 27, no. 2, pp. 50–60, Apr. 2014, doi: 10.1016/j.jpag.2013.06.005.
[12] A. Garolla et al., “Papillomavirus infection and male infertility: A systematic review and meta‐analysis,” Health Sci. Rep., vol. 7, no. 9, Sep. 2024, doi: 10.1002/hsr2.70048.
[13] E. Moretti et al., “The presence of bacteria species in semen and sperm quality,” J. Assist. Reprod. Genet., vol. 26, no. 1, pp. 47–56, Jan. 2009, doi: 10.1007/s10815-008-9283-5.
[14] K. A. Workowski et al., “Sexually Transmitted Infections Treatment Guidelines, 2021,” MMWR. Recommendations and Reports, vol. 70, no. 4, pp. 1–187, Jul. 2021, doi: 10.15585/mmwr.rr7004a1.
[15] B. Van Der Pol, “Clinical and Laboratory Testing for Trichomonas vaginalis Infection,” J. Clin. Microbiol., vol. 54, no. 1, pp. 7–12, Jan. 2016, doi: 10.1128/JCM.02025-15.
[16] B. Bernard M. et al., “Laboratory testing for the diagnosis of HIV infection : updated recommendations,” Atlanta, GA, Jun. 2014. doi: 10.15620/cdc.23447.
[17] J. Rowley et al., “Chlamydia, gonorrhoea, trichomoniasis and syphilis: global prevalence and incidence estimates, 2016,” Bull. World Health Organ., vol. 97, no. 8, pp. 548-562P, Aug. 2019, doi: 10.2471/BLT.18.228486.