CVPH. Ngô Thị Lan Phương
Đơn vị HTSS IVFMD Family, Bệnh viện Đa khoa Gia Đình Đà Nẵng
-
Giới thiệu
Ống dẫn trứng là cơ quan quan trọng trong sinh sản nữ, đảm nhiệm vận chuyển giao tử và phôi, đồng thời tạo môi trường thuận lợi cho thụ tinh và phát triển phôi sớm [1]. Cơ quan này có đặc điểm miễn dịch riêng và tham gia các cơ chế như hóa hướng động và nhiệt hướng động để hỗ trợ sự gặp gỡ giữa tinh trùng và noãn.
Ống dẫn trứng chịu sự điều hòa bởi các biến đổi nội tiết, ảnh hưởng trực tiếp đến hoạt động co bóp của cơ trơn và tính chất dịch trong lòng ống. Nhờ hệ thống cấp máu từ cả động mạch tử cung và buồng trứng, cơ quan này có khả năng đáp ứng sớm với những thay đổi hormone theo chu kỳ kinh nguyệt, từ đó điều chỉnh môi trường vi mô nhằm đảm bảo quá trình vận chuyển giao tử và phôi diễn ra đồng bộ với sự chuẩn bị của nội mạc tử cung [2].
Các hormone steroid buồng trứng, đặc biệt là estradiol (E2) và progesterone (P4), đóng vai trò trung tâm trong việc điều hòa cấu trúc và chức năng biểu mô ống dẫn trứng. E2 thúc đẩy sự phát triển và hoạt động của tế bào có lông mao, làm tăng tần số đập lông mao, tăng co bóp cơ trơn và giảm độ nhớt dịch, qua đó tạo điều kiện thuận lợi cho sự di chuyển của tinh trùng và noãn tới vị trí thụ tinh. Ngược lại, P4 có xu hướng ức chế các quá trình này, làm giảm hoạt động lông mao và co bóp, đồng thời tăng độ nhớt dịch trong lòng ống [3].
Sự mất cân bằng nội tiết do các yếu tố nội sinh hoặc ngoại sinh có thể dẫn đến biến đổi cấu trúc và chức năng ống dẫn trứng, bao gồm các bất thường tế bào học và suy giảm khả năng vận chuyển giao tử/phôi. Những thay đổi này có liên quan đến tăng nguy cơ vô sinh và thai ngoài tử cung, nhấn mạnh tầm quan trọng của việc kiểm soát các yếu tố ảnh hưởng đến môi trường nội tiết đối với sức khỏe sinh sản nữ.
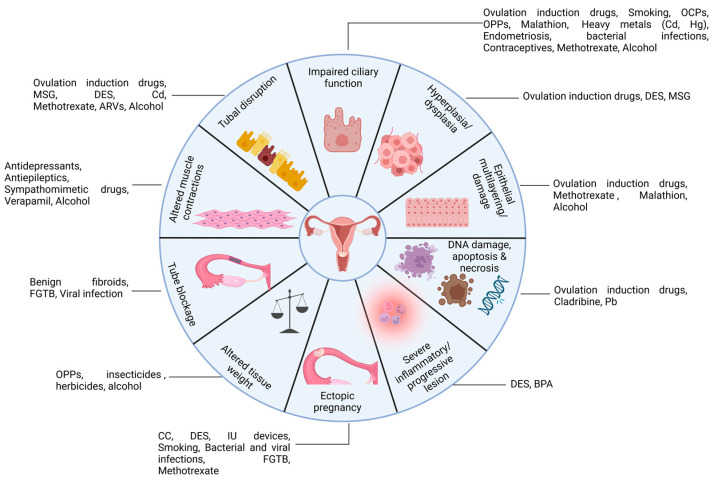
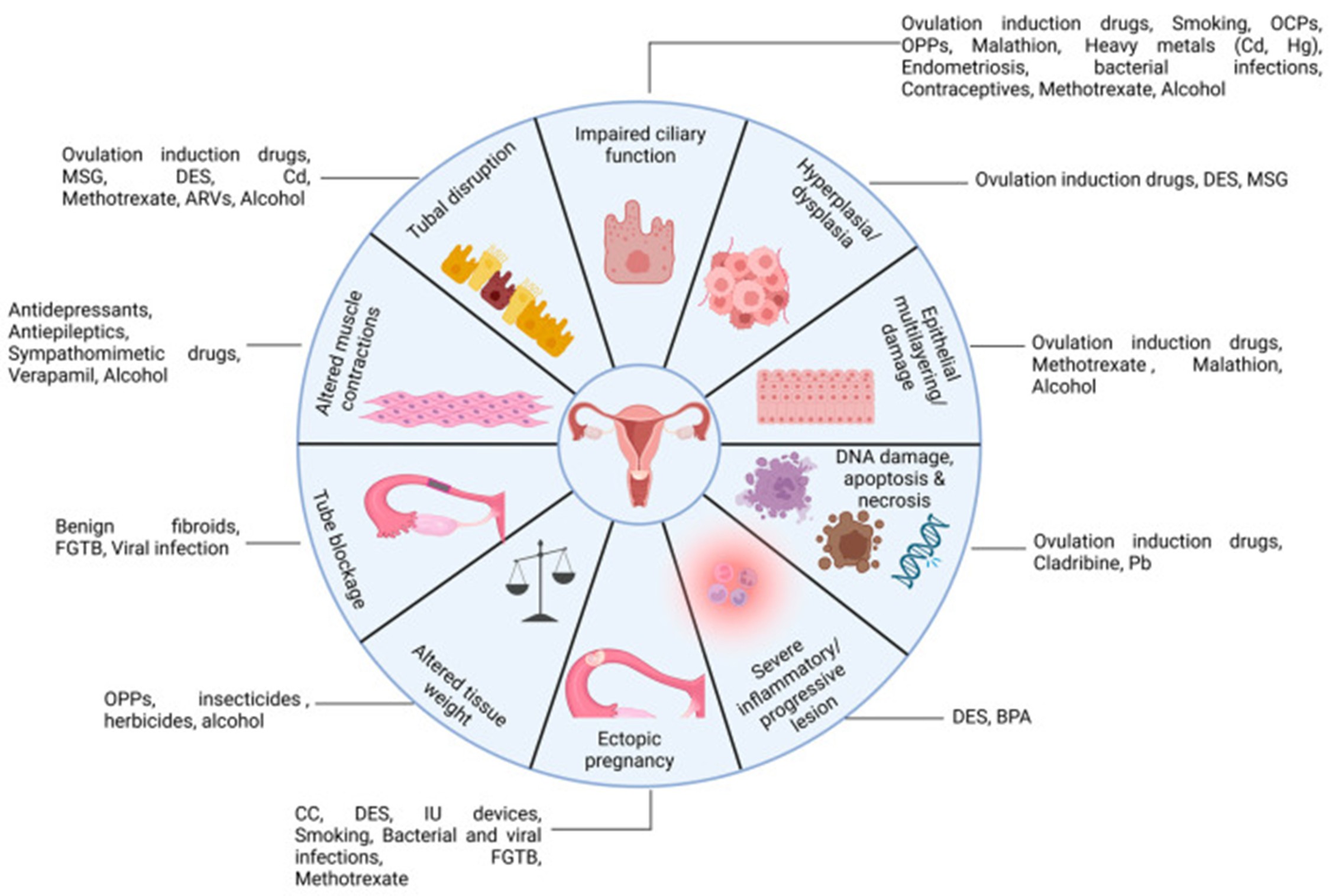
Hình 1. Hình minh họa các yếu tố nguy cơ tiểm ẩn ảnh hưởng đến cấu trúc và chức năng của ống dẫn trứng [4].
-
Các yếu tố ảnh hưởng ống dẫn trứng
-
Các chất độc hại trong môi trường
-
-
Thuốc trừ sâu, thuốc diệt côn trùng và thuốc diệt cỏ
Tiếp xúc với thuốc trừ sâu là một vấn đề sức khỏe toàn cầu đáng lo ngại, với khoảng 32% dân số thế giới sử dụng vượt mức an toàn và khoảng 3 triệu ca ngộ độc mỗi năm, trong đó hơn 10% dẫn đến tử vong [5]. Mặc dù bằng chứng trực tiếp về tác động của thuốc trừ sâu lên ống dẫn trứng ở người còn hạn chế, các dữ liệu gián tiếp cho thấy những ảnh hưởng bất lợi đáng kể đối với chức năng sinh sản.
Các nghiên cứu dịch tễ học ghi nhận rằng người làm việc trong lĩnh vực nông nghiệp có nguy cơ rối loạn ống dẫn trứng cao hơn 4–16 lần và gia tăng tỷ lệ vô sinh so với nhóm nghề khác [6]. Ngoài ra, nghiên cứu đoàn hệ quy mô lớn tại Hoa Kỳ cũng cho thấy nguy cơ tăng các khối u buồng trứng và ống dẫn trứng ở vợ/chồng của người tiếp xúc với thuốc trừ sâu, có thể liên quan đến nhiều yếu tố nguy cơ trong môi trường nông nghiệp như hóa chất, khí thải và tác nhân sinh học [7]. Những bằng chứng này nhấn mạnh tác hại của thuốc trừ sâu trong việc làm suy giảm chức năng ống dẫn trứng và sức khỏe sinh sản.
-
Chất hóa học gây rối loạn nội tiết
Các chất gây rối loạn nội tiết (endocrine-disrupting chemicals – EDCs) là nhóm tác nhân ngoại sinh có khả năng can thiệp vào hoạt động bình thường của hệ nội tiết thông qua việc bắt chước, đối kháng hoặc làm thay đổi quá trình tổng hợp, vận chuyển và chuyển hóa hormone [8]. Những tác động này có thể gây rối loạn cân bằng nội tiết, từ đó ảnh hưởng sâu rộng đến chức năng sinh sản và phát triển.
Tác động của EDCs đặc biệt nghiêm trọng tại các quốc gia có thu nhập thấp và trung bình, nơi mức độ phơi nhiễm cao hơn do điều kiện môi trường và kiểm soát hóa chất còn hạn chế. Ước tính trong hai thập kỷ qua, phơi nhiễm với các chất này có liên quan đến hơn 400.000 trường hợp trẻ sơ sinh nhẹ cân, phản ánh ảnh hưởng đáng kể của EDCs lên sức khỏe bà mẹ và trẻ em [9].
Đáng chú ý, các bằng chứng dịch tễ học ở người cho thấy phơi nhiễm với diethylstilbestrol (DES) trong thai kỳ có thể gây ra những biến đổi lâu dài và mang tính liên thế hệ. Cụ thể, con gái của những phụ nữ sử dụng DES trong thời gian mang thai có nguy cơ xuất hiện các bất thường cả về cấu trúc và chức năng của ống dẫn trứng, bao gồm thay đổi hình thái và suy giảm chức năng vận chuyển [10]. Điều này nhấn mạnh khả năng tác động qua nhau thai của EDCs và vai trò của giai đoạn bào thai như một “cửa sổ nhạy cảm”, nơi các rối loạn nội tiết có thể để lại hậu quả lâu dài đối với sức khỏe sinh sản trong suốt cuộc đời.
-
-
Ảnh hưởng của lối sống
-
-
Caffeine/ thuốc lá/ rượu
Caffeine, thuốc lá và rượu là các yếu tố phổ biến có thể ảnh hưởng tiêu cực đến chức năng ống dẫn trứng và khả năng sinh sản. Caffeine có thể làm giảm hoạt động co bóp của ống dẫn trứng, trong khi hút thuốc gây rối loạn tái tạo biểu mô và làm tăng nguy cơ mang thai ngoài tử cung [11]. Bên cạnh đó, rượu làm suy giảm chức năng buồng trứng và giảm hoạt động co bóp ống dẫn trứng thông qua con đường nitric oxide [12]. Những yếu tố này có thể làm gián đoạn vận chuyển giao tử và phôi, từ đó làm giảm khả năng sinh sản ở nữ giới.
-
-
Nhiễm trùng
-
Nhiễm trùng do vi khuẩn và virus là yếu tố quan trọng gây tổn hại cấu trúc và chức năng ống dẫn trứng, từ đó ảnh hưởng đến khả năng sinh sản nữ. Các tình trạng như nhiễm trùng sau sảy thai, hậu sản hoặc liên quan đến dụng cụ tử cung đều có thể gây tổn thương ống dẫn trứng. Các tác nhân như Chlamydia trachomatis và Neisseria gonorrhoeae làm giảm hoạt động lông mao, co bóp và tăng nguy cơ mang thai ngoài tử cung [13], trong khi một số virus (cytomegalovirus (CMV) và virus herpes simplex (HSV)) kích hoạt phản ứng viêm và thụ thể miễn dịch gây tổn thương mô [14].
Đặc biệt, lao sinh dục nữ (Female genital tuberculosis-FGTB) là nguyên nhân hàng đầu gây tắc ống dẫn trứng và vô sinh ở các nước đang phát triển. Bệnh gây ra các biến đổi nghiêm trọng như tắc nghẽn, dính, ứ dịch và biến dạng hình thái ống dẫn trứng, dẫn đến giảm khả năng thụ thai và tăng nguy cơ mang thai ngoài tử cung [15].
-
-
Các tác nhân dược lý
-
-
Thuốc chống trầm cảm và thuốc chống động kinh
Việc sử dụng thuốc chống trầm cảm, đặc biệt ở phụ nữ bị trầm cảm hoặc lo âu, có liên quan đến giảm khả năng sinh sản và khả năng thụ thai. Các nghiên cứu chỉ ra rằng nhóm thuốc SSRI (selective serotonin reuptake inhibitor) như escitalopram và paroxetine có thể làm tăng các cơn co thắt tự phát của ống dẫn trứng, gây rối loạn quá trình vận chuyển giao tử và phôi [16]. Sự tăng co bóp này có thể dẫn đến vận chuyển tinh trùng sớm hoặc giữ lại trứng đã thụ tinh, góp phần gây vô sinh [17].
Ngoài ra, một số thuốc khác như carbamazepine và lamotrigine được ghi nhận làm giảm co thắt ống dẫn trứng theo cách phụ thuộc liều, cho thấy thuốc có thể ảnh hưởng đáng kể đến chức năng sinh lý của ống dẫn trứng [18].
-
Thuốc kích thích hệ thần kinh giao cảm
Thuốc kích thích hệ thần kinh giao cảm ảnh hưởng đến chức năng ống dẫn trứng thông qua hoạt hóa các thụ thể adrenergic. Kích thích thụ thể alpha (ví dụ adrenaline) làm tăng co bóp ống dẫn trứng, trong khi chất chủ vận beta (như isoprenaline) gây giãn cơ; norepinephrine có thể tác động lên cả hai loại thụ thể này. Sự thay đổi hoạt động co bóp này có thể ảnh hưởng đến quá trình vận chuyển giao tử và phôi [4].
Ngoài ra, kích thích adrenergic kéo dài, đặc biệt bởi norepinephrine, có thể liên quan đến cơ chế sinh ung thư. Các nghiên cứu cho thấy tiếp xúc lâu dài với norepinephrine làm tăng khả năng tăng sinh và hình thành khuẩn lạc của tế bào biểu mô ống dẫn trứng, gợi ý vai trò tiềm tàng trong sự khởi phát và tiến triển của ung thư buồng trứng [19].
-
Thuốc tránh thai
Các biện pháp tránh thai nội tiết, đặc biệt là levonorgestrel (LNG), có thể ảnh hưởng đến chức năng ống dẫn trứng thông qua việc làm giảm tần số chuyển động lông mao (ciliary beat frequency-CBF), từ đó tác động đến quá trình vận chuyển giao tử và phôi [13]. Nghiên cứu dịch tễ học cho thấy nguy cơ mang thai ngoài tử cung cao hơn ở những phụ nữ sử dụng dụng cụ tử cung chứa LNG so với các phương pháp tránh thai nội tiết khác, và các trường hợp mang thai hiếm gặp khi dùng IUD (intrauterine devices) thường là thai ngoài tử cung [20].
Ngoài ra, các thuốc tránh thai khẩn cấp khác như mifepristone và ulipristal acetate cũng được ghi nhận có khả năng ức chế hoạt động lông mao và co bóp cơ trơn ống dẫn trứng, có thể thông qua tác động lên thụ thể progesterone [21]. Những ảnh hưởng này cho thấy các biện pháp tránh thai nội tiết có thể làm thay đổi chức năng sinh lý của ống dẫn trứng.
-
Thuốc kích thích rụng trứng
Kích thích rụng trứng là phương pháp phổ biến trong điều trị vô sinh, sử dụng các thuốc như clomiphene citrate, letrozole và gonadotropin nhằm điều chỉnh hoạt động của trục hạ đồi–tuyến yên–buồng trứng. Những can thiệp này làm thay đổi đáng kể nồng độ hormone, từ đó ảnh hưởng đến các cơ quan nhạy cảm với nội tiết như ống dẫn trứng. Cụ thể, các chất điều biến thụ thể estrogen chọn lọc (selective estrogen receptor modulators-SERM) như clomiphene citrate hoặc tamoxifen làm tăng nồng độ estrogen, trong khi letrozole – một chất ức chế aromatase – lại làm giảm estrogen huyết thanh bằng cách ngăn cản chuyển đổi androgen thành estrogen. Những thay đổi nội tiết này có thể tác động đến chức năng sinh lý của ống dẫn trứng trong quá trình điều trị vô sinh [4].
-
Chỉ định lâm sàng
Rối loạn chức năng ống dẫn trứng có ý nghĩa lâm sàng quan trọng trong đánh giá và điều trị vô sinh, đặc biệt trong bối cảnh hỗ trợ sinh sản. Nhiều nghiên cứu đã chứng minh rằng các bệnh lý ống dẫn trứng như hydrosalpinx làm giảm đáng kể tỷ lệ thành công của IVF/ICSI, bao gồm giảm tỷ lệ làm tổ, tỷ lệ có thai và tăng nguy cơ sảy thai sớm [22]. Can thiệp ngoại khoa như cắt hoặc tắc ống dẫn trứng trước IVF có thể cải thiện đáng kể kết quả điều trị, bao gồm tăng tỷ lệ có thai lâm sàng và trẻ sinh sống [23].
Trong thực hành lâm sàng, đánh giá tình trạng ống dẫn trứng là bước quan trọng trong tiếp cận vô sinh. Các phương pháp như chụp tử cung–vòi trứng (Hysterosalpingography-HSG), siêu âm và nội soi ổ bụng giúp xác định độ thông và chức năng của ống dẫn trứng. Đặc biệt, HSG không chỉ có giá trị chẩn đoán mà còn có thể liên quan đến tiên lượng khả năng mang thai, khi độ thông của ống dẫn trứng tương quan chặt chẽ với tỷ lệ có thai tự nhiên [24].
Về tiên lượng, tình trạng bệnh lý của ống dẫn trứng (như tắc nghẽn, hydrosalpinx hoặc tổn thương cấu trúc) là yếu tố dự báo quan trọng đối với khả năng sinh sản. Phụ nữ có tổn thương ống dẫn trứng thường có tỷ lệ mang thai tự nhiên thấp hơn và nguy cơ thai ngoài tử cung cao hơn. Do đó, việc phát hiện sớm và xử trí phù hợp các bất thường ống dẫn trứng có ý nghĩa then chốt trong tối ưu hóa kết quả sinh sản và lựa chọn chiến lược điều trị thích hợp.
-
Kết luận
Sức khỏe sinh sản nữ đang chịu ảnh hưởng bởi nhiều yếu tố như chất độc môi trường, lối sống, nhiễm trùng, bệnh lý và can thiệp dược lý. Những yếu tố này, riêng lẻ hoặc kết hợp, có thể làm suy giảm chức năng ống dẫn trứng và khả năng sinh sản. Mặc dù dữ liệu trên động vật khá rõ ràng, bằng chứng trên người vẫn còn hạn chế và cần được nghiên cứu thêm.
Các yếu tố liên quan mạnh nhất ở người bao gồm hút thuốc, uống rượu, nhiễm trùng, lao sinh dục và các can thiệp nội tiết. Việc bảo vệ sức khỏe sinh sản cần cách tiếp cận toàn diện, bao gồm giảm phơi nhiễm với tác nhân có hại, cải thiện lối sống và sử dụng thuốc một cách thận trọng.
Tài liệu tham khảo
1. Barton, B. E., Herrera, G. G., Anamthathmakula, P., Rock, J. K., Willie, A. M., Harris, E. A., Takemaru, K.-I., & Winuthayanon, W. (2020). Roles of steroid hormones in oviductal function. Reproduction (Cambridge, England), 159(3), R125–R137.
2. Eddy, C. A., & Pauerstein, C. J. (1980). Anatomy and physiology of the fallopian tube. Clinical Obstetrics and Gynecology, 23(4), 1177–1193. https://doi.org/10.1097/00003081-198012000-00023
3. Hunter, M. I., Thies, K. M., & Winuthayanon, W. (2024). Hormonal regulation of cilia in the female reproductive tract. Current opinion in endocrine and metabolic research, 34, 100503. https://doi.org/10.1016/j.coemr.2024.100503
4. Roy, O., Kumari, S., Adiga, S. K., Joshi, M. B., Kumar, A., Venkatraman, G., Kannan, N., & Kalthur, G. (2026). Functional Changes in the Fallopian Tube: Environmental Factors, Lifestyle, Pathological Conditions and Pharmacological Agents. Cells, 15(3), 269. https://doi.org/10.3390/cells15030269
5. Keswani, C., Dilnashin, H., Birla, H., Roy, P., Tyagi, R. K., Singh, D., Rajput, V. D., Minkina, T., & Singh, S. P. (2022). Global footprints of organochlorine pesticides: A pan-global survey. Environmental Geochemistry and Health, 44(1), 149–177. https://doi.org/10.1007/s10653-021-00946-7
6. Fuortes, L., Clark, M. K., Kirchner, H. L., & Smith, E. M. (1997). Association between female infertility and agricultural work history. American Journal of Industrial Medicine, 31(4), 445–451. https://doi.org/10.1002/(sici)1097-0274(199704)31:4%253C445::aid-ajim11%253E3.0.co;2-%2523
7. Lerro, C. C., Koutros, S., Andreotti, G., Sandler, D. P., Lynch, C. F., Louis, L. M., Blair, A., Parks, C. G., Shrestha, S., Lubin, J. H., Albert, P. S., Hofmann, J. N., & Beane Freeman, L. E. (2019). Cancer incidence in the Agricultural Health Study after twenty years of follow-up. Cancer causes & control : CCC, 30(4), 311–322. https://doi.org/10.1007/s10552-019-01140-y
8. Scsukova, S., Rollerova, E., & Bujnakova Mlynarcikova, A. (2016). Impact of endocrine disrupting chemicals on onset and development of female reproductive disorders and hormone-related cancer. Reproductive Biology, 16(4), 243–254. https://doi.org/10.1016/j.repbio.2016.09.001
9. Duh-Leong, C., Maffini, M. V., Kassotis, C. D., Vandenberg, L. N., & Trasande, L. (2023). The regulation of endocrine-disrupting chemicals to minimize their impact on health. Nature Reviews. Endocrinology, 19(10), 600–614. https://doi.org/10.1038/s41574-023-00872-x
10. McLachlan, J. A., Simpson, E., & Martin, M. (2006). Endocrine disrupters and female reproductive health. Best Practice & Research. Clinical Endocrinology & Metabolism, 20(1), 63–75. https://doi.org/10.1016/j.beem.2005.09.009
11. Gaskins, A. J., Missmer, S. A., Rich-Edwards, J. W., Williams, P. L., Souter, I., & Chavarro, J. E. (2018). Demographic, lifestyle, and reproductive risk factors for ectopic pregnancy. Fertility and sterility, 110(7), 1328–1337. https://doi.org/10.1016/j.fertnstert.2018.08.022
12. Xu, T., Yang, Q., Liu, R., Wang, W., Wang, S., Liu, C., & Li, J. (2016). Ethanol impedes embryo transport and impairs oviduct epithelium. Toxicology, 357–358, 44–51. https://doi.org/10.1016/j.tox.2016.06.001
13. Lenz, J. D., & Dillard, J. P. (2018). Pathogenesis of Neisseria gonorrhoeae and the Host Defense in Ascending Infections of Human Fallopian Tube. Frontiers in Immunology, 9, 2710. https://doi.org/10.3389/fimmu.2018.02710
14. Ashshi, A. M., Batwa, S. A., Kutbi, S. Y., Malibary, F. A., Batwa, M., & Refaat, B. (2015). Prevalence of 7 sexually transmitted organisms by multiplex real-time PCR in Fallopian tube specimens collected from Saudi women with and without ectopic pregnancy. BMC Infectious Diseases, 15, 569. https://doi.org/10.1186/s12879-015-1313-1
15. Yue, J., Zhang, B., Wang, M., Yao, J., Zhou, Y., Ma, D., & Jin, L. (2019). Effect of antitubercular treatment on the pregnancy outcomes and prognoses of patients with genital tuberculosis. Frontiers of Medicine, 13(1), 121–125. https://doi.org/10.1007/s11684-018-0615-2
16. Milosavljević, M. N., Janković, S. V., Janković, S. M., Djurić, J., Protrka, Z., Arsenijević, S., Folić, M., Stojadinović, D., & Dimitrijević, A. (2019). Effects of selective serotonin reuptake inhibitors on motility of isolated fallopian tube. Clinical and Experimental Pharmacology & Physiology, 46(8), 780–787. https://doi.org/10.1111/1440-1681.13118
17. Ekerhovd, E., & Norström, A. (2004). Involvement of a nitric oxide-cyclic guanosine monophosphate pathway in control of fallopian tube contractility. Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology, 19(5), 239–246. https://doi.org/10.1080/09513590400019296
18. Jankovic, S. M., Jankovic, S. V., Kostic, J., Kostic, I., & Jakovljevic, M. (2006). Inhibitory effects of selected antiepileptics on spontaneous motility of isolated human oviducts. European Journal of Clinical Pharmacology, 62(9), 707–712. https://doi.org/10.1007/s00228-006-0172-5
19. Dash, S., Yoder, S., Mesa, T., Smith, A., Cen, L., Eschrich, S., Armaiz-Pena, G. N., & Monteiro, A. N. A. (2021). Effects of long-term norepinephrine treatment on normal immortalized ovarian and fallopian tube cells. Scientific Reports, 11(1), 14334. https://doi.org/10.1038/s41598-021-93506-z
20. Kopp-Kallner, H., Linder, M., Cesta, C. E., Segovia Chacón, S., Kieler, H., & Graner, S. (2022). Method of Hormonal Contraception and Protective Effects Against Ectopic Pregnancy. Obstetrics and Gynecology, 139(5), 764–770. https://doi.org/10.1097/AOG.0000000000004726
21. Christow, A., Sun, X., & Gemzell-Danielsson, K. (2002). Effect of mifepristone and levonorgestrel on expression of steroid receptors in the human Fallopian tube. Molecular Human Reproduction, 8(4), 333–340. https://doi.org/10.1093/molehr/8.4.333
22. Camus, E., Poncelet, C., Goffinet, F., Wainer, B., Merlet, F., Nisand, I., & Philippe, H. J. (1999). Pregnancy rates after in-vitro fertilization in cases of tubal infertility with and without hydrosalpinx: A meta-analysis of published comparative studies. Human Reproduction, 14(5), 1243–1249. https://doi.org/10.1093/humrep/14.5.1243
23. Hydrosalpinx treatment before in-vitro fertilization: Systematic review and network meta-analysis—PubMed. (không ngày). Truy vấn 20 Tháng Ba 2026, từ https://pubmed.ncbi.nlm.nih.gov/38764191/
24. Yang, H., Xu, Y., Cheng, S., Zhang, H., Cheng, J., & Gao, F. (2025). Evaluation of pregnancy outcomes using a novel hysterosalpingography scoring system for tubal patency. European Journal of Obstetrics & Gynecology and Reproductive Biology: X, 29, 100437. https://doi.org/10.1016/j.eurox.2025.100437