CVPH. Ngô Thị Lan Phương
IVFMD FAMILY, Bệnh viện Đa khoa Gia Đình Đà Nẵng
Giới thiệu
Ty thể đóng vai trò trung tâm trong sản xuất năng lượng và điều hòa oxy hóa khử ở tinh trùng, hỗ trợ các chức năng quan trọng như di động, hoạt hóa và phản ứng acrosome. Những quá trình này rất cần thiết cho sự thụ tinh thành công và phát triển phôi thai. Ty thể cũng tạo ra các gốc oxy phản ứng (reactive oxygen species-ROS), ở mức sinh lý, chúng hỗ trợ chức năng của tinh trùng nhưng có thể gây ra stress oxy hóa và tổn thương khi sản sinh quá mức. Rối loạn chức năng ty thể và ROS quá mức có thể làm suy giảm điện thế màng, gây ra apoptosis và làm tổn thương DNA nhân và ty thể, cuối cùng ảnh hưởng đến chất lượng tinh trùng. DNA ty thể của tinh trùng rất dễ bị đột biến và mất đoạn, làm giảm khả năng vận động và khả năng sinh sản. Các chiến lược chống oxy hóa có mục tiêu đã nổi lên như những biện pháp can thiệp điều trị đầy hứa hẹn để giảm thiểu tổn thương do oxy hóa.
Quá trình chuyển hóa năng lượng của ty thể trong tinh trùng
Quá trình đường phân và phosphoryl hóa oxy hóa ty thể (oxidative phosphorylation-OXPHO ) là hai con đường trao đổi chất chính tạo ra năng lượng tế bào dưới dạng ATP. Ở tinh trùng, các con đường trao đổi chất này được định vị trong các ngăn tế bào riêng biệt. OXPHOS xảy ra trong ty thể, chỉ nằm ở phần giữa của tinh trùng, trong khi quá trình đường phân diễn ra chủ yếu ở lớp vỏ xơ của roi tinh trùng, nơi các enzyme đường phân được neo giữ chặt chẽ [1]. Một lượng nhỏ các enzyme đường phân có thể được tìm thấy ở các vị trí khác của tinh trùng, chẳng hạn như đầu. Điều này có thể liên quan đến sự hiện diện của các chất vận chuyển glucose riêng biệt ở các vùng tinh trùng xa roi tinh trùng. Hơn nữa, chất nền chính cho quá trình đường phân là glucose, được chuyển hóa thành pyruvate và/hoặc lactate trong điều kiện kỵ khí. Các chất nền cho OXPHOS ty thể đa dạng hơn và thường được đại diện bởi các phân tử khác nhau có nguồn gốc từ quá trình dị hóa carbohydrate, lipid và protein. Hơn nữa, quá trình đường phân và quá trình phosphoryl hóa oxy hóa ty thể không phải là các con đường thay thế cho nhau, như thường được nêu trong các tài liệu, mà con đường đầu tiên là bước chuẩn bị cho con đường thứ hai khi xét đến quá trình oxy hóa glucose hoàn toàn và hiếu khí.
Tác động của ROS ty thể lên tinh trùng
-
Nguồn gốc của ROS ty thể trong tinh trùng
Việc tạo ra ROS đòi hỏi sự kích hoạt chuỗi vận chuyển điện tử ty thể và chủ yếu diễn ra trên màng trong ty thể trong quá trình OXPHOS. Ty thể là nguồn chính tạo ra các loại ROS trong tinh trùng, bao gồm anion superoxide (O2-), gốc hydroxyl (-OH) và hydrogen peroxide (H2O2). Quá trình này chủ yếu diễn ra trong chuỗi vận chuyển điện tử của OXPHOS tại màng trong ty thể. Ở điều kiện sinh lý bình thường, tinh trùng có hệ thống chống oxy hóa giúp duy trì cân bằng ROS, từ đó hỗ trợ các chức năng thiết yếu. Tuy nhiên, khi ROS tăng quá mức sẽ gây stress oxy hóa (oxidative stress-OS), dẫn đến tổn thương tế bào và suy giảm chất lượng tinh trùng. Sự hình thành ROS trong ty thể chịu ảnh hưởng của nhiều yếu tố, bao gồm quá trình sinh tinh, hoạt động chuyển hóa năng lượng và rối loạn vận chuyển điện tử trong điều kiện căng thẳng, làm gia tăng tạo thành O2− và H2O2. Ngoài ra, bạch cầu, tinh trùng chưa trưởng thành hoặc bất thường, cũng như bệnh lý, thiếu hụt dinh dưỡng, lối sống không lành mạnh và ô nhiễm môi trường, đều góp phần làm tăng ROS và suy giảm chức năng ty thể [2].
-
Hậu quả của việc sản sinh quá mức ROS ty thể và mất cân bằng oxy hóa khử đối với chất lượng tinh trùng
Do chuỗi sự kiện phức tạp và năng động xảy ra trong quá trình sinh tinh (nguyên phân, giảm phân và biệt hóa tế bào), với các hệ thống kiểm soát cần thiết ở cả cấp độ trung ương và ngoại vi, một lượng lớn ROS được tạo ra về mặt sinh lý bởi các tế bào mầm như là sản phẩm phụ của quá trình trao đổi chất của chúng. Tuy nhiên, một lượng ROS vừa phải cũng có lợi cho các chức năng thông thường, chẳng hạn như truyền tín hiệu tế bào, cân bằng nội môi, hoạt hóa tinh trùng và tương tác giữa tinh trùng và noãn. Đặc biệt, hoạt hóa tinh trùng được hưởng lợi từ sự trung gian của ROS trong việc tạo ra cAMP, sự thoát cholesterol màng huyết tương tinh trùng và ức chế hoạt động của tyrosine phosphatase. Ngược lại, sự tích tụ ROS trong tinh hoàn gây ra những thay đổi về hình thái trong biểu mô ống sinh tinh và sự hình thành các không bào trong tế bào chất ở cả tế bào mầm, tế bào Sertoli và chết theo chu trình tế bào (apoptosis) [3].
-
Tác động của ROS ty thể lên bộ gen và hệ gen biểu sinh của tinh trùng: Tổn thương DNA do oxy hóa ở tinh trùng bao gồm sự phân mảnh DNA do đứt gãy sợi đơn và sợi kép, sự xuất hiện của các vị trí không có bazơ hoặc các bazơ bị oxy hóa. Những tác động này chắc chắn bị trầm trọng thêm bởi cấu trúc vật lý của tinh trùng, vì chúng bị thiếu các enzyme tế bào chất thiết yếu hoặc hệ thống sửa chữa DNA hoạt động đầy đủ, không có khả năng kích hoạt phiên mã của các gen mã hóa các enzyme chống oxy hóa liên quan và sự bảo vệ DNA hạt nhân của chúng bằng cách xâm nhập của nuclease. Điều đáng báo động là tinh trùng có DNA bị tổn thương vẫn có thể thụ tinh, với những hậu quả nguy hiểm đối với phôi. Tăng tổn thương DNA do oxy hóa ở tinh trùng có tác động mạnh mẽ đến các thế hệ tiếp theo; Nó có liên quan đến bệnh ung thư ở trẻ em, rối loạn não như tự kỷ và tâm thần phân liệt [4].
-
ROS ty thể quá mức cũng có thể gây ra những thay đổi biểu sinh, rút ngắn telomere, mất đoạn nhỏ nhiễm sắc thể Y và kích hoạt các con đường apoptosis. Do khả năng sửa chữa DNA hạn chế trong tế bào tinh trùng, tổn thương DNA thường không được sửa chữa, dẫn đến tăng phosphoryl hóa và kích hoạt p53, từ đó kích hoạt con đường apoptosis phụ thuộc vào ty thể [5].
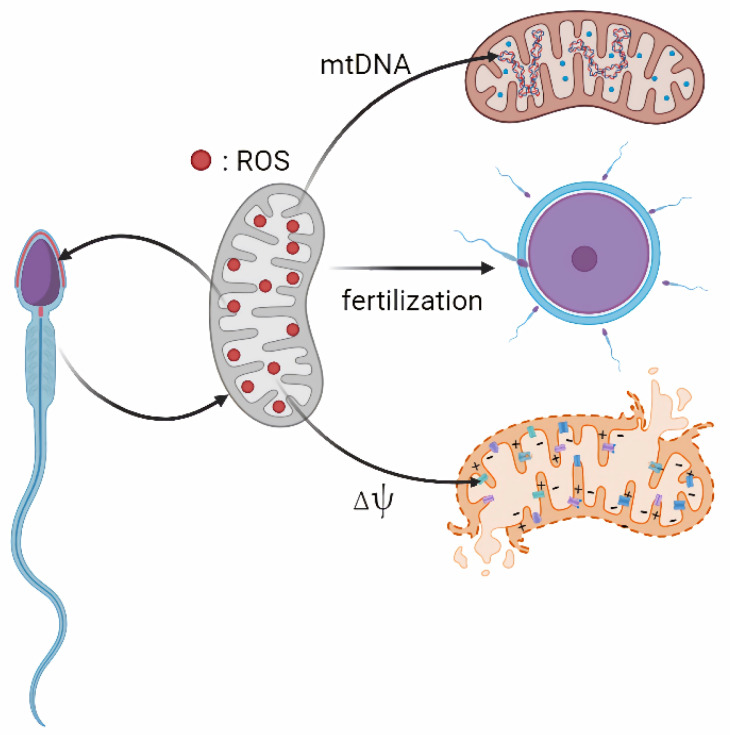
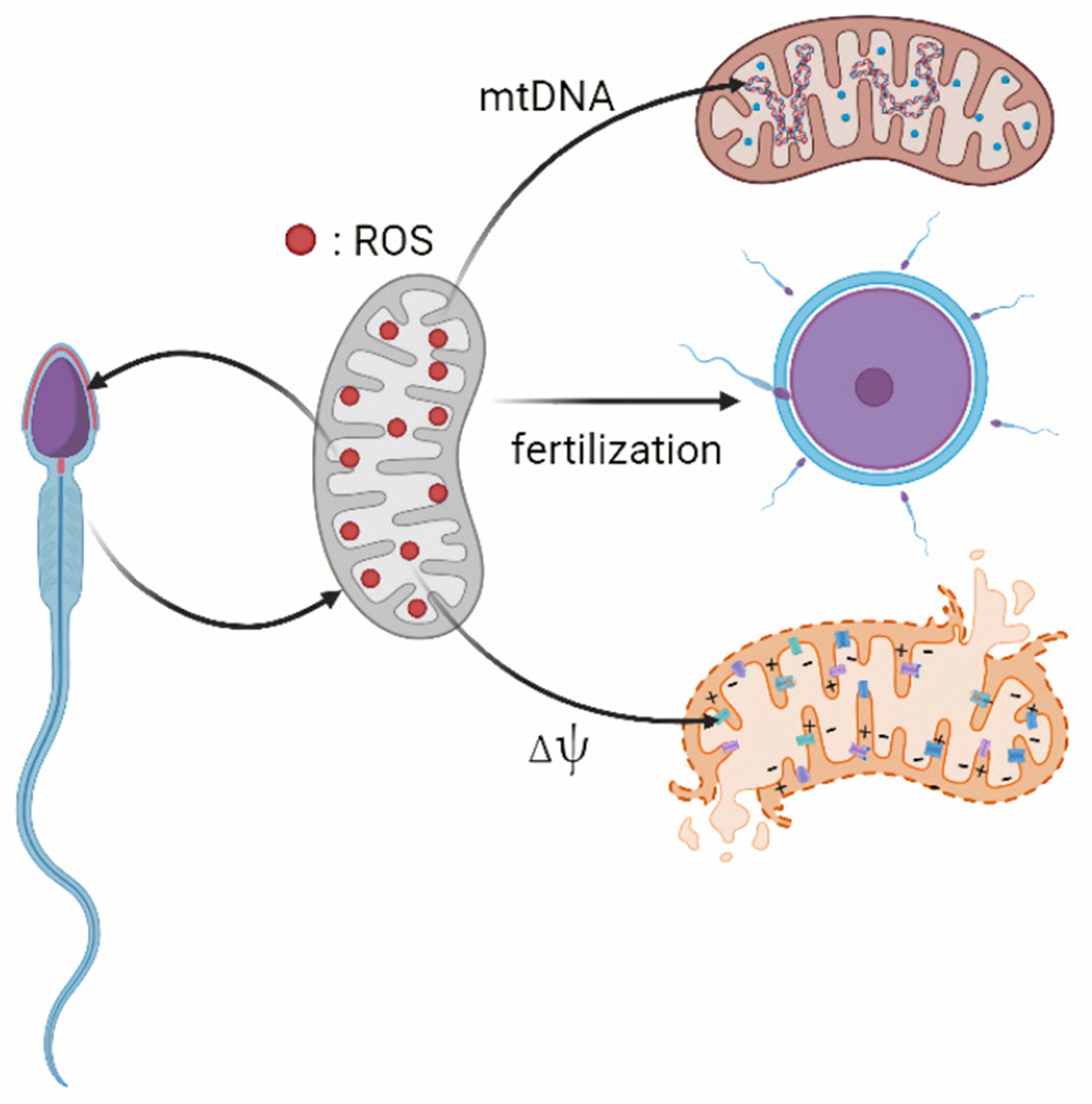
Hình 1. Tác động của ROS ty thể lên tinh trùng [2].
-
Tác động của ROS lên lipid và protein trong tinh trùng: Trên thực tế, tính nhạy cảm của tinh trùng đối với ROS bị trầm trọng thêm bởi thành phần lipid rất đặc biệt của màng huyết tương của nó là giàu axit béo không bão hòa (polyunsaturated fatty acids - PUFA). Là mục tiêu chính của ROS, màng huyết tương của tinh trùng có thể kích thích một chuỗi tín hiệu hạ lưu, làm tổn thương cả bộ gen nhân và ty thể. Cùng với lipid, protein tinh trùng, đặc biệt là protein nằm trong nhân, có thể bị ảnh hưởng bởi ROS thông qua quá trình cacbonyl hóa và sửa đổi thiol khử oxy hóa. Các protein nhân tinh trùng chứa thiol đặc biệt là protamine, quá trình oxy hóa của chúng làm thay đổi hoàn toàn sự gấp nếp và chức năng của chromatin. Mặc dù sự thay đổi của protamine không được cho là gây hại cho phôi thai do chúng được loại bỏ nhanh chóng sau khi thụ tinh, nhưng có khả năng quá trình cacbonyl hóa protamine ảnh hưởng đến liên kết chéo protein-protein và cấu trúc nhân tổng thể. Nguy hiểm hơn đối với phôi thai là quá trình oxy hóa histone của bố vẫn còn lại sau khi thụ tinh, tạo ra các vấn đề không ngờ tới trong phôi đang phát triển. Về vấn đề này, stress oxy hóa làm tăng quá trình methyl hóa histone, có liên quan đến các đứt gãy chuỗi kép và chất lượng tinh trùng kém. Cùng với quá trình methyl hóa, quá trình acetyl hóa histone cũng bị suy giảm do stress oxy hóa. Quá trình tái cấu trúc chromatin chắc chắn bị ảnh hưởng [6].
Tầm quan trọng của sự ổn định mtDNA (mitochondrial DNA) trong việc duy trì chức năng ty thể
-
Đặc điểm của mtDNA tinh trùng
DNA ty thể của tinh trùng có những đặc điểm di truyền riêng biệt, đáng chú ý là kiểu di truyền theo dòng mẹ. Cả người và động vật đều đã phát triển một loạt các cơ chế để loại bỏ ty thể và DNA ty thể của tinh trùng. Kết quả là, số lượng ty thể và DNA ty thể trong tinh trùng giảm dần trong quá trình sinh tinh và thụ tinh. Do đó, DNA ty thể chủ yếu hoạt động trong các quá trình trao đổi chất của tinh trùng trước khi thụ tinh. Và khả năng đột biến của DNA ty thể cũng rất đáng chú ý. mtDNA là một phân tử trần không có intron và histon, và cả hai chuỗi của nó đều được phiên mã để tổng hợp các protein chức năng. Do sao chép vô tính, cơ chế sửa chữa rất cơ bản, thiếu histon bảo vệ và gần các vị trí hình thành gốc tự do, mtDNA có tỷ lệ đột biến cao hơn 10 đến 20 lần so với DNA nhân. Hơn nữa, mtDNA sao chép nhanh chóng khi không có bộ máy sửa chữa DNA. Do đó, mtDNA dễ bị đột biến hơn 100 lần so với DNA nhân. Hơn nữa, các enzyme sao chép DNA ty thể có khả năng sửa lỗi kém, dẫn đến xác suất xảy ra lỗi cao hơn trong quá trình sao chép. Và sự thiếu vắng các hệ thống sửa chữa hiệu quả góp phần đáng kể vào nguy cơ đột biến DNA ty thể gia tăng, với tần suất cao hơn nhiều lần so với tần suất quan sát được ở DNA nhân. Ngoài ra, mtDNA thiếu sự bảo vệ từ histon và protein liên kết DNA, khiến nó tiếp xúc trực tiếp với chất nền ty thể. Điều này khiến nó dễ bị tổn thương do ROS, dẫn đến sự suy giảm các chức năng sinh lý bình thường của tinh trùng [2].
-
Ảnh hưởng của đột biến mtDNA đến chức năng tinh trùng
Người ta ước tính rằng khoảng 15% đến 30% trường hợp vô sinh ở nam giới là do khiếm khuyết di truyền. Ty thể có bộ gen riêng (hơn 93.000 gen). Một số gen liên quan đến khả năng sinh sản và tuổi thọ cũng được biết là có liên quan đến ty thể [7]. Ngày càng có nhiều bằng chứng cho thấy các đa hình đơn nucleotide (single-nucleotide polymorphisms-SNP) trong mtDNA có thể ảnh hưởng đáng kể đến khả năng sinh sản của nam giới. Ví dụ, mức độ cao của đột biến điểm A3243G trong mtDNA có liên quan chặt chẽ đến việc giảm khả năng vận động của tinh trùng. Và một số SNP trong các gen mtDNA, chẳng hạn như MT-CYB, MT-CO3 và MT-ATP6, đã được chứng minh là có liên quan đến khả năng sinh sản của nam giới [8].
Một nghiên cứu trước đây đã báo cáo rằng khả năng vận động của tinh trùng có tương quan nghịch với sự xóa bỏ mtDNA. Theo kết quả nghiên cứu, các đột biến xóa bỏ mtDNA được tìm thấy ở tinh trùng bất động, trong khi tinh trùng có khả năng vận động bình thường không có các đột biến xóa bỏ này. Hơn nữa, người ta đã lưu ý rằng tỷ lệ đột biến xóa bỏ này trong mtDNA cao hơn ở tinh trùng có khả năng vận động bình thường so với tinh trùng có khả năng vận động thấp [9].
Các phương pháp điều trị chống oxy hóa nhắm vào ty thể để cải thiện chất lượng tinh trùng
Do ty thể là nguồn gốc của ROS, các chiến lược dựa trên chất chống oxy hóa nhắm vào ty thể đã nổi lên như những biện pháp can thiệp đầy hứa hẹn để khôi phục cân bằng oxy hóa khử và cải thiện chức năng tinh trùng. Các chất chống oxy hóa nhắm vào ty thể phổ biến bao gồm ubiquinone (MitoQ), melatonin, quercetin, MitoTEMPO,… Các chất chống oxy hóa nhắm vào ty thể ngăn chặn tổn thương oxy hóa thông qua liên kết cộng hóa trị của các cation ưa lipid như cation ưa lipid triphenylphosphonium (TPP +) trong ty thể [2].
-
TPP + của các chất chống oxy hóa nhắm vào ty thể có thể dễ dàng xuyên qua lớp màng lipid của màng ty thể và đưa chất chống oxy hóa vào ty thể. Sau khi vào bên trong ty thể, các hợp chất này có thể tích lũy với số lượng lớn, thể hiện tác dụng chống oxy hóa ty thể đáng kể [10].
-
MitoQ là một chất chống oxy hóa nhắm mục tiêu vào ty thể được nghiên cứu rộng rãi. Nó nhận electron từ phức hợp protein chuỗi hô hấp ty thể I hoặc II và khử thành ubiquinol, sau đó chuyển các electron này đến phức hợp ty thể III. Ubiquinol cũng hoạt động như một chất chống oxy hóa bằng cách cung cấp các nguyên tử hydro cho các gốc peroxyl lipid. Việc bổ sung MitoQ vào tinh trùng người đã dẫn đến cải thiện chức năng tinh trùng, làm giảm tổn thương DNA và đồng thời gây ra sự điều hòa tăng cường biểu hiện gen chống oxy hóa, do đó mang lại lợi ích bổ sung cho việc bảo quản lạnh tinh trùng [11].
-
Melatonin duy trì điện thế màng ty thể (mitochondrial membrane potential- MMP) tối ưu bằng cách loại bỏ ROS, kích hoạt các protein tách cặp và ức chế sự hình thành 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine. Melatonin cũng có thể tối ưu hóa sự phân bố các enzyme cần thiết cho OXPHOS trong tinh trùng, tăng cường hoạt động của các phức hợp protein chuỗi hô hấp, cuối cùng thúc đẩy khả năng sử dụng oxy của tinh trùng đông lạnh khi rã đông. Nó được ứng dụng rộng rãi như một chất phụ gia chống oxy hóa trong quá trình đông lạnh tinh trùng [12].
-
Quercetin là một flavone nhắm mục tiêu vào ty thể; nó có thể làm giảm sự tích tụ lipid peroxide bằng cách trung hòa các gốc tự do có hại và gắn vào các ion kim loại chuyển tiếp. Hoạt động này làm thay đổi tính linh động của màng ty thể và ảnh hưởng đến các protein oxy hóa trong ty thể. Nó cũng điều chỉnh quá trình sinh tổng hợp ty thể, MMP, OXPHOS và sản xuất ATP, trạng thái oxy hóa khử của ty thể, và cuối cùng kích hoạt quá trình apoptosis do ty thể trung gian. Quercetin có thể điều chỉnh hiệu quả hô hấp ty thể của tinh trùng ở nam giới bị suy giảm khả năng vận động của tinh trùng. Tuy vậy, cơ chế phân tử chính xác đằng sau hoạt động của quercetin vẫn chưa được hiểu đầy đủ, và cũng có những nghiên cứu cho thấy quercetin không có tác dụng đáng kể đối với chất lượng tinh trùng đông lạnh. Cần nghiên cứu thêm để làm rõ tác dụng bảo vệ của nó trong quá trình đông lạnh tinh dịch.
-
MitoTEMPO là một chất loại bỏ ROS bao gồm piperidine nitroxide TEMPOL và triphenylphosphine (TPP) ưa lipid. Là một chất chống oxy hóa mới có khả năng thấm qua màng tế bào, đặc tính ưa lipid của nó cho phép nó nhanh chóng thấm qua màng lipid kép của ty thể và tích tụ ở nồng độ cao bên trong các bào quan này. Nghiên cứu đã chỉ ra rằng việc bổ sung MitoTEMPO đã cải thiện đáng kể khả năng vận động, tính toàn vẹn màng và MMP của tinh trùng sau khi rã đông ở người, đồng thời giảm mức ROS trong ty thể tinh trùng, cho thấy MitoTEMPO có thể đóng vai trò như một chất bảo vệ lạnh hiệu quả cho các mẫu tinh dịch, và cũng có thể làm giảm tổn thương do lạnh đối với tinh trùng yếu sau khi bảo quản lạnh [13].
Các chất chống oxy hóa nhắm vào ty thể đã thu hút sự chú ý đáng kể, làm nổi bật vai trò quan trọng của hoạt động chống oxy hóa ty thể trong việc duy trì chức năng tinh trùng. Tuy nhiên, tác dụng của chúng cho kết quả không nhất quán, điều này có thể được giải thích bởi phản ứng hai pha, phụ thuộc vào nồng độ của tế bào tinh trùng đối với các chất chống oxy hóa. Bên cạnh các chất chống oxy hóa nhắm vào ty thể đã được giới thiệu trước đây, ngày càng nhiều hợp chất có đặc tính chống oxy hóa ty thể cũng đang được nghiên cứu về vai trò của chúng trong chức năng tinh trùng. Có thể suy ra rằng các chất chống oxy hóa nhắm vào ty thể có tiềm năng hữu ích trong việc cải thiện stress oxy hóa (oxidative stress-OS ) ở tinh trùng, đặc biệt là cho thấy kết quả khả quan trong việc giảm thiểu stress oxy hóa ty thể do đông lạnh gây ra. Cần có những nghiên cứu và nỗ lực trong tương lai để kiểm tra hiệu quả của các chất chống oxy hóa ty thể, làm sáng tỏ cơ chế hoạt động của chúng và phát triển thêm các chất chống oxy hóa đặc hiệu ty thể mạnh mẽ hơn.
Kết luận
Ty thể giữ vai trò trung tâm trong điều hòa chuyển hóa năng lượng, cân bằng oxy hóa khử và duy trì chức năng của tinh trùng. Mức ROS ty thể sinh lý cần thiết cho các quá trình như hoạt hóa và phản ứng acrosome; tuy nhiên, sự gia tăng quá mức ROS gây stress oxy hóa, rối loạn chức năng ty thể và tổn thương DNA. Các chất chống oxy hóa hướng đích ty thể cho thấy tiềm năng trong việc cải thiện khả năng vận động, sức sống và tiềm năng thụ tinh của tinh trùng, song vẫn cần thêm nghiên cứu để tối ưu hóa loại, liều lượng và phương thức sử dụng.
Tài liệu tham khảo
1. Ferramosca, A., & Zara, V. (2014). Bioenergetics of Mammalian Sperm Capacitation. BioMed Research International, 2014, 902953. https://doi.org/10.1155/2014/902953
2. Xu, Z., Yan, Q., Zhang, K., Lei, Y., Zhou, C., Ren, T., Gao, N., Wen, F., & Li, X. (2025). Mitochondrial Regulation of Spermatozoa Function: Metabolism, Oxidative Stress and Therapeutic Insights. Animals: an Open Access Journal from MDPI, 15(15), 2246. https://doi.org/10.3390/ani15152246
3. Chianese, R., & Pierantoni, R. (2021). Mitochondrial Reactive Oxygen Species (ROS) Production Alters Sperm Quality. Antioxidants, 10(1), 92. https://doi.org/10.3390/antiox10010092
4. Smith, T. B., De Iuliis, G. N., Lord, T., & Aitken, R. J. (2013). The senescence-accelerated mouse prone 8 as a model for oxidative stress and impaired DNA repair in the male germ line. Reproduction, 146(3), 253–262. https://doi.org/10.1530/REP-13-0186
5. Liu, Y., Su, Z., Tavana, O., & Gu, W. (2024). Understanding the complexity of p53 in a new era of tumor suppression. Cancer Cell, 42(6), 946–967. https://doi.org/10.1016/j.ccell.2024.04.009
6. Montjean, D., Ravel, C., Benkhalifa, M., Cohen-Bacrie, P., Berthaut, I., Bashamboo, A., & McElreavey, K. (2013). Methylation changes in mature sperm deoxyribonucleic acid from oligozoospermic men: Assessment of genetic variants and assisted reproductive technology outcome. Fertility and Sterility, 100(5), 1241–1247. https://doi.org/10.1016/j.fertnstert.2013.06.047
7. Amor, H., & Hammadeh, M. E. (2022). A Systematic Review of the Impact of Mitochondrial Variations on Male Infertility. Genes, 13(7), 1182. https://doi.org/10.3390/genes13071182
8. Saleh Jaweesh, M., Hammadeh, M. E., Dahadhah, F. W., Al Zoubi, M. S., & Amor, H. (2022). Association between the single nucleotide variants of the mitochondrial cytochrome B gene (MT-CYB) and the male infertility. Molecular Biology Reports, 49(5), 3609–3616. https://doi.org/10.1007/s11033-022-07200-y
9. Carra, E., Sangiorgi, D., Gattuccio, F., & Rinaldi, A. M. (2004). Male infertility and mitochondrial DNA. Biochemical and Biophysical Research Communications, 322(1), 333–339. https://doi.org/10.1016/j.bbrc.2004.07.112
10. Escada-Rebelo, S., Cristo, M. I., Ramalho-Santos, J., & Amaral, S. (2022). Mitochondria-Targeted Compounds to Assess and Improve Human Sperm Function. Antioxidants & Redox Signaling, 37(7–9), 451–480. https://doi.org/10.1089/ars.2021.0238
11. Moradi Gardeshi, T., Shahandeh, E., Tavakolpoor Saleh, N., Karami, S., Mirzaei Azandaryani, Z., Mazaheri, F., & Mohammadi, H. (2024). Evaluation of the effect of mitoquinone on functional parameters, DNA structure, and genes expression related to the apoptotic and antioxidants of human sperm after freezing-thawing. Molecular Biology Reports, 51(1), 183. https://doi.org/10.1007/s11033-023-09020-0
12. Alevra, A. I., Exadactylos, A., Mente, E., & Papadopoulos, S. (2022). The Protective Role of Melatonin in Sperm Cryopreservation of Farm Animals and Human: Lessons for Male Fish Cryopreservation. Animals: an Open Access Journal from MDPI, 12(6), 791. https://doi.org/10.3390/ani12060791
13. Lu, X., Zhang, Y., Bai, H., Liu, J., Li, J., & Wu, B. (2018). Mitochondria-targeted antioxidant MitoTEMPO improves the post-thaw sperm quality. Cryobiology, 80, 26–29. https://doi.org/10.1016/j.cryobiol.2017.12.009