CVPH. Nguyễn Thị Nguyệt
Đơn vị HTSS IVFMD FAMILY, BVĐK Gia Đình, Đà Nẵng
Trong hai thập kỷ gần đây, phòng lab thụ tinh trong ống nghiệm (In vitro fertilization - IVF) đã chuyển dịch rõ rệt từ các thao tác thủ công phụ thuộc kinh nghiệm cá nhân sang các nền tảng công nghệ hướng tới chuẩn hóa quy trình. Tuy nhiên, ngay cả khi môi trường nuôi cấy, hệ thống vi thao tác và đánh giá phôi đã được cải tiến, các “điểm nghẽn” cốt lõi vẫn còn hiện hữu: khác biệt kỹ thuật xử lý mẫu, lực quay ly tâm trong chuẩn bị tinh trùng, vi môi trường nuôi cấy tĩnh khó mô phỏng sinh lý ống dẫn trứng, và hạn chế của đánh giá phôi chủ yếu dựa hình thái. Các thách thức này thúc đẩy nhu cầu về những nền tảng có khả năng kiểm soát vi môi trường sinh học ở quy mô micro–nano và dễ tích hợp vào quy trình thường quy [1].
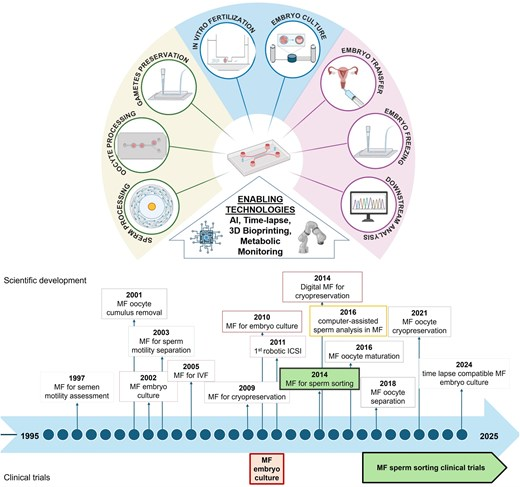
Trong bối cảnh đó, công nghệ vi lưu (Microfluidics) nổi lên không chỉ như một “thiết bị mới”, mà là một hệ nền tảng cho phép thao tác chính xác với thể tích nl–µl, kiểm soát dòng chảy/gradient và hỗ trợ tự động hóa. Tổng quan Human Reproduction Update gần đây cho thấy trong 20 năm phát triển, microfluidics đã hình thành ba cụm ứng dụng chính trong các kỹ thuật hỗ trợ sinh sản (Assisted Reproductive Technology – ART): (i) xử lý và thao tác giao tử (đặc biệt tinh trùng); (ii) giải pháp hỗ trợ phát triển phôi in vitro; và (iii) tiếp cận vi lưu cho thuỷ tinh hoá và bảo tồn sinh sản. Đồng thời, mặc dù số bằng sáng chế tích lũy rất lớn (1405 bằng từ 2000–2025), số thử nghiệm lâm sàng khởi động từ 2009 vẫn còn hạn chế (19 thử nghiệm), phản ánh khoảng cách điển hình giữa đổi mới kỹ thuật và bằng chứng lâm sàng [1].
1.Nền tảng cơ chế: vì sao vi lưu “hợp logic sinh lý” với ART?
Điểm khác biệt nền tảng của vi lưu so với các hệ “đĩa nuôi tĩnh” là khả năng tạo ra vi môi trường động: dòng chảy laminar ổn định, gradient hóa học – nhiệt độ, lực cắt có thể điều chỉnh và mô phỏng tương tác tế bào – dịch thể gần sinh lý. Về mặt sinh học sinh sản, điều này đặc biệt phù hợp ở các khâu mà tự nhiên vốn đã là một quá trình sàng lọc cơ học – hóa học (như hành trình của tinh trùng trong đường sinh dục nữ), hoặc các giai đoạn phôi sớm chịu ảnh hưởng mạnh của vi môi trường (oxy, trao đổi chất, tích lũy yếu tố tự tiết/cận tiết).
Ở góc độ vận hành lab, vi lưu còn có giá trị thực dụng: thiết kế dùng một lần, thể tích nhỏ giảm tiêu hao môi trường/hoá chất, dễ tích hợp camera– timelapse/cảm biến, và có tiềm năng chuẩn hóa thao tác giữa các kỹ thuật viên. Tuy nhiên, chính vì ART là lĩnh vực “high-stakes” (liên quan an toàn phôi và sức khỏe trẻ sinh ra), mọi ưu thế kỹ thuật đều phải được quy đổi thành kết cục lâm sàng (tỷ lệ làm tổ, tỷ lệ thai lâm sàng, tỷ lệ trẻ sinh sống) và dữ liệu theo dõi dài hạn [1].
2.Ứng dụng công nghệ vi lưu (Microfluidics) trong quy trình hỗ trợ sinh sản
-
- Xử lý và chọn lọc tinh trùng: hướng ứng dụng mới
Các phương pháp xử lý tinh trùng truyền thống như swim-up và ly tâm thang nồng độ dựa trên khả năng di động và tỷ trọng tinh trùng. Gần đây, các nền tảng vi lưu được phát triển nhằm mô phỏng môi trường sinh lý đường sinh dục nữ và tuyển chọn tinh trùng dựa trên đặc tính sinh học tự nhiên, cho phép phân lập tinh trùng chất lượng cao với độ toàn vẹn DNA cải thiện lên tới 95% so với mẫu ban đầu [2].
Các hệ thống vi lưu khai thác các cơ chế như định hướng theo dòng chảy (rheotaxis), hóa hướng động (chemotaxis), nhiệt hướng động (thermotaxis) và hội tụ quán tính để chọn lọc tinh trùng có vận động tiến triển tốt và tiềm năng thụ tinh cao, đồng thời giảm tác động cơ học và lực cắt so với ly tâm gradient, qua đó hạn chế tổn thương DNA tinh trùng [3,4].
Về lâm sàng, ở nam giới có đứt gãy DNA sợi kép cao, vi lưu giúp tăng 35,6% tỷ lệ thai lâm sàng và 35,3% tỷ lệ trẻ sinh sống; ở trường hợp đứt gãy DNA sợi đơn, tỷ lệ thụ tinh tăng thêm 11,2% và tỷ lệ phôi nguyên bội cao hơn. Ngoài ra, tỷ lệ thụ tinh khoảng 37% đã được ghi nhận ở bệnh nhân tinh trùng ít (oligospermia). Nhờ thời gian xử lý ngắn (10–30 phút), kết quả ổn định và thiết kế dùng một lần, vi lưu được xem là hướng tiếp cận tiềm năng nhằm chuẩn hóa xử lý tinh trùng trong IVF/ICSI [5].
2.2. Xử lý noãn và thụ tinh: tiềm năng chuẩn hóa thao tác, nhưng lợi ích lâm sàng chưa rõ ràng
Noãn là tế bào có kích thước lớn và nhạy cảm; mọi can thiệp cơ học–enzyme đều có thể ảnh hưởng thoi vô sắc, màng tế bào và tiềm năng phát triển phôi. Do đó, dù vi lưu có thể mang lại lợi ích về tự động hóa, việc chứng minh “ưu thế” so với thao tác thủ công còn gặp nhiều khó khăn. Một ứng dụng khá rõ ràng là tách cumulus (denudation) trên chip, nhằm giảm biến thiên thao tác giữa kỹ thuật viên và rút ngắn thời gian xử lý. Các hệ thống vi lưu được phát triển nhằm tự động hóa quy trình này bằng cách kết hợp xử lý enzym với dòng chảy cưỡng bức trong kênh vi cấu trúc, cho phép loại bỏ cumulus hiệu quả với tỷ lệ noãn được làm sạch hoàn toàn lên đến 98,6%, đồng thời giảm thời gian thao tác và tác động cơ học. Tuy nhiên, các nghiên cứu hiện chưa ghi nhận khác biệt có ý nghĩa về tỷ lệ thụ tinh hay phát triển phôi nang so với phương pháp chuẩn [6].
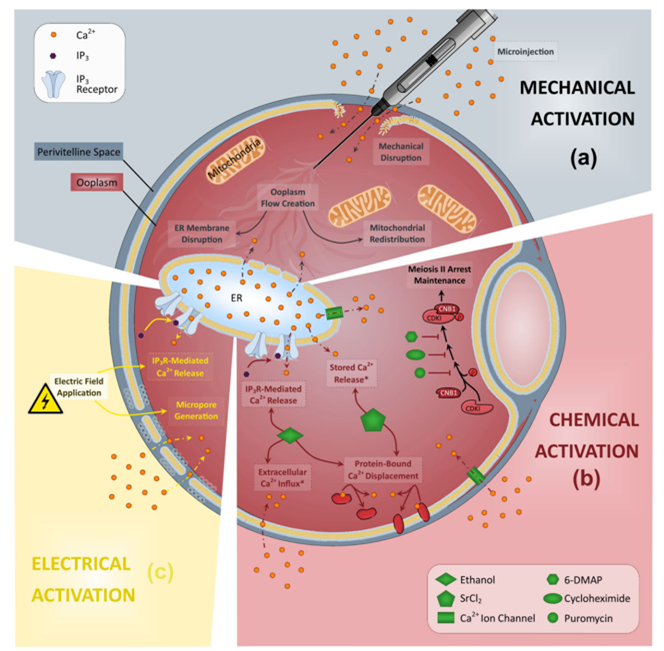
Trong bước thụ tinh, noãn sau khi “làm trần” để thực hiện IVF cổ điển hoặc tiêm tinh trùng vào bào tương noãn (Intracytoplasmic Sperm Injection - ICSI[DN1] ). Một số nền tảng vi lưu đã được đề xuất nhằm kiểm soát tỷ lệ tinh trùng/noãn và điều kiện dòng chảy nhằm tối ưu hóa đơn tinh, song ứng dụng lâm sàng vẫn hạn chế do yêu cầu kỹ thuật cao, chi phí và thiếu bằng chứng về lợi ích kết cục dài hạn [7].
2.3. Nuôi cấy phôi và vi môi trường động: từ tính khả thi đến câu hỏi “ liệu có cải thiện tỷ lệ trẻ sinh sống không?”
Nuôi cấy phôi in vitro là bước then chốt trong IVF nhằm tối ưu hóa sự phát triển phôi và lựa chọn phôi có tiềm năng làm tổ cao. Các hệ thống vi lưu cho phép kiểm soát chính xác thể tích nuôi cấy, nồng độ khí và dòng chảy, qua đó mô phỏng vi môi trường sinh lý của ống dẫn trứng và tử cung. Nuôi cấy trong thể tích cực nhỏ (sub-microliter) giúp tích lũy các yếu tố tự tiết và cận tiết, nhưng nếu thiếu hệ thống khuếch tán phù hợp có thể dẫn đến tích tụ sản phẩm chuyển hóa độc hại, thiếu oxy và suy giảm dinh dưỡng [8].
Các nghiên cứu tiền lâm sàng cho thấy hệ thống vi lưu động có khả năng cải thiện rõ rệt kết cục phát triển phôi. Tỷ lệ noãn trưởng thành MII đạt 83,0% trong hệ thống vi lưu so với 55,3% ở hệ thống nuôi cấy tĩnh; tỷ lệ thụ tinh đạt 84–88% và tỷ lệ phôi nang lên tới 84%, cao hơn đáng kể so với nhóm đối chứng (22,9%) [9].Việc kiểm soát nồng độ oxy (≈5%) trong hệ thống vi lưu góp phần mô phỏng điều kiện in vivo và hỗ trợ phát triển phôi sớm.
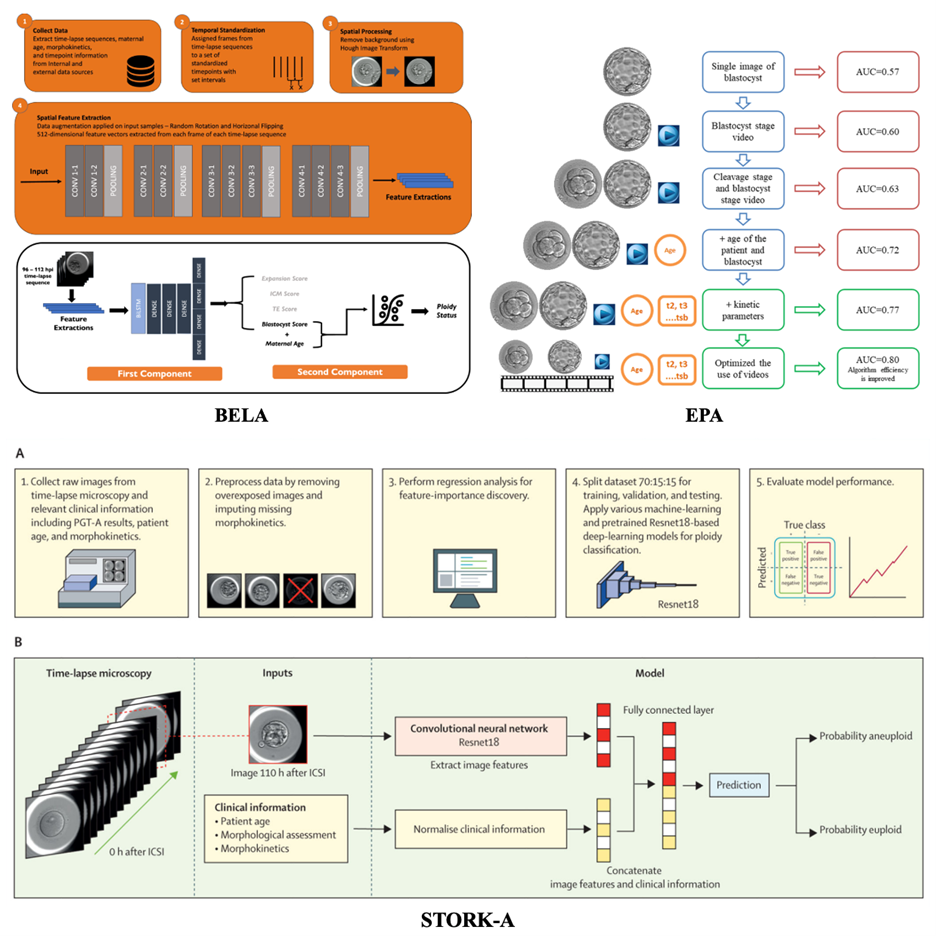
Trong chọn lọc phôi, các nền tảng vi lưu tích hợp theo dõi phôi time-lapse, trí tuệ nhân tạo (Artificial Intelligence – AI) và cảm biến chuyển hóa không xâm lấn cho phép phân tích động học phân chia và các chỉ dấu chức năng, qua đó cải thiện khả năng dự đoán tiềm năng làm tổ so với đánh giá hình thái truyền thống [7]. Tuy nhiên, việc triển khai lâm sàng rộng rãi vẫn còn hạn chế do thiếu dữ liệu kết cục dài hạn và yêu cầu chuẩn hóa quy trình.
2.4. Bảo quản lạnh trên nền tảng vi lưu: kiểm soát tính thẩm thấu để giảm thời gian
Bảo quản lạnh (cryopreservation) là thành phần thiết yếu của các chu kỳ ART, cho phép lưu trữ tinh trùng, noãn và phôi nhằm tối ưu hóa chiến lược điều trị và bảo tồn khả năng sinh sản. Các kỹ thuật thủy tinh hóa hiện đại đã cải thiện đáng kể tỷ lệ sống sót sau rã đông và hiệu quả lâm sàng của IVF.
Các hệ thống vi lưu được phát triển nhằm tự động hóa quá trình tiếp xúc với chất bảo vệ lạnh (Cryoprotectant agents - CPA) và giảm sốc thẩm thấu. Trên mô hình động vật, vi lưu cho thấy giúp giảm tổn thương do thẩm thấu trong quá trình thêm/loại CPA [10]. Tuy nhiên, dữ liệu lâm sàng người cho thủy tinh hóa bán tự động vẫn cho kết quả “chưa vượt trội rõ ràng” so với thao tác tay, Gatimel và cộng sự (2021) báo cáo khác biệt về tỷ lệ sống và kết cục lâm sàng còn hạn chế. Điều này gợi ý vi lưu trong bảo quản lạnh có thể phù hợp nhất ở vai trò chuẩn hóa quy trình và giảm phụ thuộc tay nghề [11].
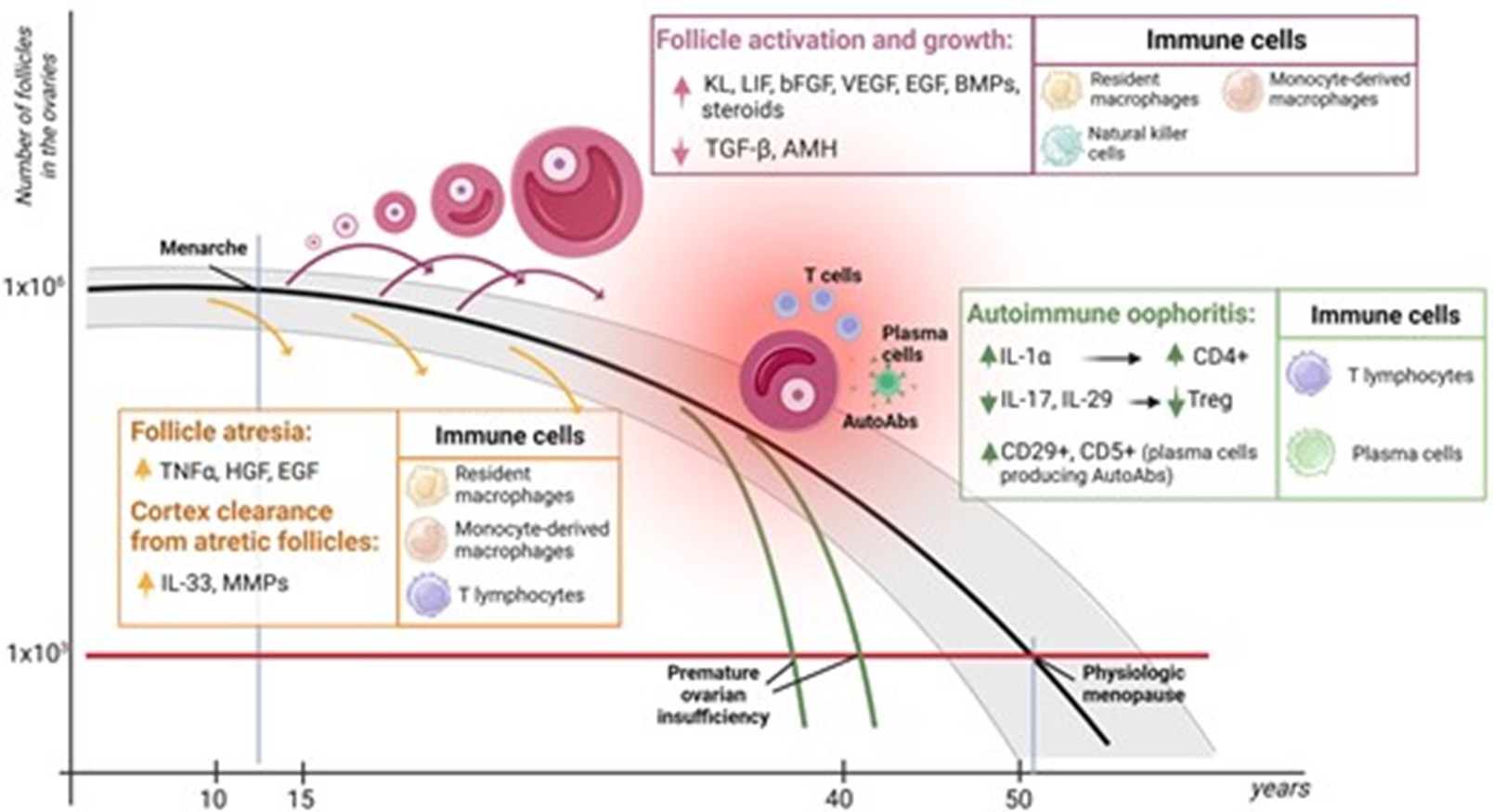
2.5. Bảo tồn khả năng sinh sản ở nữ giới, nuôi cấy nang noãn và noãn: triển vọng dài hạn của “ovary-on-a-chip”
Ở nhóm bệnh nhân cần bảo tồn sinh sản (trước điều trị ung thư, suy buồng trứng sớm, trì hoãn sinh con), các nền tảng nuôi cấy nang noãn và trưởng thành noãn in vitro là hướng đi chiến lược. Vi lưu hỗ trợ duy trì vi môi trường dài hạn, cung cấp trao đổi chất và tín hiệu sinh học ổn định cho nang noãn. Các hệ thống vi lưu cho phép mô phỏng vi môi trường động của buồng trứng, hỗ trợ phát triển nang noãn trong thời gian dài. Aziz và cộng sự (2017) ghi nhận sự tăng trưởng nang và xu hướng hormone tương đương nuôi cấy truyền thống [12]. Choi và cộng sự (2014) báo cáo tỷ lệ phát triển nang thứ cấp đạt 28% và tỷ lệ rụng trứng 100% trong hệ thống 3D alginate–collagen tối ưu [13]. Ở mô vỏ buồng trứng người, nang noãn phát triển đến giai đoạn thứ cấp sau 8 ngày, tuy nhiên dòng chảy cao (0,5 ml/phút) làm tăng apoptosis mô đệm. Các hệ thống IVM vi lưu cho thấy tăng tỷ lệ noãn MII và cải thiện phát triển phôi nang, đặc biệt khi kiểm soát môi trường hypoxic [14].
- Từ ý tưởng đến lâm sàng: vì sao “nhiều bằng sáng chế nhưng ít RCT”?
- Bức tranh đổi mới: tăng mạnh nghiên cứu và IP, nhưng “nút thắt” là thẩm định lâm sàng
Theo Pensabene và cộng sự (2025), tính đến năm 2025 có 1405 bằng sáng chế liên quan vi lưu–ART. Tuy nhiên chỉ 19 thử nghiệm lâm sàng bắt đầu từ 2009, chủ yếu tập trung vào microfluidic sperm sorting và một phần hệ nuôi cấy phôi. Khoảng cách này phản ánh rào cản điển hình của thiết bị y sinh trong ART: cần tiêu chí kết cục “cứng” (live birth), cần đa trung tâm để giảm thiên lệch vận hành, và cần theo dõi an toàn trẻ sinh ra [1].
-
- Lộ trình pháp lý và quản trị chất lượng: “khác quốc gia, khác chuẩn dữ liệu”
Xác nhận lâm sàng là điều kiện then chốt để được phê duyệt sử dụng thiết bị y tế trong IVF. Các cơ quan quản lý như FDA (Hoa Kỳ), EMA (châu Âu), MHRA (Vương quốc Anh), NMPA (Trung Quốc) và CDSCO (Ấn Độ) đặt ra các yêu cầu khác nhau về dữ liệu lâm sàng, thiết kế thử nghiệm và tiêu chuẩn chất lượng [7].
Tại châu Âu, theo Quy định thiết bị y tế MDR (2017/745), các thiết bị lớp IIa–IIb (ví dụ hệ thống chọn lọc tinh trùng hoặc nuôi cấy phôi) có thể dựa vào dữ liệu thực tế hoặc tổng quan hệ thống, trong khi thiết bị lớp III bắt buộc phải có thử nghiệm lâm sàng quy mô lớn. Tại Hoa Kỳ, quy trình 510(k) cho phép phê duyệt dựa trên thiết bị tương đương, nhưng các thiết bị nguy cơ cao phải trải qua quy trình xác thực trước khi đưa ra thị trường (Premarket Approval – PMA) với dữ liệu an toàn và hiệu quả đầy đủ [7].
Sự khác biệt giữa các khu vực pháp lý dẫn đến yêu cầu thử nghiệm lâm sàng lặp lại, làm tăng chi phí và kéo dài thời gian phê duyệt. Thời gian trung bình để phê duyệt thiết bị y tế trong IVF dao động từ 6 đến 36 tháng, tùy khu vực và mức độ rủi ro, trong đó Trung Quốc và Ấn Độ thường yêu cầu thử nghiệm lâm sàng tại địa phương ngay cả khi thiết bị đã được phê duyệt bởi FDA (Food and Drug Administration) hoặc CE(Clinical Evaluation).
3.3. Rào cản thiết kế thử nghiệm lâm sàng trong IVF
Thử nghiệm lâm sàng là điều kiện then chốt để chứng minh ưu thế của công nghệ vi lưu so với quy trình IVF truyền thống, nhưng việc thiết kế nghiên cứu gặp nhiều thách thức. Các tiêu chí lâm sàng quan trọng như tỷ lệ thụ tinh, tỷ lệ tạo phôi nang, thai lâm sàng và trẻ sinh sống yêu cầu cỡ mẫu lớn và thời gian theo dõi dài, làm tăng chi phí nghiên cứu. Ngoài ra, sự khác biệt về đặc điểm bệnh nhân, quy trình phòng thí nghiệm và kinh nghiệm chuyên viên phôi học giữa các trung tâm tạo ra sự không đồng nhất dữ liệu và khó khăn trong chuẩn hóa kết quả [7]. Ngoài ra, yêu cầu dữ liệu an toàn dài hạn, đặc biệt liên quan đến kết cục thai kỳ và sức khỏe trẻ sinh ra, tiếp tục là rào cản lớn đối với phê duyệt lâm sàng.
- Định hướng phát triển và triển vọng ứng dụng của công nghệ vi lưu trong IVF
Những năm gần đây, vai trò của công nghệ vi lưu trong IVF đang dịch chuyển từ các thiết bị đơn chức năng sang nền tảng tích hợp đa mô-đun, nhằm hỗ trợ đồng thời xử lý giao tử, nuôi cấy phôi và đánh giá không xâm lấn. Các tổng quan gần đây nhấn mạnh rằng giá trị cốt lõi của vi lưu không chỉ nằm ở khả năng cải thiện một bước riêng lẻ trong quy trình IVF, mà ở tiềm năng chuẩn hóa vi môi trường sinh học và giảm phụ thuộc vào thao tác thủ công trong toàn bộ chu trình điều trị [9].
Một xu hướng nổi bật là tích hợp vi lưu với các hệ thống phân tích dữ liệu nâng cao, đặc biệt là trí tuệ nhân tạo (AI) và theo dõi phôi time-lapse. Vi lưu cho phép thu thập dữ liệu động học và chuyển hóa trong thể tích nuôi cấy cực nhỏ, tạo nền tảng dữ liệu phong phú cho các thuật toán AI dự đoán tiềm năng phát triển và làm tổ của phôi. Cách tiếp cận này được xem là bước chuyển từ đánh giá hình thái học đơn thuần sang mô hình đánh giá phôi đa tham số, không xâm lấn và mang tính cá thể hóa cao [15].
Bên cạnh đó, sự kết hợp giữa vi lưu và in sinh học 3D đang mở ra khả năng tái tạo các cấu trúc mô sinh sản và gradient sinh lý phức tạp, hướng tới mô hình “IVF-on-a-chip”. Các nền tảng này được kỳ vọng hỗ trợ nghiên cứu cơ chế sinh học phôi sớm, sàng lọc môi trường nuôi cấy và tối ưu hóa điều kiện can thiệp trước khi triển khai lâm sàng [6]. Tuy nhiên, phần lớn các ứng dụng này hiện vẫn ở giai đoạn tiền lâm sàng.
Từ góc độ thực hành, nhiều tác giả cho rằng công nghệ vi lưu có khả năng được triển khai sớm nhất trong các quy trình có mức độ nhạy cảm sinh học thấp hơn, như xử lý tinh trùng và một phần nuôi cấy phôi, trước khi mở rộng sang xử lý noãn và phôi giai đoạn sớm. Việc định vị vi lưu như công cụ hỗ trợ chuẩn hóa và tự động hóa, thay vì thay thế hoàn toàn các quy trình hiện hành, được xem là chiến lược phù hợp để thúc đẩy ứng dụng lâm sàng trong ngắn và trung hạn.
- Kết luận
Công nghệ vi lưu đại diện cho một hướng tiếp cận đầy tiềm năng nhằm chuẩn hóa và tự động hóa quy trình IVF, đặc biệt trong xử lý tinh trùng và nuôi cấy phôi. Tuy nhiên, phần lớn ứng dụng hiện nay vẫn dựa trên bằng chứng tiền lâm sàng hoặc dữ liệu hồi cứu. Việc chuyển giao thành công vào thực hành lâm sàng đòi hỏi các thử nghiệm ngẫu nhiên đa trung tâm, đánh giá kết cục dài hạn và chiến lược tích hợp công nghệ phù hợp với điều kiện thực tế của phòng lab IVF.
Nguồn tham khảo
1. Pensabene, V., Agate, F., Santos Miranda, A., & Picton, H. M. (2025). Microfluidics for in vitro fertilization: From science to clinical validation. Human Reproduction Update, dmaf028. https://doi.org/10.1093/humupd/dmaf028
2. Simchi, M., Riordon, J., You, J. B., Wang, Y., Xiao, S., Lagunov, A., Hannam, T., Jarvi, K., Nosrati, R., & Sinton, D. (2021). Selection of high-quality sperm with thousands of parallel channels. Lab on a Chip, 21(12), 2464–2475. https://doi.org/10.1039/d0lc01182g
3. Ghassemi Panah, A., Zabetian Targhi, M., Heydari, A., & Halvaei, I. (2022). A novel microfluidic system to separate sperm using spermatozoa inherent motion and inertial effect. Journal of Biomechanics, 142, 111256. https://doi.org/10.1016/j.jbiomech.2022.111256
4. Jeon, H., Cremers, C., Le, D., Abell, J., & Han, J. (2022). Multi-dimensional-double-spiral (MDDS) inertial microfluidic platform for sperm isolation directly from the raw semen sample. Scientific Reports, 12(1), 4212. https://doi.org/10.1038/s41598-022-08042-1
5. Ma, J., Xie, Q., Zhang, Y., Xiao, Q., Liu, X., Qiao, C., & Tian, Y. (2024). Advances in microfluidic technology for sperm screening and in vitro fertilization. Analytical and Bioanalytical Chemistry, 416(16), 3717–3735. https://doi.org/10.1007/s00216-023-05120-9
6. Weng, L., Lee, G. Y., Liu, J., Kapur, R., Toth, T. L., & Toner, M. (2018). On-chip oocyte denudation from cumulus-oocyte complexes for assisted reproductive therapy. Lab on a Chip, 18(24), 3892–3902. https://doi.org/10.1039/c8lc01075g
7. Pensabene, V., Agate, F., Santos Miranda, A., & Picton, H. M. (n.d.). Microfluidics for in vitro fertilization: From science to clinical validation. Retrieved January 22, 2026, from https://dx.doi.org/10.1093/humupd/dmaf028
8. Heo, Y. S., Cabrera, L. M., Bormann, C. L., Shah, C. T., Takayama, S., & Smith, G. D. (2010). Dynamic microfunnel culture enhances mouse embryo development and pregnancy rates. Human Reproduction (Oxford, England), 25(3), 613–622. https://doi.org/10.1093/humrep/dep449
9. Alegretti, J. R., Rocha, A. M. D., Nogueira-de-Souza, N. C., Kato, N., Barros, B. C., Motta, E. L. A., Serafini, P. C., Takayama, S., & Smith, G. D. (2024). Controlled Dynamic Microfluidic Culture of Murine, Bovine, and Human Embryos Improves Development: Proof-of-Concept Studies. Cells, 13(24), 2080. https://doi.org/10.3390/cells13242080
10. Guo, Y., Yang, Y., Yi, X., & Zhou, X. (2019). Microfluidic method reduces osmotic stress injury to oocytes during cryoprotectant addition and removal processes in porcine oocytes. Cryobiology, 90, 63–70. https://doi.org/10.1016/j.cryobiol.2019.08.005
11. Gatimel, N., Moreau, J., Bettiol, C., Parinaud, J., & Léandri, R. D. (2021). Semi-automated versus manual embryo vitrification: Inter-operator variability, time-saving, and clinical outcomes. Journal of Assisted Reproduction and Genetics, 38(12), 3213–3222. https://doi.org/10.1007/s10815-021-02346-3
12. Aziz, A. U. R., Fu, M., Deng, J., Geng, C., Luo, Y., Lin, B., Yu, X., & Liu, B. (2017). A Microfluidic Device for Culturing an Encapsulated Ovarian Follicle. Micromachines, 8(11), 335. https://doi.org/10.3390/mi8110335
13. Choi, J. K., Agarwal, P., Huang, H., Zhao, S., & He, X. (2014). The crucial role of mechanical heterogeneity in regulating follicle development and ovulation with engineered ovarian microtissue. Biomaterials, 35(19), 5122–5128. https://doi.org/10.1016/j.biomaterials.2014.03.028
14. Sadeghzadeh Oskouei, B., Pashaiasl, M., Heidari, M. H., Salehi, M., Veladi, H., Ghaderi Pakdel, F., Shahabi, P., & Novin, M. G. (2016). Evaluation of Mouse Oocyte In Vitro Maturation Developmental Competency in Dynamic Culture Systems by Design and Construction of A Lab on A Chip Device and Its Comparison with Conventional Culture System. Cell Journal, 18(2), 205–213. https://doi.org/10.22074/cellj.2016.4315
15. Olawade, D. B., Teke, J., Adeleye, K. K., Weerasinghe, K., Maidoki, M., & Clement David-Olawade, A. (2025). Artificial intelligence in in-vitro fertilization (IVF): A new era of precision and personalization in fertility treatments. Journal of Gynecology Obstetrics and Human Reproduction, 54(3), 102903. https://doi.org/10.1016/j.jogoh.2024.102903