CNSH. Phan Thị Thanh Loan - Bệnh viện đa khoa Mỹ Đức
Tế bào mầm nguyên thủy (Primordial Germ Cells - PGCs) là quần thể tế bào tiền thân duy nhất có chức năng bảo tồn và truyền đạt thông tin di truyền qua các thế hệ. Trong phôi thai học người, sự biệt hóa và di chuyển của PGCs là một tiến trình sinh học được kiểm soát chặt chẽ dưới sự phối hợp giữa yếu tố phân tử và tín hiệu từ vi môi trường. Việc giải mã các cơ chế phân tử điều phối sự phát triển của PGCs không chỉ có ý nghĩa trong việc xác định nguyên nhân gây ra các rối loạn sinh noãn, mà còn là tiền đề cho các chiến lược can thiệp vô sinh hiện đại. Đặc biệt, những hiểu biết về vi môi trường của PGCs đang mở ra triển vọng ứng dụng công nghệ tạo giao tử in vitro (In vitro gametogenesis - IVG) từ tế bào gốc vạn năng cảm ứng. Bài tổng quan này tập trung phân tích nguồn gốc, các yếu tố phân tử và hành trình di chuyển của PGCs trong quá trình sinh noãn, qua đó cung cấp cơ sở khoa học cho các ứng dụng trong y học tái tạo và hỗ trợ sinh sản tiên tiến.
- Nguồn gốc tế bào mầm nguyên thủy
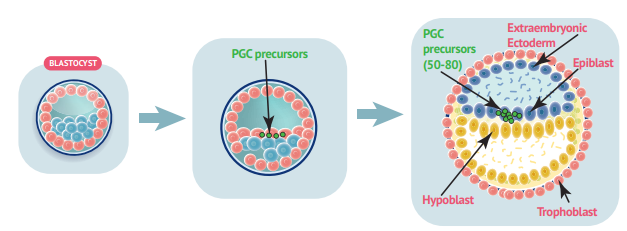
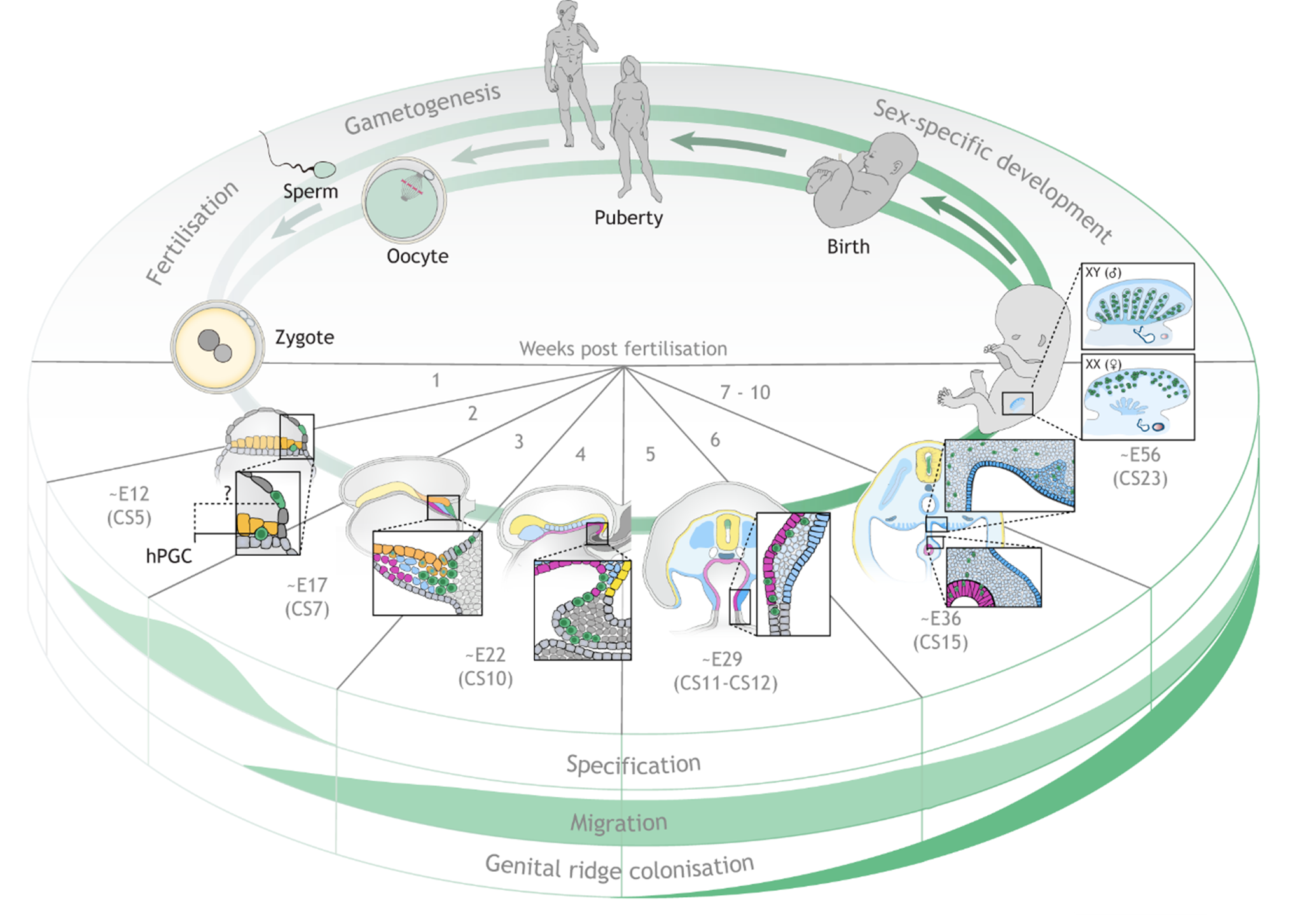
Hình 1. Nguồn gốc PGC [1]
Tế bào mầm nguyên thủy có nguồn gốc từ một nhóm nhỏ khoảng 50 - 80 tế bào tại thượng bì phôi (epiblast) vào tuần thứ 2 đến tuần thứ 3 của thai kỳ. Dưới tác động của các tín hiệu cảm ứng từ mô nhau thai sớm và trung bì ngoài phôi, đặc biệt là các protein thuộc họ BMP (BMP4, BMP8b), một quần thể tế bào từ thượng bì phôi được biệt hóa thành PGCs. Các tín hiệu này khởi động chương trình phiên mã đặc hiệu của dòng mầm thông qua sự hoạt hóa các yếu tố BLIMP1 (PRDM1), PRDM14, TFAP2C và SOX17 đồng thời ức chế các chương trình biệt hóa soma [2, 3].
- Quá trình di chuyển tế bào mầm nguyên thủy ở giai đoạn phôi thai
Hành trình PGCs di chuyển đến gờ sinh dục là một quá trình phức tạp, bao gồm hai giai đoạn: di chuyển thụ động và di chuyển chủ động. Trong giai đoạn phát triển sớm của phôi (tuần thứ 3 - 4), PGCs di chuyển một cách thụ động do các biến đổi hình thái của phôi, đặc biệt là quá trình gấp nếp của đĩa phôi. Sự tái sắp xếp cấu trúc này đưa PGCs từ thượng bì phôi đến định cư tạm thời tại nội bì của ruột giữa và ruột sau nguyên thủy. Bước sang tuần thứ 5, quần thể PGCs chuyển sang di chuyển chủ động bằng kiểu vận động kiểu amíp (amoeboid movement). Đặc trưng bởi sự hình thành các giả túc (filopodia/lamellipodia) giàu actin, PGCs có khả năng xuyên qua các lớp mô của mạc treo ruột, di chuyển dọc theo vùng trung thận và cuối cùng xâm nhập vào gờ sinh dục vào khoảng tuần thứ 6.
Sự chính xác của quá trình di cư này được điều hòa bởi mạng lưới tín hiệu SDF1 (CXCL12) - CXCR4 và SCF/c-KIT, cùng sự tương tác với các thành phần của chất nền ngoại bào như fibronectin và laminin tạo nên giá đỡ phân tử hỗ trợ sự bám dính, định hướng và di chuyển của PGCs [4]. Ở giai đoạn sớm, các tế bào này chủ yếu sử dụng chuyển hóa yếm khí, đi kèm với số lượng ty thể tương đối thấp. Sau khi định cư tại gờ sinh dục, PGCs chuyển sang chuyển hóa hiếu khí mạnh mẽ, đồng thời mật độ ty thể trong tế bào tăng lên đáng kể để đáp ứng nhu cầu năng lượng cao cho quá trình biệt hóa và phát triển [4]. Song song với những biến đổi chuyển hóa, PGCs còn trải qua quá trình khử methyl hóa DNA trên diện rộng, nhằm xóa bỏ các dấu ấn di truyền (genomic imprinting), khôi phục tính toàn năng (totipotency) cho thế hệ sau [5, 6].
Ngoài các tín hiệu hóa hướng động, yếu tố cơ sinh học (biomechanics) cũng đóng vai trò quan trọng trong sự di chuyển của PGCs [7]. Các nghiên cứu thực nghiệm trên mô hình tế bào di cư cho thấy rằng khi tế bào di chuyển xuyên qua các cấu trúc mô có kích thước hạn chế, sự biến dạng cơ học của nhân có thể xảy ra. Hiện tượng này dẫn đến rò rỉ màng nhân và tổn thương DNA, buộc tế bào phải kích hoạt các cơ chế sửa chữa DNA tức thời để duy trì tính toàn vẹn của bộ gene. Cơ chế bảo vệ này có ý nghĩa đặc biệt quan trọng đối với PGCs, bởi đây là dòng tế bào chịu trách nhiệm truyền thông tin di truyền cho thế hệ sau [7, 8].
- Định cư và biệt hóa tại gờ sinh dục
Sau khi hoàn tất di cư, PGCs định cư tại gờ sinh dục và chịu sự chi phối của vi môi trường đặc hiệu (germline niche). Tại đây, sự hoạt hóa trục WNT/β-catenin (thông qua WNT4, RSPO1) đóng vai trò trung tâm trong việc tắt chương trình duy trì tính vạn năng, thông qua ức chế phiên mã các gene như OCT4 (POU5F1) và NANOG [9]. Quá trình này được xem như bước “cấp phép”, cho phép PGCs thoát khỏi trạng thái chưa biệt hóa; nếu thiếu tín hiệu này, các tế bào sẽ duy trì đặc tính vạn năng và không thể nguyên phân chuyển thành nguyên bào noãn. Đồng thời, các cytokine thuộc họ TGF-β, bao gồm BMP2 và Activin A do mô đệm của gờ sinh dục tiết ra, đóng vai trò điều hòa sự biệt hóa. BMP2 thúc đẩy PGCs chuyển sang trạng thái tế bào có khả năng biệt hóa tạo giao tử (gametogenesis-competent cells), trong khi Activin A hỗ trợ chuyển đổi chuyển hóa và chuẩn bị cho tế bào bước vào quá trình giảm phân.
Từ khoảng tuần thứ 8, dưới tác động cảm ứng của acid retinoic (RA) có nguồn gốc từ trung thận, các nguyên bào noãn bắt đầu khởi phát chương trình giảm phân thông qua hoạt hóa gene STRA8 [10]. Đây là dấu ấn phân tử đặc hiệu đánh dấu sự kết thúc hoàn toàn của chương trình PGCs và chuyển sang giai đoạn sinh giao tử.
Đến khoảng tuần thứ 20, số lượng nguyên bào noãn đạt khoảng 7 triệu. Từ tháng thứ 5 của thai kỳ trở đi, quá trình chết theo chương trình (apoptosis) diễn ra mạnh mẽ đối với các tế bào không tham gia giảm phân, dẫn đến sự suy giảm đáng kể quần thể tế bào mầm. Các tế bào đã bước vào giảm phân sẽ dừng ở kỳ trước giảm phân I, đồng thời thiết lập tương tác chặt chẽ với các tế bào tiền hạt để hình thành nang noãn nguyên thủy, đặt nền tảng cho dự trữ noãn sau sinh.
Tóm lại, quá trình định cư và biệt hóa tại gờ sinh dục là một chuỗi sự kiện phát triển liên tục, được điều hòa bởi nhiều yếu tố, trong đó các tín hiệu phân tử đặc hiệu theo thời gian định hướng chính xác các biến đổi, đảm bảo sự chuyển đổi trạng thái vạn năng sang dòng tế bào mầm biệt hóa, đồng thời xác lập dự trữ noãn hữu hạn ngay từ giai đoạn phôi thai.
- Ý nghĩa lâm sàng và ứng dụng
Việc nghiên cứu hành trình di chuyển của tế bào mầm nguyên thủy (PGCs) trong phôi thai, cùng với các yếu tố và cơ chế điều hòa liên quan, cung cấp nền tảng quan trọng để giải thích căn nguyên của các bệnh lý sinh sản và định hướng cho các chiến lược điều trị. Cụ thể:
- Căn nguyên bệnh lý khối u và suy giảm dự trữ buồng trứng
Sự thất bại trong cơ chế apoptosis đối với các PGCs lạc chỗ chính là nguồn gốc trực tiếp của các khối u tế bào mầm ngoài tuyến sinh dục (Extragonadal Germ Cell Tumors). Điển hình là u quái (Teratoma) vùng xương cùng cụt, trung thất hoặc nội sọ, mang đặc điểm mô học đa dạng từ cả ba lá thai do tính vạn năng chưa được biệt hóa của PGCs [7]. Song song đó, các đột biến ở gene điều hướng như CXCR4 hoặc hệ thống thụ thể c-Kit làm giảm tín hiệu hóa hướng động của PGCs đến gờ sinh dục, dẫn đến sụt giảm nghiêm trọng của quần thể noãn bào vào tuần thứ 20. Đây là một trong số tiền đề di truyền quan trọng giải thích tình trạng suy buồng trứng sớm (Premature Ovarian Insufficiency - POI) và mãn kinh sớm ở phụ nữ trẻ tuổi.
- Giả thuyết "Dây chuyền sản xuất - production line hypothesis" và chất lượng giao tử
Lý thuyết về các PGCs "tiên phong" (pioneer cells) - những tế bào thoát khỏi vi môi trường ức chế sớm nhất và định cư tại các vị trí ưu tiên ở gờ sinh dục cung cấp một góc nhìn mới về chất lượng noãn bào. Theo giả thuyết "Dây chuyền sản xuất" (Production line hypothesis), những tế bào mầm tiên phong này thường là nhóm đầu tiên bước vào giảm phân và hình thành nang noãn nguyên thủy, từ đó có xu hướng được chiêu mộ và rụng trứng đầu tiên [7]. Điều này gợi ý rằng tính ổn định di truyền của PGCs trong giai đoạn phôi thai có mối liên hệ mật thiết đến chất lượng giao tử ở những năm đầu của độ tuổi sinh sản.
- Tạo giao tử in vitro
Ứng dụng thực tiễn đột phá nhất hiện nay là việc mô phỏng quá trình di cư và biệt hóa PGCs trong môi trường nhân tạo. Dựa trên các tín hiệu điều phối như WNT4, BMP2 và Acid Retinoic, các nhà khoa học đang nỗ lực phát triển công nghệ IVG từ tế bào gốc vạn năng cảm ứng (iPSCs). Thành công của kỹ thuật này hứa hẹn tạo cơ hội cho những bệnh nhân không có trứng tự thân do điều trị ung thư, bất thường di truyền hoặc suy buồng trứng sớm, bằng cách tạo ra các noãn bào có nguồn gốc di truyền tự thân từ tế bào soma, mở ra một chương mới cho y học tái tạo trong lĩnh vực hỗ trợ sinh sản.
Quá trình hình thành và di chuyển của PGCs là một tiến trình sinh học phức tạp, được điều hòa nghiêm ngặt bởi mạng lưới tín hiệu phân tử và tương tác vi môi trường. Sự chuyển đổi từ trạng thái vạn năng sang khả năng sinh giao tử tại gờ sinh dục không chỉ đánh dấu bước ngoặt về mặt hình thái mà còn là sự tái lập trình biểu sinh sâu sắc để bảo tồn thông tin di truyền qua các thế hệ.
Bất kỳ rối loạn nào trong hành trình di cư hoặc tại gờ sinh dục đều dẫn đến các hệ quả bệnh lý nghiêm trọng như u tế bào mầm lạc chỗ hoặc suy giảm dự trữ buồng trứng sớm (POI). Việc nắm rõ các nguyên lý điều hòa PGCs chính là chìa khóa để tối ưu hóa các kỹ thuật hỗ trợ sinh sản hiện đại, đặc biệt là tiềm năng tái tạo noãn bào tự thân thông qua công nghệ IVG. Những hiểu biết này không chỉ làm sáng tỏ căn nguyên vô sinh mà còn mở ra hướng đi mới trong y học tái tạo và điều trị bảo tồn sinh sản trong tương lai.
Tài liệu tham khảo:
[1] Development of Reproductive Systems at the Embryo Stage. (2021). In A Textbook of Clinical Embryology (pp. 3–7). Cambridge University Press.
[2] Johnson, M. H. (2018). Essential reproduction. John Wiley & Sons.
[3] Hancock, G. V., Wamaitha, S. E., Peretz, L., & Clark, A. T. (2021). Mammalian primordial germ cell specification. Development, 148(6), dev189217.
[4] De Felici, M. (2012). Origin, migration, and proliferation of human primordial germ cells. In Oogenesis (pp. 19-37). London: Springer London.
[5] Goodwin, K., Emrich, T. A., Arnold, S., & McDole, K. (2025). Primordial germ cells experience increasing physical confinement and DNA damage during migration in the mouse embryo. BioRxiv, 2025-03.
[6] Ramakrishna, N. B., Alves-Lopes, J. P., & Gruhn, W. H. (2025). Emerging principles and models of human primordial germ cell development. Development, 152(17), dev204968.
[7] Cantú, A. V., & Laird, D. J. (2017). A pilgrim's progress: Seeking meaning in primordial germ cell migration. Stem cell research, 24, 181-187.
[8] Raab, M., Gentili, M., de Belly, H., Thiam, H. R., Vargas, P., Jimenez, A. J., ... & Piel, M. (2016). ESCRT III repairs nuclear envelope ruptures during cell migration to limit DNA damage and cell death. Science, 352(6283), 359-362.
[9] Le Rolle, M., Massa, F., Siggers, P., Turchi, L., Loubat, A., Koo, B. K., ... & Chassot, A. A. (2021). Arrest of WNT/β-catenin signaling enables the transition from pluripotent to differentiated germ cells in mouse ovaries. Proceedings of the National Academy of Sciences, 118(30), e2023376118.
[10] Sánchez, F., & Smitz, J. (2012). Molecular control of oogenesis. Biochimica et Biophysica Acta (BBA)-Molecular Basis of Disease, 1822(12), 1896-1912.