CVPH Cao Vân Anh, CVPH Ngô Thị Lan Phương
Đơn vị HTSS IVFMD FAMILY, BVĐK Gia Đình, Đà Nẵng
1. Giới thiệu
Trong các bệnh lý như hội chứng buồng trứng đa nang (polycystic ovary syndrome-PCOS) và lạc nội mạc tử cung (LNMTC), chất lượng và số lượng noãn có khả năng bị suy giảm, làm hạn chế khả năng thụ tinh và tiềm năng phát triển phôi. Điều này đã thúc đẩy nhiều nghiên cứu nhằm làm sáng tỏ các cơ chế sinh học nền tảng và phát triển các chiến lược điều trị hiệu quả.
Gần đây, có nhiều nghiên cứu ghi nhận túi ngoại bào (extracellular vesicles-EVs) là thành phần quan trọng trong giao tiếp giữa các tế bào. EVs bao gồm exosomes và microvesicles, mang theo nhiều phân tử hoạt tính sinh học (bao gồm axit nucleic, protein, lipid và chất chuyển hóa) và tham gia điều hòa các quá trình sinh lý cũng như bệnh lý của noãn. Nhờ khả năng vận chuyển phân tử hiệu quả, EVs được xem như những tác nhân điều trị đầy triển vọng. Tuy nhiên, các nghiên cứu về vai trò của EVs đối với noãn vẫn còn hạn chế. Do đó, bài viết này nhằm làm rõ vai trò của EVs trong noãn, đồng thời cập nhật tiềm năng ứng dụng EVs trong cải thiện chất lượng noãn và điều trị các bệnh lý buồng trứng.
2. Thành phần và nguồn gốc của EVs trong cơ quan sinh sản nữ
Ở động vật có vú, buồng trứng là cơ quan sinh sản đảm nhiệm chức năng sản xuất giao tử cái, hay còn gọi là noãn bào. Cơ quan này chứa số lượng lớn nang noãn, là các đơn vị chức năng phụ trách sự phát triển và trưởng thành của noãn. Trong mỗi nang, noãn được bao bọc bởi nhiều lớp cấu trúc bảo vệ: lớp ngoài cùng là zona pellucida-một lớp giàu glycoprotein có vai trò kiểm soát sự xâm nhập của tinh trùng cũng như sự trao đổi của nhiều phân tử khác. Bao quanh noãn còn có các lớp tế bào soma chuyên biệt, gồm tế bào cumulus, tế bào hạt và tế bào vỏ. Những lớp tế bào này cấu thành thành nang, bao bọc khoang nang chứa dịch nang noãn [1].
EVs là các túi màng tự nhiên có nguồn gốc từ tế bào, giữ vai trò trung gian trong giao tiếp liên bào. Dựa trên kích thước và nguồn gốc sinh học, EVs được chia thành ba nhóm chính: exosome (30–150 nm, có nguồn gốc từ endosome), microvesicles (100–1000 nm, nảy chồi từ màng tế bào) và thể apoptotic (1–5 µm, hình thành trong quá trình chết tế bào theo chương trình(apoptosis)). Trong khi exosome và microvesicles được tiết ra trong hoạt động sinh lý bình thường, thể apoptotic chỉ xuất hiện khi tế bào trải qua apoptosis (Hình 1) [2].
Về mặt phân tử, EVs mang theo nhiều “hàng hoá” sinh học (EVs-cargo) như lipid, protein, mRNA, miRNA và các acid nucleic khác, cho phép truyền tải tín hiệu giữa các tế bào [3]. Sau khi được tiết vào dịch nang, EVs được các tế bào đích như tế bào cumulus và tế bào hạt tiếp nhận thông qua cơ chế nhập bào hoặc ẩm bào, qua đó thiết lập mạng lưới giao tiếp liên bào ở khoảng cách xa [1].
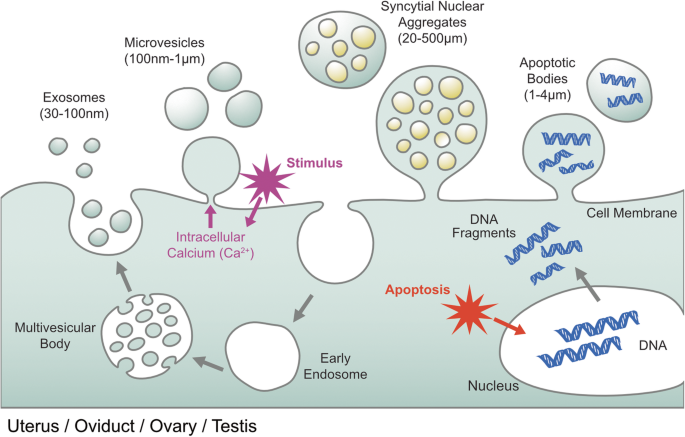
Hình 1. Phân loại EVs theo nguồn gốc và kích thước [2]
3. Vai trò của EVs trong sinh lý sinh sản nữ
3.1. Vai trò của EVs trong quá trình trưởng thành của noãn bào
Trong nang noãn, EVs góp phần thúc đẩy quá trình trưởng thành nhân và trưởng thành tế bào chất. EVs-cargo giàu các miRNA điều hòa những con đường tín hiệu quan trọng như ubiquitin–proteasome, WNT, MAPK (mitogen-activated protein kinase) và TGF-β (the transforming growth factor-beta) [3], [4]. Bên cạnh đó, EVs còn tham gia điều hòa chức năng ty thể, chuyển hóa năng lượng, biến đổi biểu sinh và kết dính tế bào-những yếu tố quyết định chất lượng noãn [5]. Lipid của EVs hoạt động như các chất truyền tin thứ cấp, trong khi mRNA của các gen chuỗi hô hấp ty thể trong EVs tương quan thuận với nồng độ FSH và LH, những hormone này thường tăng ở nang chứa noãn chất lượng tốt [6].
Bên cạnh vai trò chức năng, nhiều EV-miRNA được xem là dấu ấn sinh học đánh giá chất lượng noãn, như miR-132, miR-100, miR-99a, miR-218. Một số miRNA (miR-132, miR-212, miR-214) hỗ trợ tái khởi động giảm phân, trong khi miR-29a liên quan điều hòa biểu sinh. Ngoài ra, các miRNA như miR-31a-5p biến đổi theo tuổi, cho thấy tiềm năng làm chỉ dấu sinh học cho suy giảm chất lượng noãn do lão hóa [4].
3.2. Vai trò của EVs trong thụ tinh
Thụ tinh là một quá trình đa bước bao gồm hoạt hóa noãn, tinh trùng bám vào zona pellucida, phản ứng cực đầu, hòa màng giao tử và hình thành tiền nhân. Màng noãn trước thụ tinh biểu hiện các tetraspanin quan trọng như CD9 và CD81, giữ vai trò thiết yếu trong hòa màng tinh trùng-noãn. EVs giàu CD9 được giải phóng từ noãn vào khoang quanh noãn, tạo điều kiện thuận lợi cho sự hợp nhất tinh trùng-noãn bào bằng cách chuyển CD9 đến màng tinh trùng. Noãn bào thiếu CD9 cho thấy những bất thường trong vi nhung mao của chúng và không thể hợp nhất với tinh trùng. CD81, chủ yếu có nguồn gốc từ tế bào cumulus, hiện diện trong zona pellucida và tham gia các giai đoạn tiền hòa màng. Sự biểu hiện bất thường các protein này có thể làm suy giảm khả năng thụ tinh.
Ngoài protein, EVs còn vận chuyển miRNA điều hòa thụ tinh. Một số EVs nguồn gốc ống dẫn trứng có thể được tinh trùng tiếp nhận và chuyển tải các phân tử điều hòa, trong đó có miR-34c-5p được ghi nhận cần thiết cho lần phân chia đầu tiên của hợp tử. Một số miRNA trong dịch nang như miR-92a và miR-130b tăng ở các trường hợp không thụ tinh, cho thấy tiềm năng trong dự báo kết quả thụ tinh, tuy nhiên cơ chế điều hòa chi tiết vẫn cần nghiên cứu thêm [4].
3.3. Vai trò của EVs trong sự phát triển phôi và quá trình làm tổ
Sự khởi phát thai kỳ là quá trình phức tạp, đòi hỏi sự phối hợp nhịp nhàng giữa phôi và nội mạc tử cung (NMTC) trong suốt giai đoạn làm tổ và phát triển nhau thai sớm. Các yếu tố tiết từ NMTC trong dịch tử cung có thể điều hòa phát triển phôi, khả năng bám dính biểu mô và tính tiếp nhận nội mạc. Trong đó, EVs do nguyên bào nuôi và NMTC tiết ra rất quan trọng trong việc thúc đẩy tương tác giữa các tế bào tại điểm nối mẹ-thai nhi trong giai đoạn đầu thai kỳ [4].
Trên các nghiên cứu in vitro ở mô hình động vật, khi bổ sung vào hệ nuôi cấy phôi EVs từ đường sinh dục nữ có thể thay biểu hiện phiên mã của phôi, cải thiện khả năng phát triển, tăng tỷ lệ phôi nang, giảm apoptosis và nâng cao chất lượng của phôi [7],[8]. Đồng thời, phôi cũng hấp thu EVs từ ống dẫn trứng và NMTC, trong khi EVs nguồn gốc phôi cũng có thể điều hòa ngược lại chức năng tử cung và ống dẫn trứng [9].
Trong dịch tử cung, EVs thúc đẩy tăng sinh, tăng bám dính và xâm lấn của nguyên bào nuôi. Nhiều miRNA EVs tham gia trực tiếp vào quá trình làm tổ như miR-92b-3p- điều hòa tăng sinh, di chuyển nguyên bào nuôi, miR-30d, miR-200c- điều hòa biểu hiện gen làm tổ- và miR-17/92, miR-1290-điều hòa xâm lấn nguyên bào nuôi và tính tiếp nhận nội mạc. Một số miRNA khác như miR-26b, miR-98 góp phần điều hòa dung nạp miễn dịch của mẹ. EVs nguồn gốc phôi còn mang interferon giúp điều hòa gen làm tổ và tổng hợp progesterone. Ngoài ra, EVs trong dịch tử cung có thể vận chuyển RNA retrovirus nội sinh giữa nguyên bào nuôi và nội mạc, thúc đẩy phát triển nhau thai và tái cấu trúc mô. Nhìn chung, EVs phối hợp với hormone và yếu tố tăng trưởng để tạo mạng lưới tín hiệu phức tạp điều hòa làm tổ. Các miRNA đặc hiệu trong EVs còn có tiềm năng trở thành dấu ấn sinh học đánh giá khả năng tiếp nhận nội mạc và tiên lượng khả năng làm tổ của phôi [4].
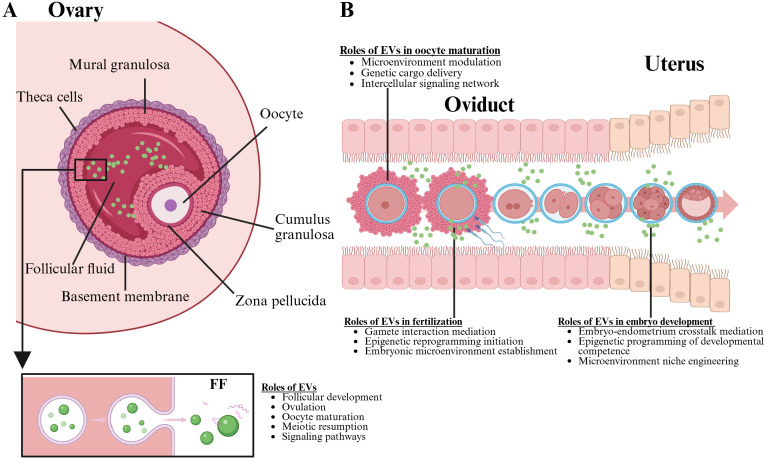
Hình 2. Vai trò của các EVs trong hệ thống sinh sản nữ [4].
Chú thích: Phần A mô tả buồng trứng, thể hiện quá trình hình thành noãn bào và chức năng của EVs trong dịch nang noãn, bao gồm thúc đẩy sự trưởng thành của noãn bào và tăng cường khả năng sinh sản. Phần B minh họa ống dẫn trứng, mô tả chi tiết tầm quan trọng của EVs đối với sự trưởng thành của noãn bào, khả năng sinh sản và sự phát triển phôi sớm.
4. Mối liên hệ giữa sự thay đổi của EVs và suy giảm chất lượng noãn trong các tình trạng bệnh lý
4.1. Sự thay đổi EVs trong PCOS
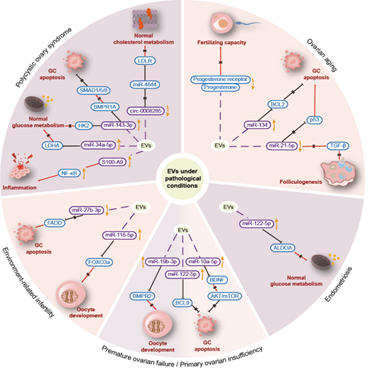
Do rối loạn tín hiệu trong quá trình hình thành nang noãn, chất lượng noãn ở bệnh nhân PCOS thường kém, từ đó ảnh hưởng bất lợi đến hiện tượng phóng noãn bình thường và chất lượng phôi thai. Ở nhóm bệnh nhân này, EVs trong dịch nang noãn bị biến đổi cả về thành phần phân tử và chức năng sinh học, góp phần làm suy giảm chất lượng noãn. EVs từ bệnh nhân PCOS có thể gây rối loạn phân bố ty thể và thoi vô sắc của noãn, đồng thời làm mất cân bằng môi trường vi mô nang noãn thông qua ba cơ chế chính:
(i) Rối loạn sinh tổng hợp steroid
(ii) Thúc đẩy apoptosis của tế bào hạt, làm cản trở sự phát triển nang và phóng noãn
(iii) Rối loạn chuyển hóa năng lượng, đặc biệt là ức chế đường phân của tế bào hạt thông qua các miRNA như miR-143-3p và miR-34a-5p
Ngoài ra, EVs còn góp phần thúc đẩy phản ứng viêm trong nang noãn thông qua việc vận chuyển các phân tử tiền viêm, hoạt hóa trục tín hiệu NF-κB [10]. Những phát hiện này không chỉ làm sáng tỏ các cơ chế phân tử gây suy giảm chất lượng noãn ở bệnh nhân PCOS mà còn cung cấp những cơ sở mới cho chẩn đoán PCOS.
4.2. Sự thay đổi của EVs trong quá trình lão hóa buồng trứng
Sự suy giảm chất lượng noãn và thất bại thụ tinh liên quan đến tình trạng vô sinh ở phụ nữ lớn tuổi. Các nghiên cứu cho thấy miRNA trong EVs dịch nang noãn thay đổi theo tuổi, với xu hướng tăng các tín hiệu thúc đẩy apoptosis và giảm các tín hiệu bảo vệ nang. Cụ thể, miR-134 tăng biểu hiện và được dự đoán nhắm vào BCL2, một yếu tố chống apoptosis trong việc duy trì khả năng sống còn của tế bào nang noãn. Song song đó, miR-21-5p giảm biểu hiện làm suy yếu vai trò điều hòa bảo vệ của nó đối với các trục tín hiệu p53 và TGF-β, vốn đóng vai trò trung tâm trong việc kiểm soát cân bằng giữa tăng sinh, biệt hóa và chết tế bào theo chương trình. Sự mất cân bằng phối hợp này dẫn đến tăng hoạt hóa các tín hiệu gây apoptosis, từ đó gây rối loạn quá trình hình thành, phát triển và duy trì nang noãn, cuối cùng góp phần làm suy giảm chất lượng noãn [11].
Đáng chú ý, cơ chế này có thể hình thành vòng phản hồi dương, trong đó sự hoạt hóa của p53 thúc đẩy giải phóng các EVs nhỏ giàu CD81, qua đó khuếch đại tín hiệu gây apoptosis trong tế bào hạt. Ngoài ra, hàm lượng progesterone và thụ thể của hormone này trong EVs dịch nang noãn giảm theo tuổi, có thể liên quan đến khả năng thụ tinh giảm. Tuy nhiên, hầu hết các bằng chứng hiện nay mang tính quan sát, và ý nghĩa chức năng trực tiếp của các thay đổi EVs-cargo trong lão hóa buồng trứng vẫn cần được xác nhận thêm bằng các nghiên cứu thực nghiệm [12].
4.3. Sự thay đổi EVs ở bệnh nhân LNMTC
LNMTC liên quan chặt chẽ đến suy giảm chất lượng noãn và giảm khả năng sinh sản. Bên cạnh tác động cơ học và viêm mạn tính vùng chậu, các bằng chứng gần đây cho thấy EVs đóng vai trò trung gian quan trọng trong rối loạn chức năng noãn. Việc quá tải sắt do hiện tượng kinh nguyệt và xuất huyết định kỳ từ các tổn thương lạc chỗ làm thay đổi đặc điểm EVs của tế bào hạt, từ đó tác động bất lợi lên noãn thông qua rối loạn các con đường tín hiệu như MAPK, điều hòa chu kỳ tế bào, giảm phân và ferroptosis, dẫn đến ức chế sự trưởng thành noãn [13].
Bên cạnh đó, LNMTC làm ảnh hưởng đến chuyển hóa năng lượng trong nang noãn. Ở bệnh nhân LNMTC chưa điều trị, miR-122-5p-một microRNA có vai trò quan trọng trong điều hòa chuyển hóa năng lượng, stress oxy hóa và apoptosis-tăng biểu hiện trong các EVs của dịch nang noãn, dẫn đến ức chế aldolase A, một enzyme then chốt của quá trình đường phân. Sự ức chế này làm rối loạn chuyển hóa glucose ở tế bào cumulus, gây thiếu hụt năng lượng cung cấp cho noãn, từ đó làm suy giảm chất lượng và rối loạn quá trình trưởng thành noãn. Những phát hiện này góp phần làm sáng tỏ cơ chế gây rối loạn trưởng thành noãn ở bệnh nhân LNMTC [14].
4.4. Sự biến đổi của EVs trong suy buồng trứng
Suy buồng trứng sớm (Premature ovarian failure-POF) và suy buồng trứng nguyên phát (Primary ovarian insufficiency-POI) đều đặc trưng bởi suy giảm dự trữ nang noãn và giảm chất lượng noãn.
Bên cạnh các EVs có nguồn gốc tại chỗ từ buồng trứng, còn có bằng chứng cho thấy EVs lưu hành trong huyết tương, có khả năng vượt qua hàng rào máu-nang noãn cũng cho thấy tác động bệnh lý. Phân tích EVs huyết tương ở bệnh nhân POF cho thấy sự tăng biểu hiện của các miRNA ức chế các con đường quan trọng liên quan đến giảm phân noãn và tăng sinh tế bào, trong đó miR-19b-3p làm suy giảm hoạt tính BMPR2, một yếu tố thiết yếu cho sự trưởng thành noãn. Tương tự, miR-10a-5p trong EVs huyết tương của mô hình POF nhắm vào BDNF, ức chế trục AKT/mTOR và làm tăng apoptosis của tế bào hạt [15].
Gần đây, các nghiên cứu cũng ghi nhận rằng các thành viên khác của họ miR-10 có thể tham gia điều hòa sinh lý phóng noãn thông qua cùng đích tác động, cho thấy rằng hiệu ứng của EVs trong POF/POI phụ thuộc mạnh vào bối cảnh bệnh lý. Tuy nhiên, cơ chế mà các phân tử này phối hợp điều hòa chức năng và hoạt động của tế bào hạt vẫn chưa được làm rõ và cần tiếp tục nghiên cứu [16].
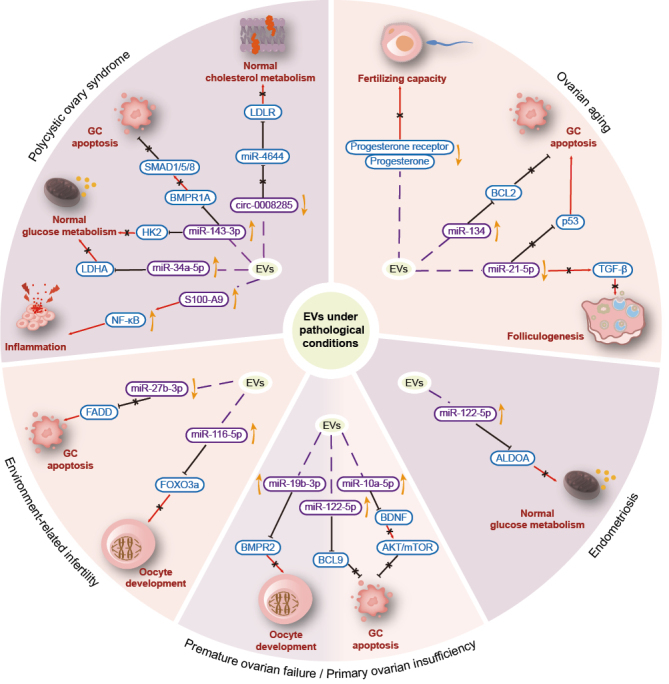
Hình 3. Tác động của EVs trong các rối loạn buồng trứng [3].
5. Tiềm năng ứng dụng EVs trong điều trị và hỗ trợ sinh sản
5.1. Nâng cao chất lượng noãn bào
Số lượng noãn ở động vật có vú được xác định trước sinh và suy giảm không hồi phục theo tuổi và các bệnh lý buồng trứng. Gần đây, EVs nổi lên như một chiến lược tiềm năng nhằm bảo vệ và cải thiện chất lượng quần thể noãn hữu hạn này. Exosome từ tế bào gốc trung mô dây rốn người (hucMSCs-Exos) có thể tích lũy trong nang nguyên thủy, mang các miRNA chức năng (miR-146a-5p, miR-21-5p) và hoạt hóa trục PI3K/mTOR, qua đó thúc đẩy hoạt hóa nang nguyên thủy. Ở chuột già, can thiệp này làm giảm stress oxy hóa và cải thiện hình thái thoi vô sắc của noãn, hiệu quả tương tự được ghi nhận trong các mô hình nuôi trưởng thành noãn in vitro [17].
Về cơ chế, EVs chủ yếu cải thiện chức năng ty thể và tính toàn vẹn bộ máy phân bào của noãn. Exosome từ tế bào gốc trung mô màng ối mang miR-320a điều hòa bất thường tín hiệu Sirtuin–OPA1, góp phần khôi phục động học ty thể. Đồng thời, EVs từ dịch nang noãn cung cấp các protein cấu trúc (ARP2/3, myosin, F-actin), giúp ổn định thoi vô sắc và tăng khả năng tái khởi động giảm phân của noãn sau thủy tinh hóa [18].
5.2. Hỗ trợ tế bào hạt
Noãn phụ thuộc chặt chẽ vào tế bào hạt (granulosa cells-GCs) để duy trì môi trường nội tiết và chuyển hóa tối ưu cho phát triển. Trong nhiều bệnh lý buồng trứng, apoptosis và rối loạn chức năng GCs là cơ chế trung tâm dẫn đến suy giảm chất lượng noãn, khiến GCs trở thành đích điều trị quan trọng của các chiến lược dựa trên EVs.
Các EVs điều trị, đặc biệt có nguồn gốc từ tế bào gốc trung mô, đã được chứng minh làm tăng tính sống còn của GCs thông qua điều hòa các trục tín hiệu chống apoptosis và stress tế bào. Nổi bật là khả năng tái cân bằng trục PI3K/AKT/p53, trong đó các miRNA chức năng (như miR-144-5p, miR-664-5p) làm giảm hoạt tính p53, tăng phosphoryl hóa AKT và bảo vệ GCs khỏi apoptosis do hóa trị hoặc suy buồng trứng [19].
Bên cạnh đó, EVs còn thúc đẩy tăng sinh và duy trì chức năng GCs thông qua điều hòa các con đường Notch và Hippo; việc ức chế MST1/2 và tăng tích lũy YAP trong nhân góp phần hỗ trợ hoạt hóa nang noãn. Trong bối cảnh viêm mạn tính của PCOS và POI, EVs điều trị cũng ức chế tín hiệu NF-κB và pyroptosis qua trục NLRP3, từ đó cải thiện vi môi trường buồng trứng [20].
Sự bảo vệ GCs đi kèm với phục hồi chức năng nội tiết, thể hiện qua giảm FSH/LH và tăng AMH, estradiol trong các mô hình suy buồng trứng. Hiệu quả này một phần đến từ khả năng EVs điều hòa trực tiếp quá trình sinh steroid ở GCs. Nhìn chung, EVs không chỉ bảo vệ GCs khỏi tổn thương mà còn tái lập chức năng nội tiết, qua đó hỗ trợ gián tiếp chất lượng noãn trong các điều kiện bệnh lý.
5.3. Điều hòa quá trình tạo mạch buồng trứng
Mạng lưới mạch máu buồng trứng cung cấp oxy, gonadotrophin và tiền chất steroid, đóng vai trò thiết yếu trong việc duy trì chất lượng noãn [21]. Rối loạn tạo mạch là đặc trưng của nhiều bệnh lý buồng trứng, và các EVs điều trị có khả năng điều chỉnh quá trình này theo bối cảnh sinh lý-bệnh lý.
Trong POF và POI, suy giảm tạo mạch và mất ổn định mạch máu là những đặc trưng bệnh lý điển hình [21]. hucMSCs-Exos mang miR-126-3p đã được chứng minh làm hoạt hóa trục PI3K/AKT/mTOR, tăng các yếu tố tạo mạch như VEGF, IGF-1 và angiogenin, đồng thời cải thiện độ trưởng thành mạch, thể hiện qua sự phục hồi bao phủ của tế bào α-SMA quanh nang [22].
Ngược lại, trong lạc nội mạc tử cung và PCOS, tạo mạch bệnh lý bị hoạt hóa quá mức. Ở lạc nội mạc, EVs từ đại thực bào M1 hoặc từ tế bào gốc trung mô nguồn máu kinh có thể làm giảm tín hiệu tiền tạo mạch, bao gồm VEGF, thông qua tái lập trình kiểu hình miễn dịch [23]. Trong PCOS, BMSCs-Exos làm giảm biểu hiện PECAM-1 nội mô, góp phần hạn chế tưới máu bệnh lý ở lớp vỏ buồng trứng [24].
Những dữ liệu này cho thấy EVs có khả năng điều hòa tạo mạch theo hướng “chuẩn hóa” thay vì chỉ tăng hoặc giảm, tuy nhiên việc xác định EVs-cargo tối ưu cho từng bối cảnh bệnh lý vẫn cần được làm rõ thêm.
5.4. Sảy thai liên tiếp
Sảy thai liên tiếp (Recurrent pregnancy loss -RPL) là một biến chứng trong thai kỳ, đặc trưng bởi cơ chế bệnh sinh phức tạp, trong đó các yếu tố miễn dịch đóng vai trò trọng tâm. Gần đây, chức năng điều hòa miễn dịch của EVs trong RPL đã thu hút sự chú ý đáng kể, duy trì sự cân bằng miễn dịch mẹ-thai nhi [15].
EVs có nguồn gốc từ màng rụng điều hòa biệt hóa và chức năng tế bào T thông qua vận chuyển các miRNA đặc hiệu, đồng thời ảnh hưởng đến hoạt hóa đại thực bào và tế bào tua, qua đó duy trì cân bằng viêm và thúc đẩy dung nạp miễn dịch thai kỳ. EVs từ tế bào gốc trung mô cho thấy tiềm năng điều trị rõ rệt: trong mô hình chuột RPL, EVs giúp làm tăng cytokine chống viêm (IL-4, IL-10), giảm yếu tố tiền viêm (TNF-α, IFN-γ), điều hòa chức năng tế bào T và phân cực đại thực bào, từ đó giảm tỷ lệ thất bại làm tổ.
Ngoài ra, EVs có nguồn gốc từ nhung mao có thể điều hòa hoạt tính tế bào NK màng rụng thông qua vận chuyển miR-29a-3p, mở ra hướng điều trị mới, đặc biệt khi kết hợp với vật liệu sinh học như HA-gel. Nhìn chung, điều hòa miễn dịch qua trung gian EVs mang lại triển vọng chẩn đoán và điều trị mới cho RPL, dù vẫn cần thêm nghiên cứu lâm sàng để xác nhận hiệu quả [4].
6. Kết luận
Hiện nay, các bằng chứng cho thấy EVs đóng vai trò trung tâm trong điều hòa động các quá trình sinh lý của noãn, đồng thời góp phần vào cơ chế bệnh sinh khi hệ thống EVs bị rối loạn trong các tình trạng bệnh lý buồng trứng. Trong những năm gần đây, nghiên cứu về EVs trong sinh noãn đã dịch chuyển từ mô tả hiện tượng sang kiểm chứng cơ chế, tập trung vào việc xác định EVs-cargo và làm rõ vai trò chức năng của chúng. Cách tiếp cận này đã góp phần quan trọng vào việc hiểu sâu hơn cơ chế giao tiếp giữa các tế bào trong vi môi trường nang noãn, nền tảng cho sự hình thành các noãn có năng lực phát triển cao.
Với những đặc tính sinh học thuận lợi cùng khả năng được kỹ thuật hóa, EVs cho thấy tiềm năng điều trị đầy hứa hẹn trong các bệnh lý buồng trứng gắn liền với suy giảm chất lượng noãn và nang noãn. Tuy nhiên, các ứng dụng hiện nay vẫn chủ yếu dừng lại ở mô hình động vật và các thử nghiệm lâm sàng giai đoạn sớm. Trong tương lai, những nghiên cứu chuyên sâu hơn về EVs góp phần thúc đẩy chuyển giao từ nghiên cứu cơ bản sang ứng dụng lâm sàng, mở ra các chiến lược mới trong bảo tồn chức năng buồng trứng và điều trị vô sinh.
Từ khoá: Túi ngoại bào, noãn bào, bệnh lý buồng trứng, exosome
Tài liệu tham khảo
[1] “Kowalczyk, A., Wrzecińska, M., Czerniawska-Piątkowska, E., & Kupczyński, R. (2022). Exosomes–Spectacular role in reproduction. Biomedicine & Pharmacotherapy, 148, 112752.”
[2] “Gurunathan, S., Kang, M. H., Song, H., Kim, N. H., & Kim, J. H. (2022). The role of extracellular vesicles in animal reproduction and diseases. Journal of Animal Science and Biotechnology, 13(1), 62.”
[3] Z. Zhao và c.s., “Extracellular vesicles: Roles in oocytes and emerging therapeutic opportunities”, Chin. Med. J. (Engl.), vol 138, số p.h 9, tr 1050–1060, tháng 5 2025, doi: 10.1097/CM9.0000000000003578.
[4] “Wang, J., Wang, D., Zhang, Y., Sun, P., Yi, L., Han, A., ... & Ma, H. (2025). Extracellular vesicles in reproductive biology and disorders: a comprehensive review. Frontiers in Endocrinology, 16, 1550068.”
[5] “Pournourali, M., Mizban, N., Ehsani, R., Ebrahimian, S., Nadri, T., & Azari-Dolatabad, N. (2025). Extracellular vesicles: Key mediators in in vitro embryo production. Frontiers in Veterinary Science, 12, 1641966.”
[6] L. Yu và c.s., “Follicular fluid steroid and gonadotropic hormone levels and mitochondrial function from exosomes predict embryonic development”, Front. Endocrinol., vol 13, tr 1025523, 2022, doi: 10.3389/fendo.2022.1025523.
[7] “da Silveira JC, Andrade GM, Del Collado M, Sampaio RV, Sangalli JR, Silva LA, et al. Supplementation with small-extracellular vesicles from ovarian follicular fluid during in vitro production modulates bovine embryo development. PloS One. (2017) 12:e0179451. doi: 10.1371/journal.pone.0179451”.
[8] “Lopera-Vasquez R, Hamdi M, Maillo V, Gutierrez-Adan A, Bermejo-Alvarez P, Ramírez M, et al. Effect of bovine oviductal extracellular vesicles on embryo development and quality in vitro . Reproduction. (2017) 153:461–70. doi: 10.1530/rep-16-0384”.
[9] “Bridi A, Perecin F, Silveira JCD. Extracellular vesicles mediated early embryo-maternal interactions. Int J Mol Sci. (2020) 21. doi: 10.3390/ijms21031163”.
[10] “Li H Huang X Chang X Yao J He Q Shen Z, et al. S100-A9 protein in exosomes derived from follicular fluid promotes inflammation via activation of NF-κB pathway in polycystic ovary syndrome. J Cell Mol Med 2020;24:114–125. doi: 10.1111/jcmm.14642.”
[11] “Battaglia R Musumeci P Ragusa M Barbagallo D Scalia M Zimbone M, et al. Ovarian aging increases small extracellular vesicle CD81(+) release in human follicular fluid and influences miRNA profiles. Aging (Albany NY) 2020;12:12324–12341. doi: 10.18632/aging.103441.”
[12] “Sysoeva A Akhmedova Z Nepsha O Makarova N Silachev D Shevtsova Y, et al. Characteristics of the follicular fluid extracellular vesicle molecular profile in women in different age groups in ART programs. Life (Basel) 2024;14:541. doi: 10.3390/life14050541.”
[13] J. Horton, M. Sterrenburg, S. Lane, A. Maheshwari, T. C. Li, và Y. Cheong, “Reproductive, obstetric, and perinatal outcomes of women with adenomyosis and endometriosis: a systematic review and meta-analysis”, Hum. Reprod. Update, vol 25, số p.h 5, tr 592–632, tháng 9 2019, doi: 10.1093/humupd/dmz012.
[14] “Zhang J Li K Gao L Zhu P Shu L Cai L, et al. Glucose metabolism disorder related to follicular fluid exosomal miR-122-5p in cumulus cells of endometriosis patients. Reproduction 2024;168:e240028. doi: 10.1530/rep-24-0028.”
[15] “Lin J Wu Z Zheng Y Shen Z Gan Z Ma S, et al. Plasma-derived exosomal miRNA profiles reveal potential epigenetic pathogenesis of premature ovarian failure. Hum Genet 2024;143:1021–1034. doi: 10.1007/s00439-023-02618-1.”
[16] “Bao Z Li J Cai J Yao S Yang N Yang J, et al. Plasma-derived exosome miR-10a-5p promotes premature ovarian failure by target BDNF via the TrkB/Akt/mTOR signaling pathway. Int J Biol Macromol 2024;277:134195. doi: 10.1016/j.ijbiomac.2024.134195.”
[17] “Song J Guo X Zhang B Zhang Q Han Y Cao D, et al. Human umbilical cord mesenchymal stem cells derived exosomes improved the aged mouse IVM oocytes quality. Reprod Sci 2024;31:2808–2819. doi: 10.1007/s43032-024-01566-z.”
[18] “de Almeida Monteiro Melo Ferraz M, Fujihara M, Nagashima JB, Noonan MJ, Inoue-Murayama M, Songsasen N. Follicular extracellular vesicles enhance meiotic resumption of domestic cat vitrified oocytes. Sci Rep 2020;10:8619. doi: 10.1038/s41598-020-65497-w.”
[19] “Song A Zhang S Zhao X Wu S Qi X Gao S, et al. Exosomes derived from menstrual blood stromal cells ameliorated premature ovarian insufficiency and granulosa cell apoptosis by regulating SMAD3/AKT/MDM2/P53 pathway via delivery of thrombospondin-1. Biomed Pharmacother 2023;166:115319. doi: 10.1016/j.biopha.2023.115319.”
[20] “Zhao Y, Pan S, Wu X. Human umbilical cord mesenchymal stem cell-derived exosomes inhibit ovarian granulosa cells inflammatory response through inhibition of NF-κB signaling in polycystic ovary syndrome. J Reprod Immunol 2022;152:103638. doi: 10.1016/j.jri.2022.103638.”
[21] “Fiorentino G Cimadomo D Innocenti F Soscia D Vaiarelli A Ubaldi FM, et al. Biomechanical forces and signals operating in the ovary during folliculogenesis and their dysregulation: Implications for fertility. Hum Reprod Update 2023;29:1–23. doi: 10.1093/humupd/dmac031.”
[22] “Eslami N Bahrehbar K Esfandiari F Shekari F Hassani SN Nazari A, et al. Regenerative potential of different extracellular vesicle subpopulations derived from clonal mesenchymal stem cells in a mouse model of chemotherapy-induced premature ovarian failure. Life Sci 2023;321:121536. doi: 10.1016/j.lfs.2023.121536.”
[23] “Davoodi Asl F Sahraei SS Kalhor N Fazaeli H Sheykhhasan M Soleimani Moud S, et al. Promising effects of exosomes from menstrual blood-derived mesenchymal stem cells on endometriosis. Reprod Biol 2023;23:100788. doi: 10.1016/j.repbio.2023.100788.”
[24] “Teng X, Wang X, Wang Z. Mesenchymal stromal cell exosome-induced vascular regeneration in a PCOS mouse model. Reprod Sci 2024. doi: 10.1007/s43032-024-01720-7.”