Kỹ sư CNSH Cao Vân Anh
Đơn vị HTSS IVFMD FAMILY, BVĐK Gia Đình, Đà Nẵng
Phôi lệch bội (aneuploidy) là phôi có bất thường về mặt số lượng nhiễm sắc thể (dư hoặc thiếu một hoặc vài nhiễm sắc thể thường hoặc nhiễm sắc thể giới tính). Phôi lệch bội có thể là nguyên nhân dẫn đến thất bại làm tổ, sảy thai sớm hoặc một số dị tật bẩm sinh. Trên thực tế, hơn 50% phôi tiền làm tổ là lệch bội và không thể đạt được thai kỳ khỏe mạnh (1). Do đó, lệch bội ở phôi là một trở ngại lớn trong việc đạt được thai kỳ thành công trong các chu kỳ thụ tinh trong ống nghiệm (IVF).
Phân tích tinh trùng và noãn người đã chỉ ra rằng lệch bội ở phôi tiền làm tổ chủ yếu là do cơ chế phân ly nhiễm sắc thể giảm phân dễ bị lỗi trong noãn và tuổi của mẹ là yếu tố quan trọng chính liên quan đến lệch bội: 50% trứng từ phụ nữ lớn tuổi (≥40 tuổi) là thể lệch bội do lỗi giảm phân. Lệch bội giảm phân có thể xảy ra do không phân ly giảm phân I (MI), không phân ly giảm phân II (MII) và MI hoặc tiền phân chia MII. Bên cạnh đó, lỗi bộ gen cũng có thể phát sinh trong quá trình phân chia nguyên phân sau thụ tinh, dẫn đến phôi khảm. Các cơ chế dẫn đến khảm phôi trong quá trình nguyên phân phôi là không phân ly nguyên phân, trễ kỳ sau và nội nhân đôi nhiễm sắc thể.
Do đó, việc hiểu rõ cơ chế phân tử của lệch bội ở phôi tiền làm tổ sẽ mở đường cho chiến lược lâm sàng giảm lệch bội và cải thiện thành công IVF.
1.Bất thường giảm phân giao tử
Các tế bào mầm trải qua một quá trình phân chia tế bào chuyên biệt-giảm phân- tạo ra các giao tử đơn bội (tinh trùng và noãn). Do đó, khi thụ tinh tạo thành bộ nhiễm sắc thể lưỡng bội do một nửa đến từ bố và một nửa đến từ mẹ (2). Trong đó, khi phân tích tinh trùng và noãn người đã chỉ ra rằng lệch bội ở phôi tiền làm tổ chủ yếu là do cơ chế phân ly nhiễm sắc thể giảm phân dễ bị lỗi trong noãn lên tới 20–30%, trong khi tinh trùng ở nam giới chỉ có 1–8% có thành phần nhiễm sắc thể bất thường (3). Điều này có thể lý giải như sau, ở tinh trùng người, giảm phân kéo dài khoảng 50–70 ngày và các điểm kiểm tra chu kỳ tế bào trong quá trình giảm phân đảm bảo rằng hầu hết các giao tử có khả năng lệch bội đều trải qua quá trình chết tế bào theo chương trình apoptosis, dẫn đến số lượng tinh trùng giảm (4). Trong khi đó, ở noãn, giảm phân là một quá trình kéo dài hàng thập kỷ bao gồm nhiều lần bắt đầu và dừng chu kỳ tế bào, và nó được kết hợp với việc đạt được năng lực phát triển để hỗ trợ quá trình thụ tinh và phát triển phôi sớm.
1.1. Giảm phân ở noãn người
Giảm phân bao gồm hai lần phân chia tế bào liên tiếp, trong đó đầu tiên là các nhiễm sắc thể tương đồng-homologous chromosomes (giảm phân I) và sau đó là các nhiễm sắc thể chị em-sister chromatid (giảm phân II) tách ra. Sự phân ly của các nhiễm sắc thể tương đồng trong lần phân chia giảm phân đầu tiên đòi hỏi các nhiễm sắc thể tương đồng phải liên kết với nhau. Những liên kết này được thiết lập trong giai đoạn đầu của quá trình phát triển noãn trong quá trình phát triển của thai nhi bé gái trong một quá trình gọi là tái tổ hợp tương đồng (Hình 1). Đầu tiên, nhiễm sắc thể của mẹ và bố được kéo lại với nhau bởi phức hợp synaptonemal và sau đó trải qua sự trao đổi chéo (Hình 1A). Sau khi trao đổi chéo, các nhiễm sắc thể chị em mới được hình thành bao gồm các phân đoạn liền kề của các nhiễm sắc thể chị em của mẹ và của bố. Các phức hợp cohesin trước đây liên kết các nhiễm sắc thể chị em của mỗi nhiễm sắc thể tương đồng bây giờ liên kết các nhiễm sắc thể tương đồng (Hình 1B): cohesin xa các vị trí giao thoa - crossover (cohesin xa-distal cohesin) liên kết các nhiễm sắc thể tương đồng với nhau, trong khi cohesin giữa các vị trí trao đổi chéo và tâm động (cohesin gần-proximal cohesin) tiếp tục để liên kết các nhiễm sắc thể chị em. Cấu hình nhiễm sắc thể mà trong đó hai nhiễm sắc thể tương đồng được liên kết được gọi là nhiễm sắc thể bivalent (Hình 1C) (5).
.png)
Hình 1. Nhiễm sắc thể bivalent được hình thành sau quá trình tái tổ hợp tương đồng (5)
Trong quá trình giảm phân I, các nhiễm sắc thể bivalent cần định hướng trên thoi phân bào sao cho hai nhiễm sắc thể chị em của mỗi nhiễm sắc thể tương đồng hướng về cùng một cực của thoi phân bào. Các kinetochore của các nhiễm sắc thể chị em cần hoạt động như một kinetochore duy nhất. Việc ghép các kinetochore chị em thành một đơn vị chức năng được cho là tạo điều kiện thuận lợi cho chức năng này.
Sau đó, các noãn bào đi vào trạng thái nghỉ ngơi của tế bào được gọi là “sự ngừng hoạt động của dictyate” có thể kéo dài vài thập kỷ ở người. Đơn vị chức năng của noãn bào và tế bào soma trong buồng trứng được gọi là nang noãn. Ở trạng thái lưu trữ của chúng, noãn bào vẫn nhỏ và được bao quanh bởi một lớp biểu mô duy nhất của các tế bào soma gọi là “nang trứng nguyên thủy”. Theo chu kỳ, một số nang trứng nguyên thủy bắt đầu phát triển. Các tế bào soma nuôi dưỡng noãn bào bằng các tiền chất đại phân tử thông qua các mối nối khe và thể tích noãn bào tăng lên đáng kể. Sự làm giàu chất dinh dưỡng này chuẩn bị cho noãn trưởng thành có thể tạo ra phôi sau khi thụ tinh.
Noãn thoát khỏi tình trạng ngừng phân bào sau tuổi dậy thì. Vào giữa chu kỳ kinh nguyệt, một đợt tăng đột biến hormone hoàng thể từ tuyến yên khiến noãn tiếp tục giảm phân. Đầu tiên, nhân bị phá vỡ và thoi phân bào được lắp ráp để sắp xếp các nhiễm sắc thể trong kỳ giữa của giảm phân I (Hình 2A). Sau đó thoi phân bào di chuyển đến vỏ noãn để phân chia các nhiễm sắc thể tương đồng. Kết quả sau giảm phân I là một bộ nhiễm sắc thể tương đồng nằm trong noãn và bộ còn lại được đẩy vào thể cực đầu tiên- first polar body (PBI) (Hình 2B).
Ở cấp độ phân tử, sự phân chia nhiễm sắc thể trong giảm phân I được kích hoạt bởi sự phân cắt Rec8, một tiểu đơn vị đặc hiệu của giảm phân của phức hợp cohesin (6). Rec8 được phân cắt bởi enzyme Separase, được kích hoạt trong kỳ sau (Hình 1B). Chỉ có cohesin ở vùng cánh tay bị cắt trong kỳ sau I, do đó các nhiễm sắc thể tương đồng có thể phân ly với nhau. Còn cohesin ở tâm động được bảo vệ khỏi sự phân cắt bởi các protein Shugoshin (Sgo), do đó các nhiễm sắc thể chị em vẫn ở cùng nhau trong kỳ sau I (Hình 2A).
Trong giảm phân II, thoi phân bào thứ hai được lắp ráp. Noãn hiện đã trưởng thành dừng lại ở kỳ giữa II và được vận chuyển đến ống dẫn trứng trong quá trình rụng trứng. Noãn chỉ hoàn thành lần phân chia giảm phân II khi được tinh trùng thụ tinh. Trong quá trình phân chia giảm phân II, các protein Sgo di chuyển đến kinetochore, cho phép phân cắt cohesin tâm động ở kỳ sau II. Các nhiễm sắc thể chị em của các nhiễm sắc thể còn lại phân chia thành noãn và thể cực thứ hai để hoàn thành giảm phân II (Hình 2B). Nhiễm sắc thể từ noãn và tinh trùng được bao bọc trong các màng nhân, sau đó hợp nhất để chuẩn bị cho lần phân chia nguyên phân đầu tiên của phôi (Hình 2C). Sau đó, phôi phát triển phân chia thành phôi nang và làm tổ ở tử cung để phát triển (5).
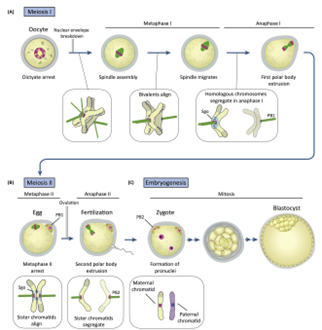
Hình 2. Sự giảm phân của noãn chuẩn bị cho quá trình thụ tinh (5)
1.2. Các loại lệch bội trong noãn người
Có 3 con đường giải thích cho các lỗi phân ly nhiễm sắc thể trong giảm phân: không phân ly-nondisjunction (NDJ), sự phân ly sớm các nhiễm sắc thể chị em- premature separation of sister chromatids (PSSC) và sự phân ly ngược- reverse segregation (RS).Lỗi không phân ly (NDJ) xảy ra khi nhiễm sắc thể tương đồng hoặc nhiễm sắc thể chị em không phân ly trong giảm phân I hoặc giảm phân II. PSSC hay sự phân ly sớm của các nhiễm sắc thể chị em tại MI thay vì MII, dẫn đến sự phân chia 3:1 của các nhiễm sắc thể ở noãn và thể cực thứ nhất. Kiểu phân ly ngược mới được xác định, xảy ra khi các nhiễm sắc thể chị em (nhưng không phải nhiễm sắc thể tương đồng) phân ly trong giảm phân I, điều này có thể cản trở sự sắp xếp và phân ly chính xác trong giảm phân II. (Hình 3A) (2), (5).
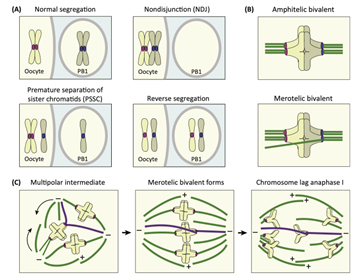
Hình 3. Lỗi phân ly nhiễm sắc thể trong giảm phân (5)
(A) Ba con đường lỗi phân ly chính; (B) Kinetochore của nhiễm sắc thể giảm phân có thể gắn không chính xác vào vi ống của thoi phân bào (sợi màu xanh lá cây); (C) Các thoi phân bào giảm phân trong noãn của người đôi khi tạo thành các chất trung gian đa cực có thể dẫn đến các liên kết merotelic dễ bị lỗi.
Theo tổng hợp của Lena Wartosch và cộng sự, ở noãn người, lỗi phân ly nhiễm sắc thể trong quá trình phân chia giảm phân I phổ biến hơn so với giảm phân II (MII). Trong một nghiên cứu gần đây của Gruhn và cộng sự, việc phân ly sai đã được xác định ở noãn người theo độ tuổi (từ 9 đến 43) và được phát hiện tuân theo đường cong chữ U (Hình 4B, đường chấm đỏ) do ba kiểu lỗi không phân ly NDJ, PSSC và RS (Hình 4A) (2).
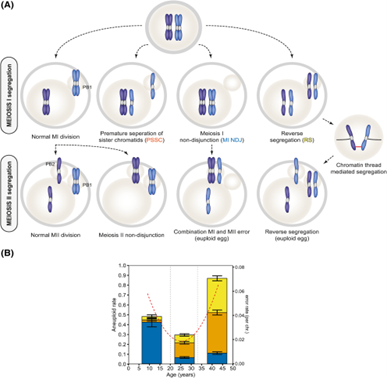
Hình 4. Lỗi phân ly giảm phân I và giảm phân II và sự phụ thuộc vào độ tuổi của chúng trong noãn người (2)
(A) Các kiểu phân ly nhiễm sắc thể trong giảm phân I và giảm phân II. (B) Đường cong chữ U của lệch bội trong noãn người (đường chấm đỏ) là sự tổng hợp của cả ba sự kiện phân ly sai nhiễm sắc thể—MI NDJ (màu xanh lam), PSSC (màu cam) và RS (màu vàng)—và hoạt động theo cách phụ thuộc vào độ tuổi.
Các phân tích tế bào học gần đây về các thể phân cực cho thấy rằng các lỗi do PSSC gây ra phổ biến hơn so với các lỗi do NDJ gây ra (7). Điều thú vị là lỗi PSSC trong giảm phân I có thể được khắc phục bằng lỗi “cân bằng” trong giảm phân II, nghĩa là nếu cả thể phân cực thứ nhất và thứ hai đều chia sẻ lỗi qua lại (ví dụ, mất ở thể phân cực thứ nhất tiếp theo là tăng ở thể phân cực thứ hai; hoặc ngược lại) thì noãn tạo thành sẽ có số lượng nhiễm sắc thể chính xác. Nhiễm sắc thể 15, 16, 21 và 22 nằm trong số những tác nhân phổ biến nhất gây ra tình trạng lệch bội ở người (7).
PSSC ban đầu được xác định là loại lỗi phân ly phổ biến nhất ở noãn. Kiểu phân ly này tăng tuyến tính theo tuổi. Do đó, giả thuyết cho rằng có thể việc mất sớm sự gắn kết tâm động trong giai đoạn dictyate kéo dài và sự gắn kết kinetochore bất thường dẫn đến PSSC ở noãn tăng lên khi tuổi của mẹ tăng lên. Trong những trường hợp mất sự gắn kết quá mức hơn (tức là, sự gắn kết của cả tâm động và cánh tay đều yếu đi trong MI) hoặc khi các nhiễm sắc thể tương đồng không trao đổi chéo, sự phân ly ngược-RS có thể xảy ra khi cả hai nhiễm sắc thể chị em tách sớm trong MI. RS được phát hiện xảy ra ở tần suất cao hơn gần 100 lần so với PSSC riêng lẻ, chứng tỏ PSSC và RS có nguồn gốc riêng biệt. Thật vậy, RS cho thấy sự gia tăng đáng kể giữa các nhóm tuổi của mẹ cả trung niên và cao tuổi phù hợp với giả thuyết mất kết dính rộng rãi hơn dọc theo toàn bộ cánh nhiễm sắc thể hoặc trên cả hai bộ tâm động. Cả PSSC và RS đều được phát hiện chủ yếu ảnh hưởng đến nhiễm sắc thể acrocentric (chr. 13-15 21 & 22), do đó cho thấy mối tương quan tiềm ẩn giữa mất kết dính và tỷ lệ lệch bội (2).
Gần đây, một kiểu lỗi thứ ba đã tái xuất hiện như một loại lỗi lớn thông qua việc đưa vào phạm vi tuổi rộng hơn trong phân tích lệch bội noãn. MI không phân ly-NDJ, trong đó các nhiễm sắc thể tương đồng không tách rời và cả bốn nhiễm sắc thể chị em đều đi vào một tế bào con (4:0), được phát hiện là cực kỳ phổ biến ở độ tuổi của bà mẹ trẻ hơn (<20). Phân tích sâu hơn cho thấy MI NDJ không chỉ xảy ra chủ yếu ở noãn của phụ nữ trẻ mà các nhiễm sắc thể bị ảnh hưởng bởi kiểu lỗi này chủ yếu là các nhiễm sắc thể lớn nhất (chr. 1–5). Các nhiễm sắc thể này cho thấy khả năng lệch bội thấp hơn ở phôi và thai kỳ được công nhận trên lâm sàng (8).
1.3. Nguyên nhân liên quan đến tuổi tác gây ra tình trạng bất thường nhiễm sắc thể
Phụ nữ dần mất khả năng mang thai khi họ già đi. Các lỗi phân ly nhiễm sắc thể giảm phân tăng mạnh trong khoảng sau 35 tuổi. Thật vậy, một phân tích tế bào di truyền toàn diện kiểm tra hơn 20.000 noãn của người bằng FISH đã báo cáo rằng tình trạng lệch bội xảy ra ở 20% noãn của phụ nữ 35 tuổi và tăng lên gần 60% noãn của phụ nữ trên 43 tuổi. Cùng quan điểm đó, Jason M. Franasiak và cộng sự cũng tìm thấy mức lệch bội thấp nhất trong độ tuổi từ 26 đến 30 với mức tăng đều đặn và có thể dự đoán được cho đến độ tuổi 43, tại thời điểm đó, tỷ lệ này đạt mức ổn định ở mức khoảng 85%, phù hợp với dữ liệu đã công bố trước đó (9). Ngoài ra, các nghiên cứu gần đây sử dụng aCGH đã xác nhận rằng tỷ lệ lệch bội tăng đáng kể ở noãn của phụ nữ lớn tuổi (5).a. Sự tách biệt kinetochore chị em thúc đẩy sự sắp xếp không chính xác với trục chính giảm phân
Các nhiễm sắc thể chị em trong noãn người mất sự gắn kết theo tuổi tác, điều này có thể dẫn đến sự sắp xếp không chính xác của các nhiễm sắc thể bivalent trong giảm phân I. Thông thường, các kinetochore chị em của các nhiễm sắc thể đôi có thể cách nhau tới 0.2 µm và tần suất các kinetochore chị em tách biệt tăng đáng kể theo tuổi của mẹ. Các nhiễm sắc thể chị em liên kết lỏng lẻo có thể hoạt động không chính xác khi sắp xếp trên thoi phân bào giảm phân. Ở noãn của người, các kinetochore chị em phân ly có xu hướng hình thành nhiều sự gắn kết merotelic hơn với các vi ống của thoi phân bào (Hình 3B). Ngoài ra, các con đường liên quan đến tuổi tác có thể thúc đẩy các sự gắn kết kinetochore-vi ống bị khiếm khuyết (5).Ngoài ra, sự tách biệt quá mức của các kinetochore chị em trong noãn người làm cho các bivalent có sự sắp xếp ngẫu nhiên trong thoi phân bào giảm phân. Trong một cấu hình mới được xác định của các bivalent được gọi là “bivalent đảo ngược- “inverted bivalents”, các bivalent được xoay theo trục thoi phân bào: các chromatid chị em của một nhiễm sắc thể tương đồng định hướng không chính xác như trong nguyên phân, do đó liên kết với các vi ống từ các cực của thoi phân bào đối diện thay vì định hướng về cùng một cực của thoi phân bào (Hình 5B). Có hai dạng: bivalent đảo ngược một nửa và hoàn toàn. Đối với bivalent đảo ngược một nửa thì chỉ có một cặp chromatid chị em liên kết các cực của thoi phân bào đối diện, trong khi bivalent đảo ngược hoàn toàn thì cả hai cặp đều liên kết với các cực đối diện. Các bivalent đảo ngược thường được quan sát thấy nhiều hơn trong các noãn của phụ nữ lớn tuổi và tương quan với khoảng cách tăng lên giữa các kinetochore chị em (5).
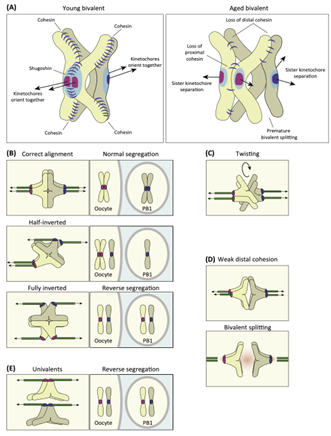
Hình 5. Những thay đổi về cấu trúc và sự sắp xếp thay thế của nhiễm sắc thể giảm phân (5)
(A) Một mô hình về những thay đổi về cấu trúc liên quan đến tuổi mà nhiễm sắc thể bivalent trong noãn của động vật có vú có thể xảy ra. (B) Các nhiễm sắc thể bivalent có sự sắp xếp bất thường trong thoi phân bào giảm phân. (C) Sự xoắn của các nhiễm sắc thể tương đồng trong nhiễm sắc thể bivalent có thể làm căng thẳng sự gắn kết giữa các nhiễm sắc thể. (D) Ở một số nhiễm sắc thể bivalent, các nhiễm sắc thể tương đồng được ngăn cách bởi các khoảng trống lớn. (E) Nhiễm sắc thể univalent hình thành khi nhiễm sắc thể bivalent phân chia sớm thành các cặp nhiễm sắc thể tương đồng.
b. Các nhiễm sắc thể bivalent có độ gắn kết xa (distal cohesin) giảm có thể phân chia sớm thành các nhiễm sắc thể univalent
Sự mất gắn kết liên quan đến tuổi trong các nhiễm sắc thể bivalent không chỉ ảnh hưởng đến vùng quanh tâm động được bao quanh bởi kinetochore, mà còn ảnh hướng đến sự gắn kết liên kết các nhiễm sắc thể tương đồng. Các nhiễm sắc thể tương đồng trong các nhiễm sắc thể bivalent thường bị tách biệt bởi các khoảng trống lớn trong noãn của phụ nữ lớn tuổi. Do đó, những khiếm khuyết về cấu trúc này chỉ ra sự gắn kết yếu giữa các nhiễm sắc thể tương đồng trong nhiễm sắc thể bivalent.Trong những trường hợp quá mức hơn, các nhiễm sắc thể bivalent có phân chia sớm thành hai nhiễm sắc thể riêng lẻ (nhiễm sắc thể univalent) trước kỳ sau I (Hình 5D). Tỷ lệ nhiễm sắc thể univalent tăng đáng kể theo tuổi, xảy ra ở 40% noãn từ phụ nữ trên 35 tuổi, trong khi phụ nữ từ 30–35 tuổi chỉ chiếm 10%. Các nhiễm sắc thể univalent này có thể xếp thẳng hàng trên thoi phân bào giảm phân I với cả hai kinetochore chị em hướng về các cực của thoi phân bào đối diện, tương tự như nhiễm sắc thể nguyên phân (Hình 5E). Do đó, có thể dẫn đến kiểu phân ly tương tự như nguyên phân và dẫn đến sự phân ly ngược: kết quả là mặc dù số lượng nhiễm sắc thể ở noãn và PBI là chính xác, nhưng các nhiễm sắc thể sẽ có nguồn gốc từ cha mẹ khác nhau (Hình 5E). Và dẫn đến các nhiễm sắc thể không thể sắp xếp chính xác với thoi phân bào ở kỳ giữa II (5).
Hiện nay, các cơ chế phân tử có thể gây ra những thay đổi đáng kể liên quan đến tuổi tác đối với cấu trúc nhiễm sắc thể trong noãn người vẫn chưa được biết rõ. Ở chuột, các nghiên cứu đã xác định mất cohesin là một yếu tố chính góp phần gây ra lệch bội liên quan đến tuổi tác. Các phức hợp cohesin chứa Rec8 trong noãn chuột đã có trong quá trình sao chép DNA ở giai đoạn đầu của giảm phân. Người ta cho rằng chúng chỉ được bổ sung sau khi thụ tinh khi DNA được sao chép lại trong phôi. Do đó, các phức hợp cohesin phải duy trì tại chỗ trong suốt thời gian kéo dài của quá trình dừng dictyate để đảm bảo phân ly nhiễm sắc thể chính xác trong giảm phân. Mức độ Rec8 giảm đáng kể ở các noãn bivalent từ chuột già tự nhiên. Ngoài ra, Sgo2 quanh tâm động cũng giảm trên các nhiễm sắc thể bivalent ở noãn của những con chuột cái lớn tuổi. Do đó, các cohesin gần không được bảo vệ khỏi sự phân cắt của Separase trong giảm phân I. Mặc dù nhiều chi tiết phân tử liên quan đến nhiễm sắc thể giảm phân của người vẫn chưa được biết, nhưng có thể tương tự như những thay đổi được quan sát thấy ở chuột (5).
1.4. Nguyên nhân gây ra tình trạng lệch bội không phụ thuộc vào độ tuổi
Tình trạng lệch bội không chỉ ảnh hưởng đến trứng của phụ nữ lớn tuổi mà còn ảnh hưởng đến trứng của phụ nữ trẻ vì trứng do phụ nữ trẻ sản xuất trong những năm tháng sung sức nhất của khả năng sinh sản vẫn thường bị khiếm khuyết. Bằng chứng là nhiều nghiên cứu đã chỉ ra trứng do phụ nữ trẻ hiến tặng để thụ tinh trong ống nghiệm thường tạo ra phôi bị lệch bội và nhiều cá nhân mắc hội chứng Down được sinh ra từ những bà mẹ dưới 35 tuổi (5). Jason M. Franasiak cũng ghi nhận tỷ lệ mắc bệnh tăng nhẹ được ghi nhận ở độ tuổi trẻ hơn, với >40% lệch bội ở phụ nữ từ 23 tuổi trở xuống (2).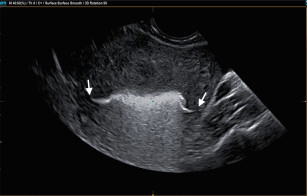
Hình 6. Tỷ lệ lệch bội theo độ tuổi của phụ nữ (2)
a.Điểm kiểm tra lắp ráp thoi phân bào (SAC-spindle assembly checkpoint) ở noãn ít nghiêm ngặt hơn so với nguyên phân
Sự phân ly nhiễm sắc thể chính xác phụ thuộc vào sự gắn kết chính xác của các vi ống thoi phân bào với thể động. Ở kỳ giữa I, các nhiễm sắc thể bivalent xếp thẳng hàng giữa hai cực của thoi phân bào (Hình 2A). Mỗi cặp thể động kinetochore chị em của thể bivalent phải được gắn vào cùng một cực của thoi phân bào, trong khi các nhiễm sắc thể tương đồng phải được gắn vào các cực của thoi phân bào đối diện. Kinetochore-kinetochore có thể tạo thành các điểm gắn kết vi ống không chính xác. Trong quá trình này, kinetochore không được gắn vào các vi ống thoi phân bào được điểm kiểm tra lắp ráp thoi phân bào (SAC) cảm nhận, điểm này chỉ cấp phép cho các tế bào tiến triển vào kỳ sau nếu tất cả các kinetochore được gắn vào các vi ống thoi phân bào.Tuy nhiên, noãn động vật có vú có thể tiến hành giảm phân mặc dù nhiễm sắc thể không thẳng hàng. Ở noãn chuột, nhiễm sắc thể không thẳng hàng chỉ làm chậm quá trình tiến triển của giảm phân, trong khi các điểm gắn thoi phân bào đúng đôi khi bị mất ổn định không đúng cách. Noãn người có nhiễm sắc thể không thẳng hàng cũng tiến triển hiệu quả vào kỳ sau. Vì sự sắp xếp của nhiễm sắc thể trên thoi phân bào kỳ giữa mất vài giờ trong noãn động vật có vú. Bằng chứng từ noãn chuột cho thấy rằng hoạt động tăng lên của CDK1 trong phức hợp với Cyclin B làm ổn định các điểm bám của vi ống và vô hiệu hóa sự bắt giữ SAC, do đó noãn được phép tiến triển vào kỳ sau mặc dù nhiễm sắc thể thẳng hàng lỗi (5).
b.Sự bất ổn của thoi phân bào và các giai đoạn thoi phân bào đa cực tạm thời cản trở sự gắn kết của nhiễm sắc thể và vi ống
Các nghiên cứu gần đây cho thấy thoi phân bào trong noãn người thường không ổn định, tạo thành các chất trung gian đa cực tạm thời có liên quan đến lỗi phân ly. Các giai đoạn đa cực tạm thời được cho là thúc đẩy sự gắn kết merotelic, xảy ra khi các thể động liên kết với các vi ống của thoi phân bào từ nhiều cực của thoi phân bào (Hình 3B) hoặc có thể hình thành trong quá trình tái tổ chức các thoi phân bào đa cực tạm thời (Hình 3C). Sự bất ổn của thoi phân bào và sự gắn kết merotelic cũng có thể được thúc đẩy bởi tổ chức chuyên biệt của các kinetochore chị em trong các noãn người và thường bị ngăn cách bởi các khoảng trống lớn thay vì liên kết chặt chẽ, ngay cả trong các noãn của phụ nữ trẻ. Do đó, các kinetochore chị em tách biệt có thể làm tăng khả năng gắn vi ống kinetochore bất thường (5).c.Tái tổ hợp tương đồng ảnh hưởng đến sự gắn kết nhiễm sắc thể ở thể bivalent
Vị trí không tối ưu của các vị trí giao thoa có thể gây ra sự liên kết yếu của nhiễm sắc thể trong thể bivalent, khiến chúng dễ bị lỗi phân ly. Vị trí của các vị trí giao thoa khác nhau giữa các loài và giới tính. Ở phụ nữ, nhiễm sắc thể có xu hướng có nhiều vị trí giao thoa hơn ở nam giới và nhiễm sắc thể dài hơn tạo ra nhiều giao thoa hơn so với nhiễm sắc thể ngắn hơn. Khi các vị trí giao thoa hình thành gần telomere, lượng cohesin giảm có thể liên kết các nhiễm sắc thể tương đồng, trong khi các vị trí giao thoa trong tâm động có thể làm giảm sự gắn kết của nhiễm sắc thể chị em hoặc ngăn cản việc loại bỏ các cohesin, gây ra lỗi NDJ. Hai vị trí giao thoa hình thành gần nhau cũng có thể dẫn đến sự gắn kết yếu giữa các nhiễm sắc thể tương đồng. Tuy nhiên, sự can thiệp giao thoa đã được báo cáo trong một số nghiên cứu, trong đó hai vị trí giao thoa có xu hướng hình thành xa hơn so với dự kiến một cách ngẫu nhiên. Cơ chế này có thể giúp giảm khả năng nhiễm sắc thể tương đồng chỉ liên kết yếu trong quá trình giảm phân I (5).2. Bất thường nguyên phân phôi tiền làm tổ (phôi khảm)
Lỗi bộ gen phát sinh trong quá trình phân chia nguyên phân sau thụ tinh dẫn đến hình thành phôi khảm- mosaic embryo. Theo định nghĩa, phôi khảm là hiện tượng đặc trưng bởi sự hiện diện của hai hoặc nhiều dòng tế bào khác biệt về mặt di truyền trong phôi. Thể khảm xuất phát từ sai hỏng phân ly nhiễm sắc thể trong quá trình nguyên phân sau thụ tinh qua nhiều cơ chế khác nhau (1).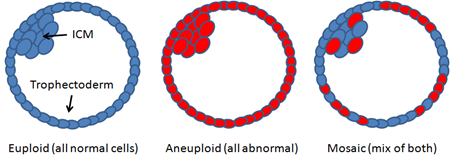
Hình 7. Đặc điểm của phôi nguyên bội, phôi lệch bội và phôi khảm (10)
2.1. Các cơ chế chính dẫn đến hình thành phôi khảm
Có ba cơ chế chính có thể dẫn đến hiện tượng thêm hoặc mất nhiễm sắc thể: sự không phân ly, nguyên phân trễ kỳ sau, và nội nhân đôi nhiễm sắc thể.a.Sự không phân ly nguyên phân
Không phân ly nguyên phân là sự thất bại của việc phân chia nhiễm sắc tử chị em trong suốt quá trình nguyên phân. Thay vì phân chia, nhiễm sắc thể được kéo về một tế bào tạo ra một tế bào thể đơn bội (monosomy) và một tế bào thể tam bội (trisomy). Nếu sự không phân ly diễn ra trước quá trình biệt hoá tế bào phôi giai đoạn tiền làm tổ sẽ tạo ra thể khảm. Nếu sự không phân ly diễn ra tại giai đoạn phôi nang- giai đoạn sau của quá trình biệt hoá phôi bào- thì chỉ có nhau thai mang các dòng tế bào khảm, tế bào phôi vẫn có thể ở dạng nguyên bội. Ảnh hưởng của sự không phân ly lên quá trình phát triển tiền làm tổ của phôi vẫn còn gây nhiều tranh cãi và một số nghiên cứu cho thấy mức độ ảnh hưởng này phụ thuộc vào giai đoạn phát triển và các nhiễm sắc thể liên quan (1).b. Trễ kỳ sau (trễ Anaphase)
Trễ kỳ sau (trễ Anaphase) là sự thất bại trong việc kết hợp của một nhiễm sắc tử vào nhân tế bào, kết quả tạo ra một tế bào monosomy và tế bào còn lại là disomy. Hai lý do chính đằng sau sự chậm trễ ở kỳ sau là: khi nhiễm sắc tử không gắn được vào thoi vô sắc hoặc khi nhiễm sắc tử gắn được vào thoi vô sắc nhưng thất bại trong việc kết hợp vào nhân. Giống như trong không phân ly nguyên phân, thời điểm xảy ra sự chậm trễ ở kỳ sau quyết định loại khảm (khảm toàn bộ hoặc khảm giới hạn). Nếu quá trình này diễn ra trước giai đoạn biệt hoá, cơ thể sẽ mang hai dòng tế bào khác nhau và tạo nên thể khảm. Nếu quá trình này diễn ra sau quá trình biệt hoá lá nuôi phôi, khi đó nhau thai sẽ mang dòng tế bào bình thường và dòng tế bào monosomy, điển hình là khảm khu trú bánh nhau. Trong nghiên cứu trên phôi ngày 5 của Loannou và cộng sự (2012), nhóm tác giả đã chứng minh rằng tần suất diễn ra thể monosomy cao hơn gấp 7 lần so với thể trisomy. Điều này chỉ ra rằng trễ kỳ sau là nguyên nhân chính dẫn đến thể khảm ở phôi người giai đoạn tiền làm tổ. Các báo cáo trước đây cho thấy hơn 50% phôi khảm do trễ kỳ sau (1).c. Nội nhân đôi nhiễm sắc thể (Endoreplication)
Nội nhân đôi nhiễm sắc thể (Endoreplication) là quá trình sao chép của một nhiễm sắc thể trong pha S của chu kỳ tế bào mà không hoàn thành nguyên phân sau đó, dẫn đến tạo ra một tế bào trisomy và một tế bào disomy. Hiện tượng tăng số lượng nhiễm sắc thể được cho rằng xuất phát từ hai cơ chế, thứ nhất là do sai hỏng trong chu trình tế bào làm cho một nhiễm sắc thể được sao chép mà không có quá trình phân chia tế bào chất sau đó và thứ hai là do quá trình nguyên phân diễn ra trong thời gian rất ngắn chỉ đủ thời gian để sao chép. Nội nhân đôi nhiễm sắc thể còn được gọi là thể đa bội, thường có liên quan đến thoi vô sắc đa cực trong quá trình nguyên phân dẫn đến đa nhân và phôi phân chia hỗn loạn. Phần lớn các trường hợp lệch bội nhiễm sắc thể trong phôi người là do không phân ly và chậm trễ kỳ sau, trong khi tỷ lệ endoreplication xảy ra ở mức độ thấp hơn (1).Ở phôi tiền làm tổ của người, các lệch bội nguyên phân và thể khảm rất phổ biến trong quá trình phân chia đầu tiên. Cụ thể, xấp xỉ 15–90% trong số tất cả các phôi người ở giai đoạn phân chia là thể khảm. Ngoài ra, dữ liệu phân tích tổng hợp cho thấy các lệch bội nguyên phân tăng từ 63% ở giai đoạn phân chia lên 95% ở giai đoạn phôi nang. Một nghiên cứu tương đối đã báo cáo rằng 69% phôi nang bất thường từ phụ nữ tuổi cao là thể khảm đối với cả khối bên trong và lớp nuôi dưỡng. Mặc dù tỷ lệ phôi khảm cao hơn ở giai đoạn phôi nang, nhưng tỷ lệ tế bào lệch bội trong phôi lại giảm, dẫn đến tương đối nhiều tế bào lưỡng bội hơn ở phôi giai đoạn phôi nang (74%) so với phôi giai đoạn phân chia (62%) (1).
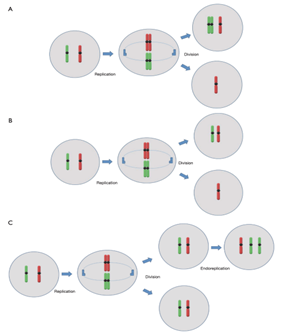
Hình 8. Tóm tắt ba cơ chế chính có thể dẫn đến hiện tượng thêm hoặc mất nhiễm sắc thể
(A) Không phân ly nguyên phân; (B) Trễ kỳ sau (trễ Anaphase); (C) Nội nhân đôi nhiễm sắc thể (Endoreplication)
2.2. Nguyên nhân
a.Các điểm kiểm tra chu kì tế bào (cell cycle checkpoints)
Ở nguyên phân, có những điểm kiểm tra chu kỳ tế bào chuyên biệt đảm bảo sự phân chia tế bào chính xác trước khi tiến triển đến giai đoạn tiếp theo. Việc nới lỏng các điểm kiểm tra chu kỳ tế bào đó có thể dẫn đến khảm bội thể bằng cách thỉnh thoảng cho phép các tế bào bỏ qua pha M. Điều này dẫn đến sự sao chép DNA mà không có sự phân chia tế bào, tạo ra một tế bào tứ bội. Tứ bội khảm rất phổ biến xảy ra ở các giai đoạn phôi sớm hơn nhưng cũng có thể được quan sát thấy trong thai trứng (<1%). Hơn nữa, khi tứ bội đi kèm với sự khuếch đại của trung thể, nó có thể dẫn đến sự phân chia tế bào đa cực trong các lần nguyên phân sau. Các điểm kiểm tra chu kỳ tế bào ở nguyên phân xảy ra trong các giai đoạn G1, G2 và kỳ giữa của chu kỳ tế bào.- Điểm kiểm soát G1 kiểm soát tất cả các yếu tố cần thiết cho quá trình tổng hợp DNA, chẳng hạn như lượng năng lượng, môi trường, kích thước tế bào và sự hiện diện của các nucleotide và chất dinh dưỡng.
- Điểm kiểm soát G2 kiểm soát quá trình nhân đôi DNA thích hợp trong pha S của chu kỳ tế bào và tiến triển thành nguyên phân (1).
b.Điểm kiểm tra lắp ráp thoi phân bào (SAC-spindle assembly checkpoint)
Ngoài các điểm kiểm tra chu kỳ tế bào đã đề cập ở trên, điểm kiểm tra chính đảm bảo sự phân chia nhiễm sắc thể thích hợp là điểm kiểm tra lắp ráp thoi phân bào (SAC). Như đã biết, thoi phân bào bao gồm các vi ống xuất hiện từ các cực của thoi phân bào (Hình 9). Các khiếm khuyết trong động lực học của vi ống, trong chức năng cực của thoi phân bào hoặc trong thành phần động học góp phần làm tăng tần suất lỗi phân chia nhiễm sắc thể.Các thành phần của SAC, chẳng hạn như Mad1, Mad2, Mad3, Mps1, Bub1, Bub3, BuBR1 và CENP-E nhận ra các thể động rỗng hoặc gắn không đúng cách và chúng kích hoạt sự chậm trễ chu kỳ tế bào cho đến khi tất cả các nhiễm sắc thể gắn đúng vào vi ống và sự liên kết thích hợp tại kỳ giữa. Sự chậm trễ này được thực hiện thông qua sự ức chế phức hợp thúc đẩy kỳ sau/cyclosome, hoạt động của phức hợp này là cần thiết cho sự tiến triển từ kỳ giữa đến kỳ sau. Các khiếm khuyết trong SAC có thể dẫn đến tình trạng lệch bội, cả trong in vitro và in vivo. Sự nghỉ hoặc không có các điểm kiểm tra chu kỳ tế bào trong phôi tiền làm tổ sớm của người góp phần gây ra tình trạng lệch bội bằng cách cho phép một phôi bào có khiếm khuyết nhiễm sắc thể xâm nhập và tiếp tục phân chia nguyên phân (1).
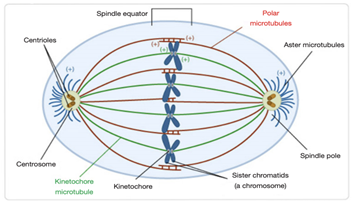
Hình 9. Vi ống kinetochore trong thoi phân bào (1)
Mỗi nhiễm sắc thể chị em của một nhiễm sắc thể được gắn vào vi ống kinetochore (hiển thị màu xanh lá cây) tại các kinetochore (một cho mỗi nhiễm sắc thể chị em). Các vi ống kinetochore được hình thành bởi các trung thể (các trung tâm tổ chức vi ống) tại các cực của thoi phân bào. Ngoài các vi ống kinetochore, còn có hai loại vi ống riêng biệt khác trong thoi phân bào: các vi ống phân cực (hiển thị màu đỏ) và các vi ống hình sao (hiển thị màu xanh). Đối với cả ba loại vi ống, các đầu âm nằm ở trung thể và các đầu dương (được chỉ định là +) phát triển ra xa trung thể.
c. Cohesin
Các cohesin có chức năng giữ cho hai nhiễm sắc thể chị em được kết nối với nhau, ngăn chúng tách ra sớm từ pha S cho đến kỳ sau. Ở kỳ sau, sự liên kết giữa các nhiễm sắc thể chị em kết thúc, cho phép chúng tách rời nhau.Các cohesin bao gồm một tiểu đơn vị kháng nguyên mô đệm (STAG) (STAG1, STAG2, STAG3), hai tiểu đơn vị duy trì cấu trúc của nhiễm sắc thể (SMC) (SMC1α, SMC1β, SMC3) và một tiểu đơn vị kleisin (RAD21, RAD21L, Rec8). Hầu hết các tiểu đơn vị được chia sẻ trong cả giảm phân và nguyên phân, ngoại trừ các tiểu đơn vị SMC1β, STAG3, RAD21L và Rec8 chỉ đặc hiệu cho giảm phân.
Khiếm khuyết của cohesin dẫn đến sự tách sớm của nhiễm sắc thể, trong khi sự chậm trễ trong việc loại bỏ chúng có thể dẫn đến sự không phân ly. Cụ thể, sự bất hoạt của STAG2 được phát hiện là dẫn đến tình trạng lệch bội ở tế bào người. Tỷ lệ lỗi nguyên phân ở tế bào soma được phát hiện là tăng lên do đột biến ở các tiểu đơn vị cohesin và các chất điều hòa của chúng. Cụ thể, người ta phát hiện ra rằng sự biểu hiện quá mức của seperase thường có thể gây ra sự tách sớm của các nhiễm sắc thể chị em, dẫn đến tình trạng lệch bội liên quan đến cả mất và tăng nhiễm sắc thể.
Tương tự như vậy, việc loại bỏ một số gen cohesin (bao gồm PLK1, STAG1, RAD21, NIPBL và SMC3) ở mô hình chuột dẫn đến tình trạng phôi ngừng phát triển sớm. Hơn nữa, các hợp tử được dự đoán sẽ tạo ra phôi ngừng phát triển biểu hiện sự biểu hiện khác biệt của một số gen cohesin bao gồm SMC3 và securin, một protein tham gia vào quá trình kiểm soát quá trình chuyển đổi giữa kỳ giữa-kỳ sau và khởi đầu kỳ sau (1).
3. Kết luận
Lệch bội ở phôi (aneuploidy) là một vấn đề nghiêm trọng trong lĩnh vực hỗ trợ sinh sản, gây ra tỷ lệ sẩy thai cao, thất bại trong các chu kỳ thụ tinh trong ống nghiệm (IVF), và các dị tật bẩm sinh. Tỷ lệ lệch bội nhiễm sắc thể cao được quan sát thấy ở phôi người trước khi làm tổ có thể phát sinh chủ yếu trong quá trình phân chia giảm phân lần thứ nhất hoặc lần thứ hai, đặc biệt là ở tuổi mẹ cao, nhưng cũng có thể phát sinh ở giai đoạn sau hợp tử trong quá trình phân chia nguyên phân của giai đoạn phân chia và phôi nang, dẫn đến thể khảm. Yếu tố nguyên nhân chính của lệch bội giảm phân là tuổi của mẹ.Việc hiểu được các cơ chế phân tử của phôi lệch bội góp phần cải thiện được các kĩ thuật thao tác của các chuyên viên phôi học trong quá trình nuôi cấy tế bào và việc lựa chọn phôi tối ưu cho bệnh nhân, góp phần tăng cơ hội thành công trong các chu kì IVF.
Tài liệu tham khảo
(1) Stolakis, V., & Bertero, M. C. (2019). Molecular aspects of aneuploidy in preimplantation human embryos: a mini-review. Reproductive BioMedicine Online, 39, e12-e13.
(2) Wartosch, L., Schindler, K., Schuh, M., Gruhn, J. R., Hoffmann, E. R., McCoy, R. C., & Xing, J. (2021). Origins and mechanisms leading to aneuploidy in human eggs. Prenatal diagnosis, 41(5), 620-630.
(3) Wang, J., Fan, H. C., Behr, B., & Quake, S. R. (2012). Genome-wide single-cell analysis of recombination activity and de novo mutation rates in human sperm. Cell, 150(2), 402-412.
(4) Miharu, N. (2005). Chromosome abnormalities in sperm from infertile men with normal somatic karyotypes: oligozoospermia. Cytogenetic and Genome Research, 111(3-4), 347-351.
(5) Webster, A., & Schuh, M. (2017). Mechanisms of aneuploidy in human eggs. Trends in cell biology, 27(1), 55-68.
(6) Prestel, M., Feller, C., & Becker, P. B. (2010). Dosage compensation and the global re-balancing of aneuploid genomes. Genome biology, 11, 1-8.
(7) Handyside, A. H., Montag, M., Magli, M. C., Repping, S., Harper, J., Schmutzler, A., ... & Geraedts, J. (2012). Multiple meiotic errors caused by predivision of chromatids in women of advanced maternal age undergoing in vitro fertilisation. European Journal of Human Genetics, 20(7), 742-747.
(8) HASSOLD, T., Jacobs, P., Kline, J., Stein, Z., & WARBURTON, D. (1980). Effect of maternal age on autosomal trisomies. Annals of human genetics, 44(1), 29-36.
( 9)Franasiak, J. M., Forman, E. J., Hong, K. H., Werner, M. D., Upham, K. M., Treff, N. R., & Scott Jr, R. T. (2014). The nature of aneuploidy with increasing age of the female partner: a review of 15,169 consecutive trophectoderm biopsies evaluated with comprehensive chromosomal screening. Fertility and sterility, 101(3), 656-663.(10
(10) Chromosomal errors in IVF: What is aneuploidy and what causes it? https://www.remembryo.com/chromosomal-errors-in-ivf-what-is-aneuploidy-and-what-causes-it/
(11) Bagó, A. C., Hernández, M. T. I., Villarreal, P. C., Ortega, C. G., & Gutiérrez, A. M. G. (2023). The importance of standardizing criteria for PGT-A interpretation of blastocysts analyzed by next-generation sequencing. JBRA Assisted Reproduction, 27(3), 453.
(12) Sanders, K. D., Silvestri, G., Gordon, T., & Griffin, D. K. (2021). Analysis of IVF live birth outcomes with and without preimplantation genetic testing for aneuploidy (PGT-A): UK Human Fertilisation and Embryology Authority data collection 2016–2018. Journal of assisted reproduction and genetics, 38, 3277-3285.
(13) Katz-Jaffe, M. G., Trounson, A. O., & Cram, D. S. (2005). Chromosome 21 mosaic human preimplantation embryos predominantly arise from diploid conceptions. Fertility and sterility, 84(3), 634-643.
(14) Baart, E. B., Martini, E., Eijkemans, M. J., Van Opstal, D., Beckers, N. G., Verhoeff, A., ... & Fauser, B. C. (2007). Milder ovarian stimulation for in-vitro fertilization reduces aneuploidy in the human preimplantation embryo: a randomized controlled trial. Human Reproduction, 22(4), 980-988.
New World Saigon Hotel, thứ bảy ngày 17 tháng 01 năm 2026
Hội Nội tiết Sinh sản và Vô sinh TP. Hồ Chí Minh (HOSREM) sẽ ...
Khách sạn Equatorial, chủ nhật ngày 23 . 11 . 2025

Ấn phẩm CẬP NHẬT KIẾN THỨC VỀ QUẢN LÝ SỨC KHỎE TUỔI MÃN ...
Y học sinh sản được phát ngày ngày 21 . 9 . 2025 và gởi đến ...
Cẩm nang Hội chứng buồng trứng đa nang được phát hành online ...








