CVPH. Ngô Thị Lan Phương
Đơn vị HTSS IVFMD FAMILY, Bệnh viện Đa khoa Gia Đình Đà Nẵng
Giới thiệu
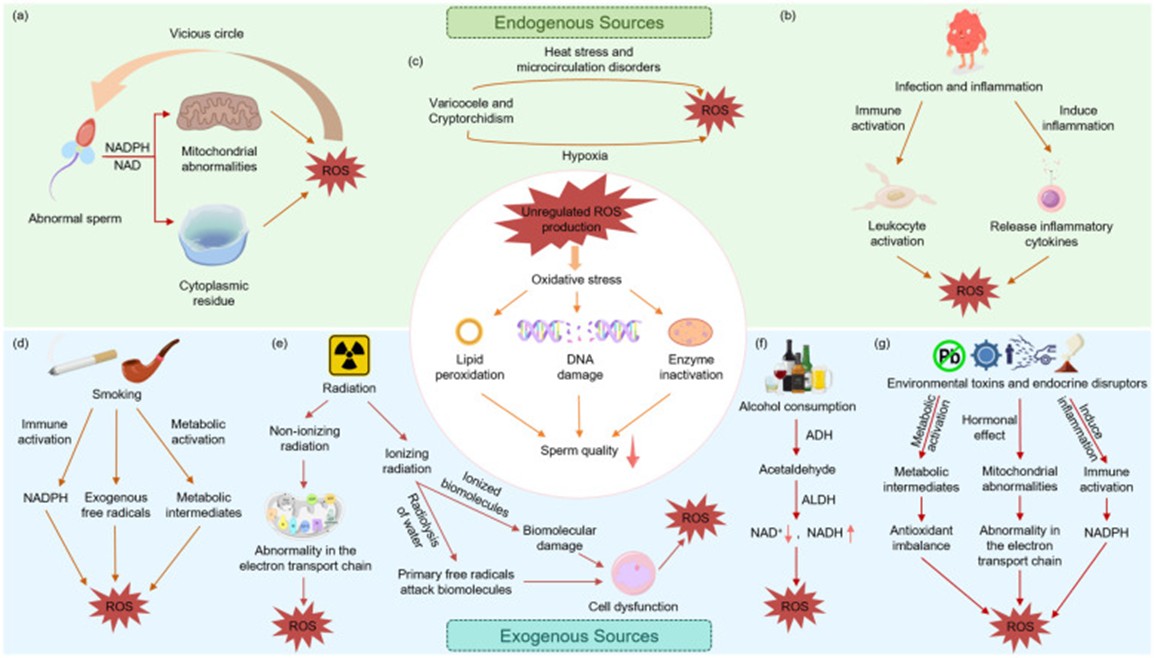
Tinh trùng yếu, một nguyên nhân hàng đầu gây vô sinh nam, có liên quan chặt chẽ với stress oxy hóa (oxidative stress-OS), phản ánh sự mất cân bằng giữa sản xuất các gốc oxy phản ứng (reactive oxygen species-ROS) và khả năng chống oxy hóa. ROS có nguồn gốc từ cả nguồn nội sinh (ví dụ: viêm nhiễm) và tiếp xúc ngoại sinh (ví dụ: lối sống và ô nhiễm môi trường). Ở cấp độ sinh lý, ROS tham gia vào các quá trình quan trọng như tăng sinh tinh trùng, trưởng thành, hoạt hóa, phản ứng acrosome và thụ tinh. Tuy nhiên, ROS quá mức sẽ gây hại, làm tổn thương lipid màng tinh trùng, tính toàn vẹn DNA và chức năng ty thể, cuối cùng dẫn đến giảm khả năng vận động của tinh trùng và suy giảm khả năng sinh sản. Việc hiểu biết một cách có hệ thống về nguồn gốc và cơ chế của ROS trong tinh trùng yếu là điều cần thiết để phát triển các biện pháp can thiệp có mục tiêu [1]. Bài tổng quan này nhấn mạnh sự tích hợp toàn diện của nhiều nguồn ROS và tác động gây hại đa cấp của chúng, đặc biệt tập trung vào rối loạn chức năng ty thể như một cơ chế trung tâm trong tổn thương tinh trùng do OS gây ra.
Nguồn gốc của ROS
-
Nguồn gốc nội sinh
Tinh trùng tạo ra ROS thông qua hai con đường chính: một là liên quan đến nicotinamide adenine dinucleotide phosphate (NADPH) oxidase bị khử nằm trên màng sinh chất, và con đường còn lại xảy ra thông qua các phản ứng oxy hóa khử phụ thuộc nicotinamide adenine dinucleotide (NAD) [1]. Trong quá trình sinh tinh, sự đẩy ra khỏi tế bào chất bị khiếm khuyết dẫn đến việc giữ lại tế bào chất dư thừa (excess residual cytoplasm-ERC), dẫn đến tinh trùng bất thường về mặt hình thái. Những giọt tế bào chất còn sót lại này rất giàu các enzyme chuyển hóa như glucose-6-phosphate dehydrogenase (G6PD) và NADPH oxidase, có thể liên tục kích hoạt các con đường sản xuất ROS và làm tăng đáng kể nồng độ ROS [2].
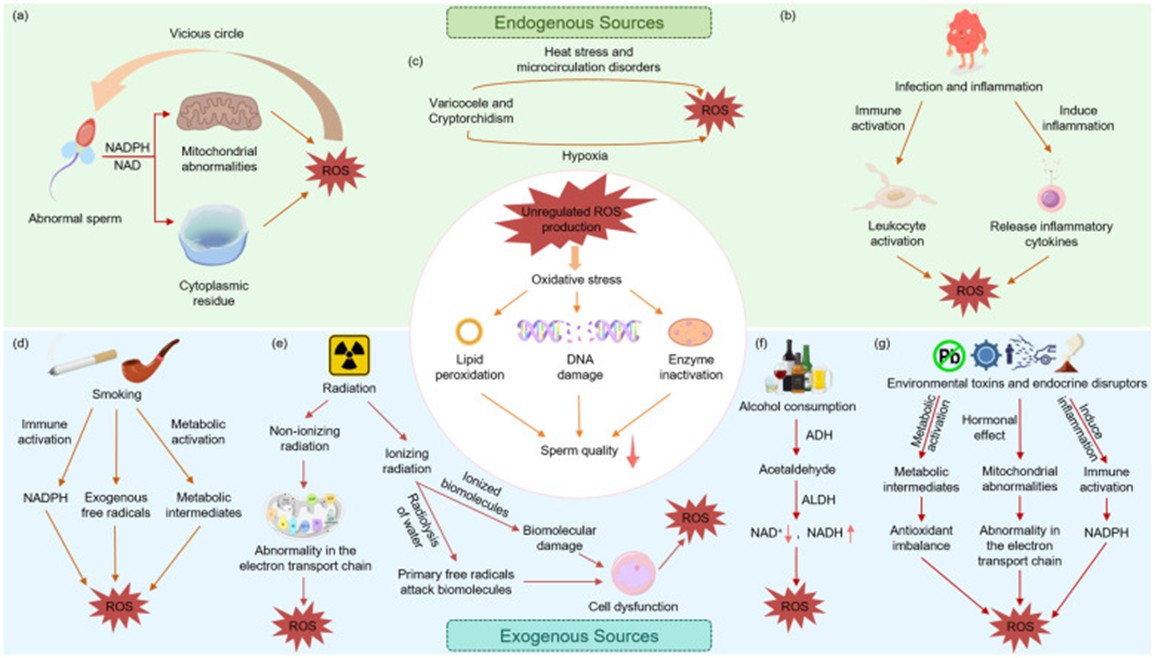
Hình 1. Sự hình thành ROS dư thừa do các nguồn nội sinh và ngoại sinh [1].
Viêm và nhiễm trùng là một nguồn nội sinh lớn khác của ROS. Bạch cầu hoạt hóa tạo ra một lượng lớn ROS thông qua "sự bùng nổ hô hấp" (respiratory burst), một cơ chế phòng vệ miễn dịch có thể làm tăng sản xuất ROS theo cấp số nhân so với mức cơ bản. Quá trình này được khuếch đại thêm thông qua con đường pentose phosphate, giúp tăng cường tạo ra NADPH và làm trầm trọng thêm OS. Viêm tuyến tiền liệt do vi khuẩn, và các bệnh nhiễm trùng gây bệnh khác có thể gây ra sự gia tăng ROS phụ thuộc vào bạch cầu. Viêm tuyến tiền liệt mãn tính không do vi khuẩn (không do nhiễm trùng) cũng có liên quan chặt chẽ với việc tăng mức OS trong tinh dịch. Hơn nữa, dưới sự kích thích của các cytokine gây viêm (ví dụ IL-6, IL-8, TNF-α), cả tế bào sinh tinh và tế bào soma trong tinh hoàn đều có thể góp phần vào việc sản xuất quá mức ROS và làm giảm khả năng chống oxy hóa, dẫn đến tổn thương oxy hóa [1].
Một số rối loạn sinh sản ở nam giới cũng có liên quan chặt chẽ với mức ROS tăng cao. Giãn tĩnh mạch thừng tinh, đặc trưng bởi nhiệt độ tinh hoàn tăng cao và tình trạng thiếu oxy cục bộ, có thể gây ra stress oxy hóa và làm suy giảm chức năng tinh hoàn [3]. Các nghiên cứu đã chỉ ra rằng mức ROS và peroxy hóa lipid tăng cao đáng kể trong tinh dịch của những bệnh nhân bị ảnh hưởng, có mối tương quan thuận với tỷ lệ phân mảnh DNA của tinh trùng. Ngay cả sau khi phẫu thuật điều chỉnh thông qua phẫu thuật cố định tinh hoàn, những bệnh nhân bị ẩn tinh hoàn vẫn tiếp tục biểu hiện tăng sản xuất ROS và làm trầm trọng thêm tổn thương DNA. Mặt khác, xoắn tinh hoàn gây ra tổn thương tinh hoàn thông qua tổn thương do thiếu máu cục bộ, dẫn đến thâm nhiễm bạch cầu và bùng phát các gốc tự do, cuối cùng làm suy giảm quá trình sinh tinh [4].
Rối loạn nội tiết và chuyển hóa cũng góp phần gây tổn thương sinh tinh do ROS. Đái tháo đường có liên quan đến sự gia tăng tổn thương DNA do oxy hóa trong tinh trùng. Các bệnh lý toàn thân như bệnh thận mạn tính và bệnh hemoglobin (ví dụ bệnh thalassemia β) cũng có thể gây tổn thương tinh trùng do oxy hóa do giảm khả năng chống oxy hóa [5]. Các cơ chế này cùng nhau dẫn đến suy giảm tính toàn vẹn của màng tinh trùng, phân mảnh DNA và bất thường chức năng, và thậm chí có thể ảnh hưởng đến sự phục hồi chức năng sinh sản sau khi phẫu thuật nối lại ống dẫn tinh [6].
-
Nguồn gốc ngoại sinh
Các nguồn ROS ngoại sinh chủ yếu bao gồm các yếu tố vật lý, hóa học và lối sống. Lối sống không lành mạnh có thể kích hoạt sản xuất ROS quá mức thông qua hoạt hóa tế bào miễn dịch, làm cạn kiệt dự trữ chất chống oxy hóa và thúc đẩy các phản ứng oxy hóa. Hút thuốc làm tăng số lượng bạch cầu trong tinh dịch lên 48% và nâng mức ROS lên 107%, đồng thời làm giảm khả năng chống oxy hóa tổng thể, cuối cùng dẫn đến apoptosis tế bào mầm và tổn thương DNA [7]. Kim loại nặng trong thuốc lá làm tăng thêm mức ROS và làm suy giảm khả năng vận động của tinh trùng. Uống rượu, thông qua chất chuyển hóa acetaldehyde, cũng thúc đẩy sự tạo ra ROS và làm suy yếu chức năng của tinh trùng [1].
Tinh hoàn, vốn phụ thuộc vào cơ chế điều hòa nhiệt độ bề mặt, đặc biệt nhạy cảm với bức xạ không ion hóa. Các nghiên cứu chỉ ra rằng việc tiếp xúc với bức xạ không ion hóa như bức xạ điện thoại di động có thể làm tăng nhiệt độ bìu, giảm hoạt động của enzyme chống oxy hóa, phá vỡ chức năng ty thể và thúc đẩy sự hình thành ROS trong huyết tương tinh dịch, cuối cùng dẫn đến tổn thương DNA và làm suy giảm các thông số tinh trùng [4]. Trường điện từ tần số vô tuyến, thông qua cả tác động nhiệt và phi nhiệt, can thiệp vào chuỗi vận chuyển điện tử và màng tế bào, gây ra stress oxy hóa và phân mảnh DNA, đồng thời làm suy yếu chức năng sinh steroid [8].
Các tác nhân hóa học là một nguồn ROS ngoại sinh đáng kể khác. Các hóa chất gây rối loạn nội tiết (ví dụ: phthalate) từ các sản phẩm công nghiệp và nhựa, cũng như các kim loại nặng (ví dụ: chì, cadmium và thủy ngân), có thể xâm nhập vào cơ thể con người qua nhiều con đường khác nhau. Các hợp chất này gây ra sự sản sinh ROS quá mức bằng cách làm cạn kiệt các chất chống oxy hóa, kích hoạt các hệ thống enzyme tạo ra ROS (ví dụ: NADPH oxidase) và gây rối loạn chức năng ty thể, cuối cùng làm suy giảm quá trình sinh tinh và chất lượng tinh trùng [9].
Mặc dù có nguồn gốc đa dạng, cả yếu tố nội sinh và ngoại sinh đều hội tụ trên một con đường gây bệnh chung: bằng cách gây rối loạn chức năng ty thể, kích hoạt hệ thống enzyme sản xuất ROS, hoặc làm suy yếu khả năng chống oxy hóa, chúng dẫn đến sự tích tụ ROS quá mức. Điều này sau đó làm tổn thương tính toàn vẹn của màng tinh trùng, sự ổn định DNA và khả năng vận động, cuối cùng dẫn đến vô sinh nam.
OS: Vai trò kép của ROS và cơ chế gây tổn thương đa mục tiêu ở bệnh nhân tinh trùng yếu
Là những tế bào giàu ty thể, tinh trùng cần mức ROS sinh lý để thụ tinh thành công. Tuy nhiên, ROS quá mức gây ra tổn thương nhiều mục tiêu, bao gồm: kích hoạt quá trình peroxy hóa lipid, phá vỡ tính lưu động của màng và tính toàn vẹn về cấu trúc; gây ra sự phân mảnh DNA của nhân và ty thể; làm suy yếu chức năng màng huyết tương; và dẫn đến rối loạn chức năng ty thể với sự suy giảm tổng hợp ATP. Những thay đổi này đặc biệt nổi bật ở những bệnh nhân bị asthenozoospermia. Các cơ chế này góp phần làm giảm khả năng vận động của tinh trùng, khiếm khuyết về chức năng và mất khả năng thụ tinh, tạo thành cơ sở phân tử quan trọng của vô sinh nam. Đáng chú ý, nồng độ chất chống oxy hóa quá cao cũng có thể gây hại bằng cách gây ra căng thẳng khử, gây hại tương tự như OS. Do đó, chìa khóa để quản lý OS nằm ở việc điều chỉnh chính xác cả mức ROS và chất chống oxy hóa [1] [10].
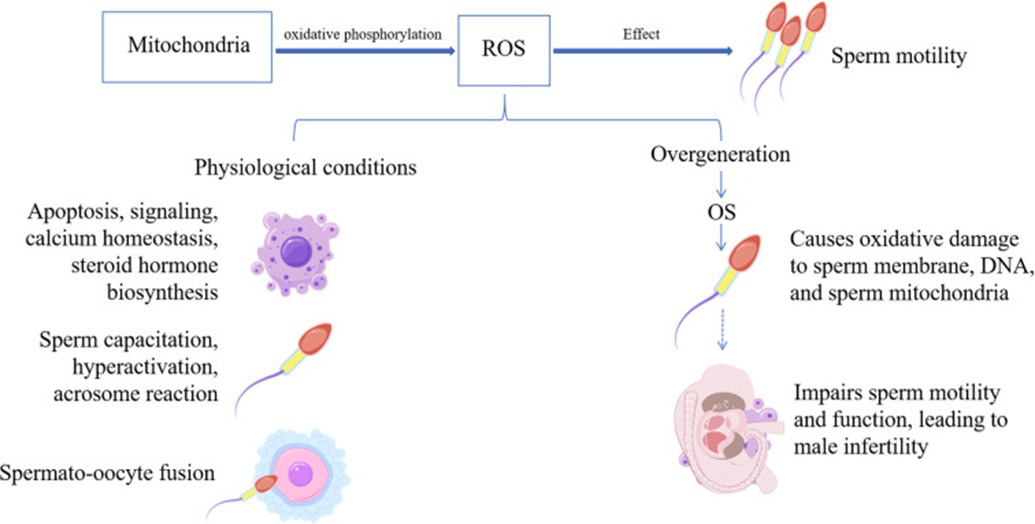
Hình 2. Tác động sinh lý của ROS và mối nguy hiểm khi tăng quá mức [1].
-
Tổn thương oxy hóa ở màng tinh trùng
Màng tinh trùng giàu axit béo không bão hòa đa (polyunsaturated fatty acids-PUFA), các liên kết đôi của chúng làm suy yếu các liên kết C–H liền kề và làm tăng khả năng bị OS. Các protein nhúng màng liên quan đến quá trình truyền tín hiệu, kênh ion và sự kết dính tế bào càng làm tăng thêm tính dễ bị tổn thương của nó trước sự tấn công của quá trình oxy hóa. ROS có nguồn gốc từ nhiều nguồn, bao gồm rò rỉ electron ty thể trong tinh trùng, rối loạn chức năng của các enzyme chống oxy hóa nội sinh và các yếu tố ngoại sinh như hút thuốc hoặc bức xạ [11]. Các phản ứng này gây ra quá trình peroxy hóa lipid, phá vỡ cấu trúc màng, tính lưu động, tính toàn vẹn và chức năng protein. Dẫn đến rối loạn điều hòa ion, gián đoạn tín hiệu và kích hoạt quá trình apoptosis, cuối cùng gây mất khả năng vận động và giảm khả năng thụ tinh. Hơn nữa, quá trình peroxy hóa lipid do OS gây ra làm tổn hại đến tính toàn vẹn của màng ty thể, làm giảm điện thế màng, ức chế tổng hợp ATP và làm thay đổi quá trình chuyển hóa năng lượng của tế bào, do đó tạo ra một vòng tích tụ ROS [12]. Vì vậy, việc duy trì khả năng chống oxy hóa hiệu quả là điều cần thiết cho sức khỏe tinh trùng trong bối cảnh thách thức về môi trường và lối sống. Các biện pháp can thiệp như chế độ ăn uống cân bằng, tập thể dục thường xuyên và tránh tiếp xúc với các tác nhân có hại có thể giúp giảm thiểu tác động tiêu cực của OS đối với chức năng tinh trùng.
-
Tổn thương DNA
Tính toàn vẹn của DNA tinh trùng là điều cần thiết cho quá trình thụ tinh thành công và phát triển phôi khỏe mạnh. Sự thay đổi trong cấu trúc DNA có thể ảnh hưởng trực tiếp đến biểu hiện gen và chức năng protein, do đó làm giảm khả năng thụ tinh. Ở nồng độ sinh lý, ROS hoạt động như các phân tử tín hiệu quan trọng trong các quá trình liên quan đến thụ tinh. Kích thước phân tử nhỏ, tạo ra nhanh chóng và thời gian bán hủy ngắn khiến chúng rất phù hợp làm chất truyền tin nội bào. ROS điều chỉnh khả năng hoạt động, khả năng di chuyển và khả năng liên kết noãn của tinh trùng thông qua kích hoạt con đường cAMP/PKA và tạo điều kiện cho sự hợp nhất tinh trùng-noãn. Tuy nhiên, ROS quá mức phá vỡ cân bằng oxy hóa khử và gây ra các sửa đổi bazơ DNA và đứt gãy chuỗi, đại diện cho một cơ chế chính của sự phân mảnh DNA tinh trùng [13]. OS có thể làm rối loạn sự cân bằng enzyme chống oxy hóa trong cả huyết tương tinh dịch và tinh trùng, làm hỏng cấu trúc và chức năng DNA, làm suy yếu sự ổn định di truyền và làm giảm khả năng thụ tinh thành công [5]. OS cũng có thể can thiệp vào quá trình trao đổi histone thành protamine, dẫn đến sự ngưng tụ chromatin bất thường và suy giảm chức năng tinh trùng. Hơn nữa, các sản phẩm peroxy hóa lipid (lipid peroxidation-LPO), chẳng hạn như aldehyde phản ứng, có thể làm trầm trọng thêm tổn thương DNA hạt nhân và rối loạn chức năng màng, cuối cùng cản trở quá trình thụ tinh [1].
Khả năng di chuyển của tinh trùng phụ thuộc rất nhiều vào nguồn cung cấp ATP của ty thể, và tính toàn vẹn của DNA ty thể (mtDNA) rất quan trọng đối với quá trình chuyển hóa năng lượng. Nằm trong ma trận ty thể, mỗi ty thể chứa một hoặc nhiều bản sao của mtDNA được di truyền từ mẹ. So với DNA nhân, mtDNA thiếu sự bảo vệ của histone, có khả năng sửa chữa hạn chế và dễ bị đột biến hơn, với tỷ lệ đột biến cao hơn khoảng 10–20 lần so với DNA nhân [14]. Nồng độ ROS tăng cao có thể gây tổn hại trực tiếp đến mtDNA, gây đứt sợi và đột biến làm suy yếu quá trình phiên mã và sao chép của nó, cuối cùng làm gián đoạn quá trình tổng hợp protein phosphoryl hóa oxy hóa và làm ảnh hưởng đến cân bằng năng lượng. Khi tỷ lệ mtDNA đột biến vượt quá ngưỡng quan trọng, sản lượng năng lượng của tế bào sẽ giảm, dẫn đến rối loạn chức năng tinh trùng và các biểu hiện lâm sàng liên quan. Nhiều nghiên cứu đã xác định được đột biến mtDNA ở nam giới vô sinh ảnh hưởng đến các gen liên quan đến con đường phosphoryl hóa oxy hóa. Những đột biến này dẫn đến tổng hợp ATP không đủ, khả năng vận động của tinh trùng giảm đáng kể và khả năng sinh sản giảm [15].
Tổn thương DNA do OS gây ra đóng vai trò trung tâm trong cơ chế bệnh sinh của chứng asthenozoospermia, không chỉ đơn thuần là sự gián đoạn di truyền mà còn là các cơ chế đa chiều góp phần gây ra chứng suy giảm khả năng vận động của tinh trùng. Các quá trình liên kết này dẫn đến sự thiếu hụt các protein cấu trúc thiết yếu cho chuyển động roi, gián đoạn cung cấp năng lượng và rối loạn điều hòa các đường dẫn truyền tín hiệu, từ đó làm sáng tỏ cơ sở phân tử của chứng suy giảm khả năng vận động trong chứng asthenozoospermia. Các chiến lược nhằm bảo vệ và sửa chữa tổn thương DNA do oxy hóa có thể mang lại các mục tiêu điều trị quan trọng để cải thiện khả năng vận động của tinh trùng.
-
Tổn thương oxy hóa với chức năng ty thể của tinh trùng
Khả năng vận động của tinh trùng phụ thuộc rất nhiều vào ATP được tạo ra thông qua quá trình phosphoryl hóa oxy hóa ty thể, và sự suy yếu của quá trình này dẫn trực tiếp đến giảm sức sống của tinh trùng và vô sinh nam. Các yếu tố như quá tải Ca2 + ty thể hoặc thiếu hụt cytochrome c có thể gây rò rỉ electron từ chuỗi vận chuyển electron, dẫn đến sản xuất ROS quá mức và OS kéo dài. Ngoài ra, tính toàn vẹn của màng ty thể bị tổn hại và các bất thường ở lớp vỏ xơ có thể ảnh hưởng xấu đến chức năng và quá trình thụ tinh của tinh trùng. Nồng độ ROS tăng cao có thể làm thay đổi oxy hóa các enzym hô hấp quan trọng, chẳng hạn như succinate dehydrogenase và cytochrome c oxidase, làm suy yếu hoạt động xúc tác và chức năng truyền electron của chúng [16]. Hơn nữa, OS thúc đẩy giải phóng các yếu tố ủng hộ apoptosis như cytochrome c từ ty thể, kích hoạt các con đường apoptosis phụ thuộc caspase và kích hoạt quá trình chết theo chương trình của tinh trùng.
Tóm lại, OS góp phần đáng kể vào quá trình sinh bệnh của chứng asthenozoospermia bằng cách làm suy yếu chức năng ty thể và phá vỡ cân bằng nội mô. Một mặt, ROS gây mất điện thế màng ty thể, ức chế tổng hợp ATP và gây ra suy giảm năng lượng, làm khuếch đại thêm sự tích tụ ROS. Đồng thời, OS làm rối loạn điều hòa mitophagy - bằng cách hoạt hóa quá mức dẫn đến thoái hóa ty thể khỏe mạnh, hoặc bằng cách làm suy yếu cơ chế thanh thải dẫn đến tích tụ các bào quan bị tổn thương - do đó làm trầm trọng thêm tổn thương oxy hóa và tín hiệu apoptosis. Các quá trình này tạo thành một vòng luẩn quẩn tự khuếch đại, cuối cùng dẫn đến giảm khả năng vận động của tinh trùng, khiếm khuyết chức năng và mất khả năng thụ tinh. Do đó, việc phục hồi chức năng ty thể và cân bằng mitophagic có thể là một chiến lược điều trị đầy hứa hẹn cho chứng asthenozoospermia.
Chiến lược chống oxy hóa và ứng dụng lâm sàng
Chất chống oxy hóa được phân loại thành hai nhóm chính dựa trên hoạt động và cấu trúc hóa học của chúng: chất chống oxy hóa bằng enzym và không bằng enzym. Chất chống oxy hóa bằng enzym dựa vào các nguyên tố vi lượng như kẽm, sắt, magie và đồng làm cofactor để xúc tác quá trình chuyển đổi ROS thành hydrogen peroxide và sau đó khử nó thành nước. Quá trình này bảo vệ tinh trùng khỏi quá trình peroxy hóa lipid và OS, do đó giúp duy trì khả năng vận động và sức sống của tinh trùng [17].
Các chất chống oxy hóa không phải enzym, chẳng hạn như vitamin C, vitamin E và melatonin, làm giảm tổn thương oxy hóa bằng cách trung hòa trực tiếp các gốc tự do và làm gián đoạn các phản ứng dây chuyền. Các nghiên cứu đã chỉ ra rằng tinh trùng có nồng độ ROS cao thường biểu hiện hàm lượng vitamin C giảm. Là chất chống oxy hóa hòa tan trong nước chính trong dịch ngoại bào, vitamin C không chỉ ức chế sự tạo ra ROS mà còn bảo vệ tính toàn vẹn của DNA tinh trùng bằng cách tái tạo tocopherol bị oxy hóa và loại bỏ các gốc hydroxyl. Vitamin E, chủ yếu bao gồm tocopherol và tocotrienol, có nhiều trong mầm lúa mì, quả bơ và dầu thực vật. Nhóm hydroxyl phenolic của nó phản ứng trực tiếp với các gốc peroxyl lipid, do đó ngăn chặn sự tiến triển của quá trình phân hủy lipid màng. Hơn nữa, sự kết hợp của vitamin C và E cho thấy tác dụng bảo vệ hiệp đồng, bảo vệ hiệu quả hơn chống lại tổn thương peroxy hóa và đứt gãy chuỗi DNA [18].
Nhiều thử nghiệm lâm sàng đã chứng minh tác dụng có lợi của việc bổ sung chất chống oxy hóa trong việc làm giảm OS ở những bệnh nhân bị asthenozoospermia. Các hợp chất như L-carnitine, axit folic và coenzyme Q10 (CoQ10) đã được chứng minh là làm giảm đáng kể sự phân mảnh DNA của tinh trùng đồng thời cải thiện mật độ tinh trùng và khả năng di chuyển tổng thể. Một nghiên cứu của Ý đã báo cáo rằng khả năng di chuyển của tinh trùng tăng trung bình khoảng 20% sau khi can thiệp bằng chất chống oxy hóa. Các nghiên cứu khác cũng chỉ ra rằng việc bổ sung chất chống oxy hóa cải thiện số lượng tinh trùng, hình thái và mức OS, kèm theo tỷ lệ thụ tinh cao hơn và tỷ lệ phôi chất lượng cao tăng lên. Phần lớn các nghiên cứu đã công bố đều ủng hộ vai trò của liệu pháp chống oxy hóa trong việc cải thiện các thông số tinh trùng và kết quả mang thai [19]. Tuy nhiên, vẫn tồn tại những điểm không nhất quán đáng kể và thậm chí là những kết luận trái ngược nhau giữa các thử nghiệm lâm sàng khác nhau. Bất chấp những tranh cãi hiện tại, can thiệp chống oxy hóa vẫn là một trong những phương pháp điều trị chính cho chứng vô sinh nam liên quan đến OS. Tuy nhiên, cần lưu ý rằng việc bổ sung quá mức có thể gây ra “căng thẳng khử”, có thể ảnh hưởng xấu đến chức năng tế bào. Do đó, trên lâm sàng, nên sử dụng các chế độ chống oxy hóa kết hợp liều vừa phải để cân bằng hiệu quả và độ an toàn.
Liệu pháp chống oxy hóa hứa hẹn mang lại nhiều triển vọng trong việc kiểm soát chứng asthenozoospermia, mặc dù hiểu biết hiện tại về mối quan hệ liều lượng, đáp ứng và cơ chế của nó vẫn chưa đầy đủ. Nghiên cứu trong tương lai nên tập trung vào việc làm rõ hiệu quả và cơ chế của các chất chống oxy hóa và liều lượng cụ thể, cũng như khám phá các chiến lược điều trị tích hợp kết hợp chất chống oxy hóa với các phương pháp khác chẳng hạn như thay đổi lối sống, tác nhân dược lý và công nghệ hỗ trợ sinh sản để mở ra những hướng đi mới nhằm cải thiện tình trạng vô sinh nam.
Kết luận
Tóm lại, OS và rối loạn chức năng ty thể là trọng tâm của cơ chế sinh bệnh của asthenozoospermia. Nghiên cứu trong tương lai nên ưu tiên xác định ngưỡng ROS sinh lý-bệnh lý, thiết lập các khuôn khổ chẩn đoán chuẩn hóa, xác nhận các can thiệp cá nhân hóa và đánh giá triển vọng các liệu pháp mới.
Tài liệu tham khảo
1. Mo, L., Wu, H., Zhang, M., Zhang, P., Peng, W., He, Y., & Gao, F. (2025). The mechanism of oxidative stress in asthenozoospermia and antioxidant strategies: A review. Frontiers in Endocrinology, 16, 1670762. https://doi.org/10.3389/fendo.2025.1670762
2. Said, T. M., Agarwal, A., Sharma, R. K., Thomas, A. J., & Sikka, S. C. (2005). Impact of sperm morphology on DNA damage caused by oxidative stress induced by beta-nicotinamide adenine dinucleotide phosphate. Fertility and Sterility, 83(1), 95–103. https://doi.org/10.1016/j.fertnstert.2004.06.056
3. Agarwal, A., Prabakaran, S., & Allamaneni, S. S. S. R. (2006). Relationship between oxidative stress, varicocele and infertility: A meta-analysis. Reproductive Biomedicine Online, 12(5), 630–633. https://doi.org/10.1016/s1472-6483(10)61190-x
4. Aitken, R. J., Gibb, Z., Baker, M. A., Drevet, J., & Gharagozloo, P. (2016). Causes and consequences of oxidative stress in spermatozoa. Reproduction, Fertility, and Development, 28(1–2), 1–10. https://doi.org/10.1071/RD15325
5. Scholze, A., Jankowski, J., Pedraza-Chaverri, J., & Evenepoel, P. (2016). Oxidative Stress in Chronic Kidney Disease. Oxidative Medicine and Cellular Longevity, 2016, 8375186. https://doi.org/10.1155/2016/8375186
6. Patel, A. P., & Smith, R. P. (2016). Vasectomy reversal: A clinical update. Asian Journal of Andrology, 18(3), 365–371. https://doi.org/10.4103/1008-682X.175091
7. Effect of Oxidative Stress on Male Reproduction—PMC. (n.d.). Retrieved December 1, 2025, from https://pmc.ncbi.nlm.nih.gov/articles/PMC4026229/
8. The effects of radiofrequency electromagnetic radiation on sperm function—PubMed. (n.d.). Retrieved December 1, 2025, from https://pubmed.ncbi.nlm.nih.gov/27601711/
9. The Disappearing Sperms: Analysis of Reports Published Between 1980 and 2015—PMC. (n.d.). Retrieved December 1, 2025, from https://pmc.ncbi.nlm.nih.gov/articles/PMC5675356/
10. Mai, Z., Yang, D., Wang, D., Zhang, J., Zhou, Q., Han, B., & Sun, Z. (2024). A narrative review of mitochondrial dysfunction and male infertility. Translational Andrology and Urology, 13(9), 2134–2145. https://doi.org/10.21037/tau-24-262
11. Villaverde, A. I. S. B., Netherton, J., & Baker, M. A. (2019). From Past to Present: The Link Between Reactive Oxygen Species in Sperm and Male Infertility. Antioxidants, 8(12), 616. https://doi.org/10.3390/antiox8120616
12. Mitochondrial Dysfunction and Oxidative Stress in Alzheimer’s Disease—PMC. (n.d.). Retrieved December 1, 2025, from https://pmc.ncbi.nlm.nih.gov/articles/PMC7930231/
13. Ribas-Maynou, J., & Yeste, M. (2020). Oxidative Stress in Male Infertility: Causes, Effects in Assisted Reproductive Techniques, and Protective Support of Antioxidants. Biology, 9(4), 77. https://doi.org/10.3390/biology9040077
14. Amor, H., & Hammadeh, M. E. (2022). A Systematic Review of the Impact of Mitochondrial Variations on Male Infertility. Genes, 13(7), 1182. https://doi.org/10.3390/genes13071182
15. Palanichamy, M. G., & Zhang, Y.-P. (2011). Identifying potential pitfalls in interpreting mitochondrial DNA mutations of male infertility cases. The Indian Journal of Medical Research, 134(4), 447–451.
16. Bhatti, J. S., Bhatti, G. K., & Reddy, P. H. (2017). Mitochondrial dysfunction and oxidative stress in metabolic disorders—A Step towards mitochondria based therapeutic strategies. Biochimica et Biophysica Acta, 1863(5), 1066–1077. https://doi.org/10.1016/j.bbadis.2016.11.010
17. Beygi, Z., Forouhari, S., Mahmoudi, E., Hayat, S. M. G., & Nourimand, F. (2021). Role of Oxidative Stress and Antioxidant Supplementation in Male Fertility. Current Molecular Medicine, 21(4), 265–282. https://doi.org/10.2174/1566524020999200831123553
18. Rahimlou, M., Sohaei, S., Nasr-Esfahani, M., & Nouri, M. (2019). Dietary Antioxidant Intake in Relation to Semen Quality Parameters in Infertile Men: A Cross-Sectional Study. Clinical Nutrition Research, 8(3), 229–237. https://doi.org/10.7762/cnr.2019.8.3.229
19. Agarwal, A., Cannarella, R., Saleh, R., Harraz, A. M., Kandil, H., Salvio, G., Boitrelle, F., Kuroda, S., Farkouh, A., Rambhatla, A., Zini, A., Colpi, G., Gül, M., Kavoussi, P., Hamoda, T. A.-A. A.-M., Ko, E., Calik, G., Toprak, T., Pinggera, G.-M., … Shah, R. (2023). Impact of Antioxidant Therapy on Natural Pregnancy Outcomes and Semen Parameters in Infertile Men: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. The World Journal of Men’s Health, 41(1), 14–48. https://doi.org/10.5534/wjmh.220067