Tin chuyên ngành
on Tuesday 21-07-2020 9:17am
Danh mục: Vô sinh & hỗ trợ sinh sản
ThS. Võ Như Thanh Trúc – Chuyên viên phôi học – IVFAS
Trong phần 1 của bài về cơ chế phân tử của quá trình trưởng thành noãn, chúng ta đã bàn về cơ chế trưởng thành noãn đến giai đoạn NST đóng xoắn cực đại. Trong phần này, chúng ta sẽ tìm hiểu về các giai đoạn tiếp theo của quá trình trưởng thành noãn.
(3). Hình thành hệ thống spindle:
Hệ thống spindle là một hỗn hợp các vi ống được cấu tạo bởi β- tubulin và được tích hợp với các protein cấu trúc khác (motor protein), được hình thành tại thời điểm chuyển tiếp giữa giảm phân I và giảm phân II. Spindle đóng vai trò quan trọng trong sự tập hợp cũng như phân chia các NST trong quá trình phân bào. Sau khi các NST đạt trạng thái co xoắn cực đại, protein kinetochore trong tế bào chất của noãn đến gắn với NST ở tâm động. Quá trình này xảy ra nhờ một số các con đường truyền tín hiệu rất phức tạp liên quan mật thiết đến chu trình tế bào của noãn, và đây là quá trình rất cần thiết trong việc hình thành cấu trúc hoàn chỉnh của NST một cách chính xác [3].
Có nhiều cơ chế hình thành hệ thống spindle, tùy thuộc vào loài và tùy thuộc vào loại tế bào. Hầu hết các tế bào động vật đều hình thành hệ thống spindle dựa vào trung thể hoặc các protein thuộc họ MTOC (MicroTubule - Organizing Center) để từ các phân tử/ cấu trúc này hình thành nên các vi ống và gắn vào NST. Nhưng noãn là tế bào đặc biệt không chứa trung thể hoặc các protein MTOC, một số giả thuyết cho rằng trong quá trình phát triển của noãn, các cấu trúc này đã bị thoái hóa. Chính vì thế, noãn có cơ chế riêng để hình thành hệ thống spindle. Quá trình hình thành spindle của noãn diễn ra từ cuối prophase I đến metaphase I. Sau khi kinetochore gắn vào tâm động để hoàn thiện cấu trúc cuộn xoắn cực đại của NST, chính ái lực của nó thu hút các vi ống tự do trong tế bào chất noãn tập trung quanh NST sao cho các đầu (+) của vi ống ở gần NST và các đầu (-) hướng ra ngoài. Đầu (+) của vi ống là nơi các đơn phân tubulin tự do đến gắn vào để kéo dài vi ống, đầu (-) là đầu được kí hiệu để dễ dàng phân biệt với đầu (+). Đầu (+) luôn được gắn mũ chụp GTP (guanine triphosphate) nên thu hút các tubulin tự do có ái lực với GTP (luôn tồn tại dưới dạng liên kết với GTP). Lúc này, protein Ran-GTPase đến thực hiện hoạt tính enzyme thủy phân của nó, giúp thủy phân phân tử GTP mũ chụp của đầu (+), giúp cho các tubulin tự do chuyển thành dạng liên kết với GDP và gắn với các tubulin dạng liên kết khác trong vi ống, kéo dài vi ống (hình 2.3) [6].
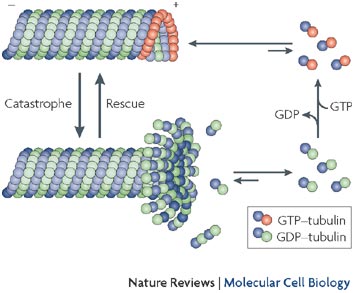
Hình 2.3. Cơ chế kéo dài vi ống
Đồng thời với quá trình kéo dài vi ống, các motor protein luôn gắn với vi ống như kinesin và dynein hỗ trợ quá trình chuyển động tịnh tiến các vi ống này sao cho đầu (+) luôn được giữ gần NST và đầu (-) có xu hướng tụ lại với nhau. Kết quả của quá trình di chuyển tịnh tiến này là tạo ra hệ thống spindle lưỡng cực dạng hình trụ. Sau cùng, một số vi ống liên kết hoàn toàn với kinetochore ở tâm động NST với sự hỗ trợ của một số protein khác trong tế bào chất noãn [11], kéo các NST sắp thành một hàng dọc tại mặt phẳng xích đạo của cấu trúc spindle, sẵn sàng cho sự phân ly NST ở anaphase I (hình 2.4).
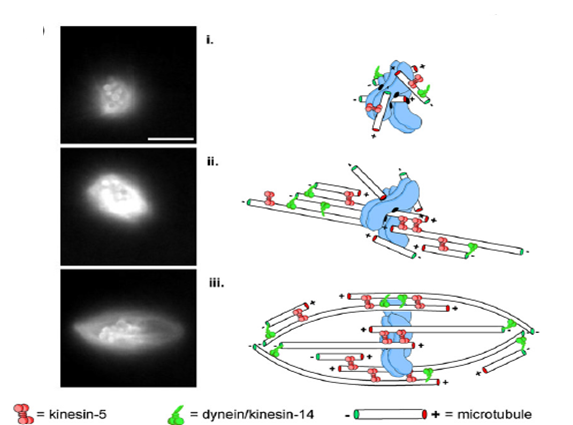
Hình 2.4. Cơ chế hình thành hệ thống spindle với ảnh chụp với tubulin được đánh dấu huỳnh quang (hình bên trái) và hình mô phỏng quá trình hình thành spindle (hình bên phải)
(3)Phân chia các cặp NST tương đồng về hai cực tế bào:
Sau khi đầu (+) của vi ống gắn với kinetochore, phức hợp APC/C (Anaphase Promoting Complex/ Cyclosome) cho phép tế bào bước vào anaphase I. Lúc này, kinetochore thể hiện hoạt tính thủy phân các tubulin ở đầu (+) vi ống [3]. Do đầu (-) đã được cố định trong cấu trúc của hệ thống spindle nên khi đầu (+) bị thủy phân, vi ống ngắn dần, mang theo NST di chuyển về hai cực của hệ thống spindle.
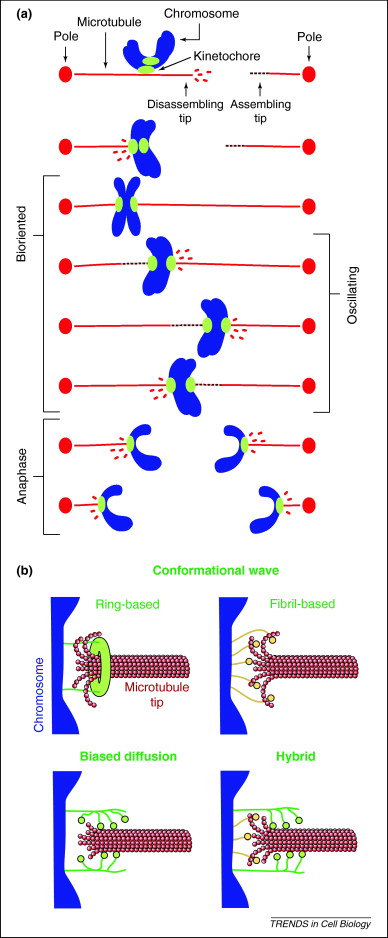
Hình 2.5. NST phân ly về hai cực của spindle [4]
(4) Phóng thích thể cực:
Từ cuối metaphase I, sau khi hệ thống spindle được hình thành hoàn thiện và nằm sát màng noãn, các vi ống trong spindle tương tác với các protein actin và myosin khung xương tế bào, hình thành cấu trúc vòng nhẫn actinomyosin (hình 2.6A) và hình thành chồi nhú trên màng noãn, nơi mà sau này sẽ phóng thích thể cực (hình 2.6B).
Đến anaphase I, chỉ một số vi ống gắn với kinetochore trên NST bị ngắn dần do bị thủy phân, những vi ống còn lại không liên kết với NST vẫn giữ nguyên vị trí. Do đó, khi NST phân ly về hai cực của hệ thống spindle sẽ làm xuất hiện khoảng trống trên mặt phẳng xích đạo của spindle. Chính khoảng trống này tương tác với các protein khung xương tế bào trên màng noãn, cảm ứng hình thành khe lõm. Quan sát thêm một thời gian xảy ra hiện tượng xoay spindle, sự xoay này cảm ứng hình thành khe lõm thứ hai trên màng noãn. Hai khe lõm này hợp lại với nhau hình thành eo thắt, dẫn đến sự phân chia tế bào chất không đồng đều, phóng thích thể cực ở giai đoạn telophase I [2].
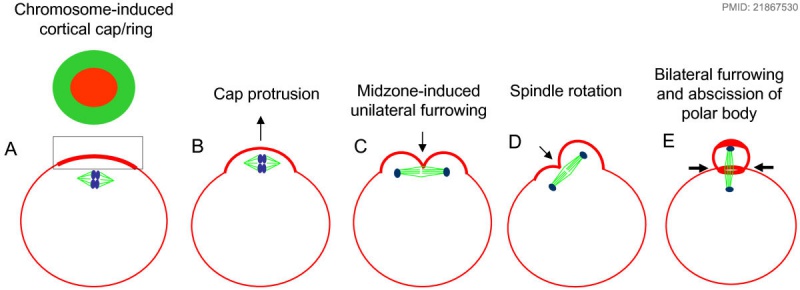
Hình 2.6. Cơ chế hình thành thể cực (từ metaphase I – telophase I)
(5) Meiotic re – arrest:
Tại thời điểm phóng thích thể cực, noãn đã hoàn tất giảm phân I. Do NST vẫn ở giai đoạn đóng xoắn cực đại nên noãn bước qua prophase II rất nhanh chóng. Chu trình giảm phân II cũng trải qua các bước tương tự giảm phân I nhưng chu trình tế bào noãn lại bị bắt giữ lần nữa ở giai đoạn metaphase II. Một số nghiên cứu cho thấy con đường truyền tín hiệu MEK/MAPK trong noãn đóng vai trò điều hòa, kích hoạt các MPF, nồng độ MPF tăng cao cho phép bắt giữ chu trình tế bào noãn tại giai đoạn metaphase của giảm phân II [9]. Một số nghiên cứu cũng cho thấy đường truyền tín hiệu MEK/MAKP cũng phosphoryl hóa, kích hoạt protein Rsk1/2 trong tế bào chất của noãn, protein này sau khi được hoạt hóa sẽ trở thành protein đầu nguồn, khởi phát một đường truyền tín hiệu khác, qua một số các phân tử tín hiệu trung gian chưa biết rõ và kết quả của đường truyền tín hiệu này là phức hợp APC/C bị ức chế, noãn không thể bước qua anaphase II nên bắt buộc phải dừng lại ở metaphase II. Noãn sẽ duy trì trạng thái MII cho đến lúc thụ tinh, nhờ cơ chế hoạt hóa các kênh Ca2+ bởi tinh trùng sẽ khởi phát các đường truyền tín hiệu cho phép phức hợp APC/C hoạt động trở lại [1].
TÀI LIỆU THAM KHẢO
1. Anja Schmitt, A.R.N., Signalling pathways in oocyte meiotic maturation. Journal of Cell Science, 2002. 115: p. 2457 - 2459.
2. Belleannee, C., Extracellular microRNAs from the epididymis as potential mediators of cell-to-cell communication. Asian J Androl, 2015. 17(5): p. 730-6.
3. Chan GK, L.S., Yen TJ, Kinetochore structure and function. Trends Cell Biol, 2005. 15(11): p. 589 - 598.
4. Charles L. Asbury, e.a., Kinetochore's gripping feat: conformational ware or biased diffusion? Trends Cell Biol, 2011. 21(1): p. 38 - 46.
5. Franck Bazile, J.S.-P., Damien D'Amours, Three-step model for condensin activation during mitotic chromosome condensation. Cell Cycle, 2010. 9(16): p. 3263 - 3275.
6. Jesse C.Gatlin, K.B., Microtubule motors in eukaryotic spindle assembly and maintenance. Seminars in Cell and Developmental Biology, 2010. Articles in press.
7. Maul G., S.G., Jimenez S., et al., Detection of nuclear lamin B epitopes in oocyte nuclei from mice, sea urchins, and clams using a human autoimmune serum. Devel Biol, 1987. 121: p. 368 - 375.
8. Racowsky C., B.K., In vitro and in vivo studies reveal that hamster oocyte meiotic arrest is maintained only transiently by follicular fluid, but persistently by membrana/cumulus granulosa cell contact. Devel Biol, 1989. 134: p. 297 - 306.
9. Seang Lin Tan, R.-C.C., William M Buckett, In-vitro maturation of human oocytes: Basic science to clinical application. 2007.
10. Stuurman N., H.S., Aebi U., Nuclear lamins: their structure, assembly, and interactions. J. Struct Biol, 1998. 122: p. 42 - 66.
11. Tanaka K, M.N., Dewar H, et al., Molecular mechanism of kinetochore capture by spindle microtubules. Nature, 2005. 434(7036): p. 987 - 994.
Từ khoá: cơ chế phân tử, trưởng thành nhân noãn, MII, spindle
Mời xem lại phần 1
Các tin khác cùng chuyên mục:
TIN CẬP NHẬT
TIN CHUYÊN NGÀNH
LỊCH HỘI NGHỊ MỚI
Năm 2020
New World Saigon Hotel, thứ bảy ngày 17 tháng 01 năm 2026
Năm 2020
Hội Nội tiết Sinh sản và Vô sinh TP. Hồ Chí Minh (HOSREM) sẽ ...
Năm 2020
Khách sạn Equatorial, chủ nhật ngày 23 . 11 . 2025
GIỚI THIỆU SÁCH MỚI

Ấn phẩm CẬP NHẬT KIẾN THỨC VỀ QUẢN LÝ SỨC KHỎE TUỔI MÃN ...
Y học sinh sản được phát ngày ngày 21 . 9 . 2025 và gởi đến ...
Cẩm nang Hội chứng buồng trứng đa nang được phát hành online ...
FACEBOOK








