CVPH: Nguyễn Thụy Trà My – IVFAS
Hiện nay, việc nuôi cấy noãn trưởng thành in vitro có thể cung cấp một lượng lớn noãn trưởng thành để điều trị vô sinh ở phụ nữ giảm dự trữ buồng trứng cũng như trước khi điều trị ung thư. Quá trình phát triển của noãn là một quá trình phức tạp, đòi hỏi sự điều hòa chủ yếu của các protein có nguồn gốc từ noãn và tế bào hạt cũng như các con đường truyền tín hiệu khác nhau ở các giai đoạn khác nhau. Do đó, việc hiểu được tường tận quá trình sinh noãn và phóng noãn ở mức độ phân tử có thể giúp chúng ta tối ưu được điều kiện nuôi cấy cũng như đánh giá được tác động của gen và sản phẩm gen nhằm đưa ra được phương thuốc điều trị mới để cải thiện khả năng sinh sản ở bệnh nhân vô sinh. Đồng thời, việc hiểu được các con đường truyền tín hiệu cũng như các yếu tố liên quan đến quá trình sinh noãn và phóng noãn cũng có thể giúp chúng ta xác định được các marker tiềm năng về chất lượng noãn.
CÁC GIAI ĐOẠN PHÁT TRIỂN CỦA NANG NOÃN VÀ SỰ SINH NOÃN
Giai đoạn nang nguyên thủy
Noãn có nguồn gốc từ các tế bào mầm nguyên thủy (primordial germ cells – PGCs). Từ tuần 4 - 6 thai kì, các PGCs di chuyển đến gờ sinh dục và bắt đầu nguyên phân để tăng số lượng, tạo ra các nguyên bào noãn. Sự tăng số lượng của PGCs được đặc trưng bởi sự phân bào chưa hoàn chỉnh và tạo ra một nhóm tế bào được gọi là “ổ tế bào gốc” [1, 2]. Tại thời điểm tuần thứ 8 thai kì, nguyên bào noãn bị ảnh hưởng bởi ba quá trình xảy ra đồng thời: (1) một phần nguyên bào noãn sẽ tiếp tục nguyên phân để tăng số lượng (đạt 600.000 nguyên bào noãn vào tuần thứ 8 thai kì và 6 - 7 triệu nguyên bào noãn ở tuần 20 thai kì); (2) một số nguyên bào noãn sẽ bước vào quá trình giảm phân I và sau khi hoàn thành hiện tượng trao đổi chéo giữa các nhiễm sắc thể tương đồng (2n kép), các nguyên bào noãn này sẽ nghỉ, từ tuần 8 - 13 thai kì [2, 3]. Sự khởi đầu của quá trình giảm phân phụ thuộc vào tín hiệu Stra8 và thụ thể axit retinonic (được kích thích bởi retinoic axit gen 8) [3]. Stra8 là yếu tố trong tế bào chất và được biểu hiện trong tế bào mầm dòng giao tử cái khi bước vào pha trước của giảm phân và trong đáp ứng với axit retinoic [1]và (3) một số nguyên bào noãn sẽ thoái hóa dần và mất đi thông qua quá trình apoptosis. Do đó, tại tuần 20 thai kì, số lượng nguyên bào noãn sẽ giảm dần [2].Quá trình hình thành nang noãn xảy ra khi “ổ tế bào gốc” vỡ ra. Cơ chế gây ra sự vỡ “ổ tế bào gốc” vẫn chưa được hiểu rõ [4, 5]. Tuy nhiên, nghiên cứu trên động vật gặm nhấm cho thấy, hormone estrogen có liên quan đến sự duy trì “ổ tế bào gốc” [5, 6]. Bên cạnh đó, các hormone steroid có nguồn gốc từ nguyên bào noãn (GDF9 và BMP15) và một số protein khác như FOXL2 và NOBOX cũng có liên quan đến sự vỡ “ổ tế bào gốc” [7-10](Hình 1).
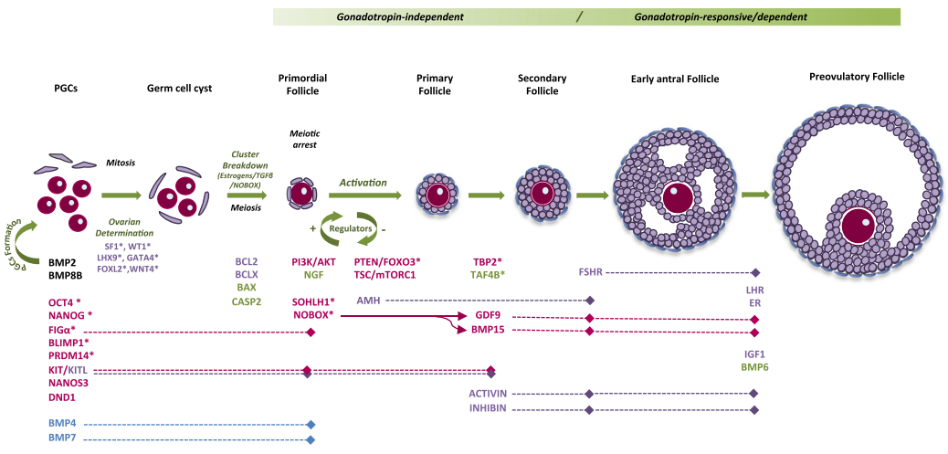
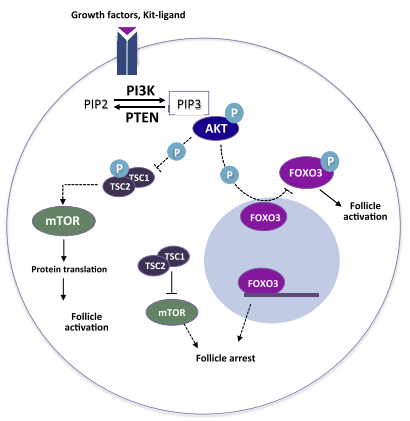
Khi KIT ligand gắn với thụ thể KIT trên màng noãn, con đường tín hiệu PI3K được kích hoạt, dẫn tới protein kinase B (Akt) – protein làm tăng cường sự biệt hóa tế bào và giúp tế bào tồn tại. Tại thời điểm này, Akt được hoạt hóa sẽ cảm ứng đồng thời hai quá trình: (1) làm bất hoạt protein FOXO3 – protein làm ngưng sự phát triển của nang noãn; (2) làm bất hoạt phức hợp TSC1/2. Khi đó, con đường tín hiệu mTOR được kích hoạt và tiến hành phiên mã, dịch mã tạo ra các protein mTOR (protein có vai trò trong tăng sinh và phát triển tế bào ở người). Con đường tín hiệu PI3K/Akt và mTOR làm bất hoạt protein FOXO3 và kích hoạt protein mTOR. Khi đó, quá trình phát triển từ nang noãn nguyên thủy đến nang noãn sơ cấp được khởi phát (Makker và cs, 2014) (Hình 3).
Giai đoạn nang thứ cấp
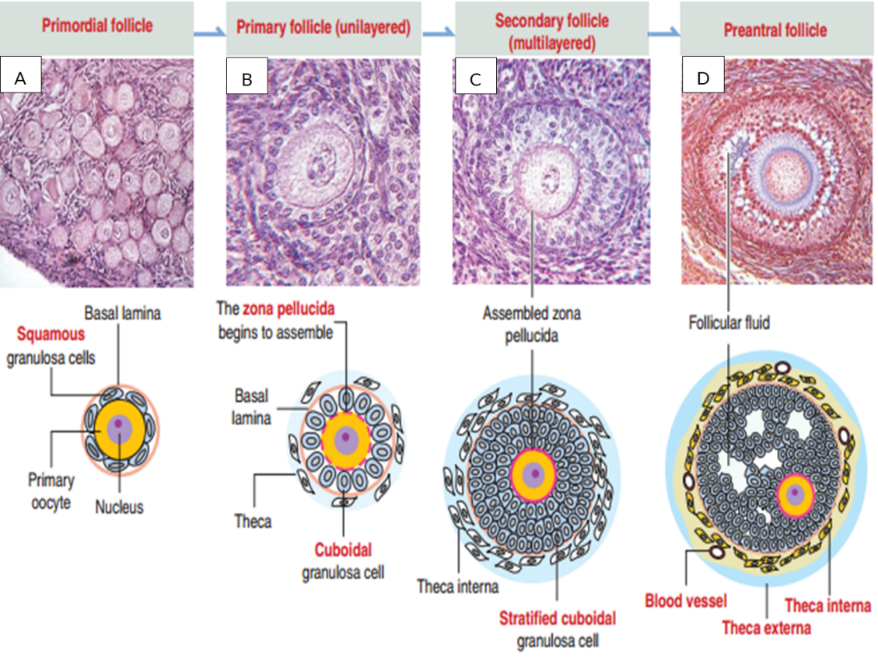
Nang noãn sơ cấp sẽ tiếp tục phát triển đến giai đoạn nang noãn thứ cấp, khi đó, cấu trúc của nang noãn bắt đầu có sự thay đổi (Hình 2-C). Một số sự thay đổi chính trong suốt quá trình phát triển của nang noãn thứ cấp là (1) sự tích lũy của các tế bào hạt và hình thành các lớp tế bào hạt bao quanh noãn và (2) sự phát triển của tế bào vỏ (theca cell) [11].(1) Sự hình thành lớp tế bào hạt bao quanh noãn
Sự phát triển của nang noãn thứ cấp đặc trưng bởi noãn được bao quanh bởi hai lớp tế bào. Một số protein có nguồn gốc từ noãn như GDF9 và BMP15 chịu trách nhiệm trong quá trình tích lũy cũng như sự thay đổi cấu trúc của các tế bào hạt, từ dạng biểu mô vuông đơn sang dạng biểu mô vuông tầng. Khi đó, kích thước của nang noãn cũng có sự thay đổi đáng kể (25-120 μm).
(2) Sự phát triển của tế bào vỏ
Tại thời điểm phát triển của nang noãn thứ cấp, sự hình thành tế bào vỏ bắt đầu khi một vài tế bào giống như chất nền xuất hiện xung quanh lớp lá nền và sự tăng tiết của các protein BMP4 có nguồn gốc từ noãn. Hai lớp cơ bản của tế bào vỏ bao gồm lớp trong (biệt hóa từ tế bào kẽ - theca interstitial cells) và lớp ngoài (biệt hóa từ tế bào cơ trơn – smooth muscle cells). Cũng tại thời điểm này, trong nang noãn bắt đầu có sự hình thành những mạch máu nhỏ xung quanh tế bào vỏ. Do đó, máu được tuần hoàn xung quanh nang noãn và mang các chất dinh dưỡng, gonadotropin và nước cần thiết cho sự phát triển của nang noãn [11].
Tại thời điểm này, noãn vẫn nghỉ ở giai đoạn GV. Nguyên nhân dẫn đến việc noãn duy trì sự nghỉ kéo dài là do nồng độ cAMP nội bào của noãn tăng cao (cAMP là chất tác động trung gian hay chất truyền tín hiệu thứ hai của hormone trong tế bào) [1].
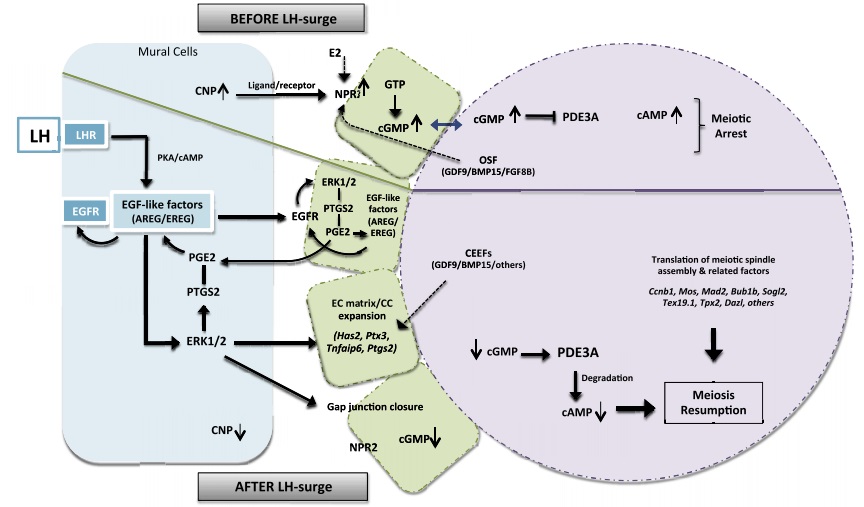
Thụ thể NPR2 (biểu hiện bởi sự điều hòa của noãn) được kích hoạt khi gắn kết với CNP ligand. Khi đó, quá trình chuyển hóa GTP thành cGMP được cảm ứng và toàn bộ cGMP được tạo ra sẽ được thẩm thấu vào noãn thông qua cầu liên bào giữa noãn và tế bào cumulus (protein conexin 37). Điều này làm nồng độ cGMP trong noãn tăng cao dẫn đến enzyme điều hòa và phân giải cAMP bị ức chế (enzyme PDE3A). Kết quả là nồng độ cAMP nội bào tăng cao khiến cho quá trình giảm phân của noãn bị trì hoãn [1](Hình 4).
Giai đoạn nang noãn tiền hốc
Khi nang noãn phát triển đến giai đoạn nang tiền hốc, một số sự kiện đặc trưng cho giai đoạn này là sự hình thành hốc nang noãn và sự biểu hiện của thụ thể FSH trên tế bào hạt [11](Hình 1).
Giả thiết đưa ra để giải thích cho sự hình thành hốc nang noãn là sự tràn vào của nước thông qua các kênh vận chuyển nước trên tế bào hạt (kênh aquaporin). Tế bào hạt sẽ vận chuyển các ion vào bên trong noãn một cách chủ động thông qua cầu liên bào, từ đó tạo ra sự chênh lệch áp suất thẩm thấu ở tế bào hạt. Khi đó, nước từ bên ngoài sẽ tràn vào noãn thông qua kênh đặc biệt – kênh aquaporin [12].Tại giai đoạn nang tiền hốc, tế bào hạt bắt đầu có sự biểu hiện của thụ thể FSH. Sự biểu hiện của thụ thể FSH trên tế bào hạt khởi động quá trình chọn lọc nang thứ cấp và phát triển thành nang vượt trội [1]. Vào đầu chu kỳ kinh nguyệt, nồng độ FSH tăng dần. Trong quá trình phát triển, LH do tuyến yên tiết ra sẽ kích thích tế bào vỏ của nang sản xuất androgen. Androgen được vận chuyển qua tế bào hạt và được men aromatase của tế bào hạt thơm hóa thành estrogen dưới tác động của FSH (đây là cơ chế 2 tế bào – 2 gonadotropin để tổng hợp estrogen). Các nang thứ cấp được chọn lọc sẽ tổng hợp estrogen (chủ yếu là estradiol) ngày càng nhiều làm nồng độ estradiol trong cơ thể tăng dần. Vào khoảng ngày 7 của chu kỳ kinh nguyệt, nồng độ của estradiol tăng quá mức sẽ tạo ra phản hồi âm lên vùng hạ đồi và tuyến yên, ức chế sự tiết GnRH và FSH. Kết quả là nồng độ FSH bắt đầu giảm. Khi nồng độ FSH không còn đủ để tác động lên tất cả các nang thứ cấp đang phát triển, sẽ xảy ra hiện tượng cạnh tranh FSH giữa các nang thứ cấp. Chỉ có nang thứ cấp có số lượng thụ thể với FSH nhiều nhất mới có thể tiếp tục phát triển, trở thành nang duy nhất vượt trội để phát triển thành nang vượt trội (nang de Graff) [11].
Giai đoạn nang de Graff, sự phóng noãn và tạo lập hoàng thể
Vào giữa chu kì kinh, nồng độ FSH vẫn tiếp tục giảm và nồng độ estradiol vẫn tăng đều do nang de Graff tiết ra. Khi nồng độ estradiol tăng đến một ngưỡng đỉnh điểm sẽ tạo ra một phản hồi dương lên vùng hạ đồi tuyến yên. Phản hồi dương này sẽ kích thích tuyến yên tiết ra LH với nồng độ rất cao, gọi là đỉnh LH. Khi xuất hiện đỉnh LH, noãn sẽ nhận tín hiệu và cảm ứng một số sự kiện liên quan đến sự trưởng thành như (1) giãn nở tế bào cumulus; (2) vượt qua sự nghỉ ở giai đoạn GV để tiếp tục hoàn thiện quá trình giảm phân và (3) xảy ra sự phóng noãn.Do noãn không có biểu hiện của thụ thể LH nên sẽ nhận tín hiệu LH thông qua trung gian bởi đường truyền tín hiệu ERK1/2 trên tế bào hạt thành nang. Khi con đường tín hiệu ERK1/2 được kích hoạt, một số gen chịu trách nhiệm cho sự giãn nở tế bào cumulus sẽ được cảm ứng và làm giãn nỡ các cầu nối liên bào giữa các tế bào cumulus với nhau (protein conexin 43). Đồng thời, cầu liên bào giữa tế bào cumulus và noãn cũng bị đóng lại. Điều này làm giảm sự tương tác giữa noãn và tế bào cumulus, khiến nồng độ cGMP trong noãn giảm do không còn được thẩm thấu vào noãn. Khi đó, enzyme PDE3A được kích hoạt và khởi phát phản ứng phân hủy cAMP, từ đó làm giảm nồng độ cAMP nội bào. Kết quả là noãn vượt qua giai đoạn GV và tiếp tục hoàn thiện quá trình giảm phân. Để noãn trưởng thành và vượt qua sự trì hoãn giảm phân, đỉnh LH phải kéo dài tối thiểu 14-27 giờ [1](Hình 4).
Cũng tại thời điểm xuất hiện đỉnh LH, các enzyme cắt có nguồn gốc từ nguyên bào sợi như metalloproteinase và protease được kích hoạt và cắt đứt các sợi collagen ở tế bào vỏ và màng nang noãn, khiến các lớp bao bọc bên ngoài noãn mỏng dần làm máu từ bên ngoài có thể tràn vào khoang chứa dịch. Sự tích tụ dịch nang noãn cùng với sự tràn vào của máu tạo ra sức căng bên trong noãn. Khi trở nên quá căng, noãn sẽ xảy ra hiện tượng phóng noãn [3].
Sau khi phóng noãn, nhóm tế bào còn lại của nang noãn sẽ tạo lập hoàng thể dưới tác động của LH. Hoàng thể sẽ tiết ra progesterone và estrogen để tác động lên nội mạc tử cung, nhằm hỗ trợ cho sự làm tổ của phôi. Nếu không có hiện tượng thụ tinh hay làm tổ xảy ra, hoàng thể sẽ thoái hóa trong vòng 10-12 ngày. Hoàng thể thoái hóa sẽ làm giảm nồng độ progesterone và estrogen, tạo cơ chế phản hồi lên vùng hạ đồi và tuyến yên. Tuyến yên sẽ tăng tiết FSH trở lại vào cuối pha hoàng thể để tiếp tục 1 chu kỳ kích thích mới.
TÀI LIỆU THAM KHẢO
1. Sanchez, F. and J. Smitz, Molecular control of oogenesis. Biochimica et Biophysica Acta. Biochimica et Biophysica Acta, 2012. 1822(12): p. 1896-1912.
2. Strauss, J.F. and R.L. Barbieri, Chapter 9 The ovarian life cycle in Yen & Jaffe’s Reproductive Endocrinology Physiology, Pathophysiology and Clinical Management, J.F. Strauss and C.J. Williams, Editors. 2014, Reproductive endocrinology: USA. p. 158-191.e8.
3. Abraham, K.L. and T.L. Laura, Histology and cell biology: An introduction to pathology, in Chapter 22: Follicle Development and the menstrual cycle, A.L. Kierszenbaum and L.L. Tres, Editors. 2016, Elsevier Saunders: Canada. p. 665-692.
4. Mayo, K., L. Jameson, and T.K. Woodruff, Eggs in the nest. Endocrinology, 2007. 148(8): p. 3577-9.
5. Tingen, C., A. Kim, and T.K. Woodruff, The primordial pool of follicles and nest breakdown in mammalian ovaries. Molecular Human Reproduction, 2009. 15(12): p. 795-803.
6. Jefferson, W., et al., Neonatal genistein treatment alters ovarian differentiation in the mouse: inhibition of oocyte nest breakdown and increased oocyte survival. Biology of Reproduction, 2006. 74(1): p. 161-168.
7. Jefferson, W.N., et al., Neonatal exposure to genistein induces estrogen receptor (ER)alpha expression and multioocyte follicles in the maturing mouse ovary: Evidence for ERbeta-mediated and nonestrogenic actions. Biology of Reproduction, 2002. 67: p. 1285-1296.
8. Rajkovic, A., NOBOX Deficiency Disrupts Early Folliculogenesis and Oocyte-Specific Gene Expression. Science, 2004. 305(5687): p. 1157-1159.
9. Uda, M., et al., Foxl2 disruption causes mouse ovarian failure by pervasive blockage of follicle development. Human Molecular Genetics, 2004. 13(11): p. 1171-1181.
10. Chen, Y., et al., Estradiol, progesterone, and genistein inhibit oocyte nest breakdown and primordial follicle assembly in the neonatal mouse ovary in vitro and in vivo. Endocrinology, 2007. 148(8): p. 3580-90.
11. Williams, C.J. and G.F. Erickson, Morphology and physiology of the ovary National Library of Medicine, 2012. 0: p. 1-39.
12. Rodgers, R.J. and H.F. Irving-Rodgers, Formation of the ovarian follicular antrum and follicular fluid. Biology of Reproduction, 2010. 82(6): p. 1021-1029.
Tiền Hội nghị: Trung tâm Hội nghị Grand Saigon, thứ bảy ngày ...
New World Saigon hotel, thứ bảy 14 tháng 06 năm 2025 (12:00 - 16:00)
Vinpearl Landmark 81, ngày 9-10 tháng 8 năm 2025
Kính mời quý đồng nghiệp quan tâm đến hỗ trợ sinh sản tham ...
Y học sinh sản số 73 (Quý I . 2025) ra mắt ngày 20 . 3 . 2025 và ...
Sách ra mắt ngày 6 . 1 . 2025 và gửi đến quý hội viên trước ...








