-


GIỚI THIỆU VỀ
HOSREM -


THÔNG TIN HỘI VIÊN
CỦA HOSREM -


CUNG CẤP KIẾN THỨC
VỀ Y HỌC -


BÁO CÁO
HỘI NGHỊ
Mục tiêu sáng lập
HOSREM ra đời nhằm tập hợp nhân viên y tế trong lãnh vực chăm sóc sức khỏe sinh sản để phát huy tiềm năng của một trung tâm y tế lớn, tạo điều kiện giao lưu, chia sẻ kinh nghiệm, cập nhật thông tin, góp phần vào sự phát triển của ngành.
Nhiệm vụ chính
Trở thành hội viên của HOSREM?
Kiến thức chuyên ngành sản phụ khoa & vô sinh
Khi càng có nhiều thông tin, bạn sẽ được trang bị kiến thức tốt hơn để đưa ra các quyết định đúng đắn về những vấn đề liên quan đến sức khỏe của mình. Những bài viết, những thông tin ở trang web của HOSREM được biên soạn với mục đích cung cấp kiến thức để Bạn đọc có một cách nhìn tổng quan và công bằng về các vấn đề liên quan đến sức khỏe, nhằm trang bị kiến thức phổ thông nhất về sản phụ khoa và vô sinh. Các chuyên đề HOSREM cung cấp bao gồm:
Sản khoa và nhi sơ sinh.
Phụ khoa.
Mãn kinh.
Nam khoa.
Vô sinh và hỗ trợ sinh sản.
Các thông tin khác.
Hướng dẫn lâm sàng VSRM và tạp chí, ẩn phẩm
Được HOSREM cập nhật thường xuyên bao gồm:
Báo cáo hội nghị







- Tin nổi bậtTin cộng đồng, quốc tế, trong nước
- Tin chuyên ngành Phụ khoa, Mãn kinh, Nam khoa...
- Hoạt độngHội nghị - Hội thảo - Khóa đào tạo
- Sách mớiPhụ san, tập san
miR-6881-3p góp phần làm giảm dự trữ buồng trứng bằng cách điều ...
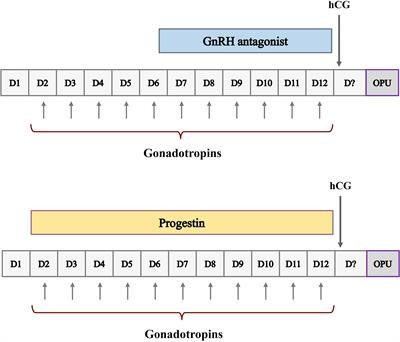
Phác đồ kích thích buồng trứng sử dụng mồi Progestin (PPOS) mang lại ...
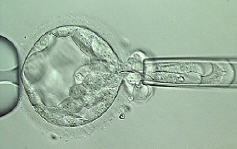
Mối liên quan giữa sự lệch bội của phôi và tổn thương DNA tinh trùng ...
Tác động của thể lệch bội giảm phân có nguồn gốc từ mẹ đến ...
_Bai_dan_NAM_KHOA.jpg)
Giải mã khả năng sinh sản ở nam giới lớn tuổi và các hướng điều ...
_Bai_d.jpg)
Tác động của biến đổi khí hậu đến sức khoẻ sinh sản

Hiệu quả của phác đồ PPOS trong kích thích buồng trứng
Ảnh hưởng của bất thường acrosome và không bào ở tinh trùng đến ...


























