Tin chuyên ngành
on Tuesday 18-05-2021 8:33am
Danh mục: Vô sinh & hỗ trợ sinh sản
Nguyễn Thị Minh Phượng, Chuyên viên phôi học – IVFMD Tân Bình
Điều trị hỗ trợ sinh sản (ART) là một trong những hướng tiếp cận hiệu quả dành cho bệnh nhân vô sinh hiện nay. Theo báo cáo của Hội Sinh sản người và Phôi học châu Âu (ESHRE) và Trung tâm kiểm soát và phòng chống dịch bệnh Hoa Kỳ (CDC) tỷ lệ mang thai thành công trên mỗi chu kỳ điều trị ART trong năm 2014 và 2016 lần lượt là khoảng 21% và 22% (De Geyter và cs., 2018; CDC, 2018). Một trong những lý do giải thích cho tỷ lệ thấp này được cho là do chất lượng tinh trùng. Sự hiện diện của tinh trùng hư hỏng DNA có thể làm giảm kết quả điều trị của bệnh nhân. Nhằm đảm bảo chất lượng tinh trùng được sử dụng trong các kỹ thuật hỗ trợ sinh sản (HTSS), nhiều phương pháp chọn lọc tinh trùng mới đã ra đời nhằm mục tiêu cải thiện kết quả lâm sàng của bệnh nhân. Mục tiêu của bài viết này là nhằm đưa ra cái nhìn tổng quan cũng như tiềm năng phát triển của các phương pháp này.
Tại sao việc chọn lựa tinh trùng quan trọng trong một chu kỳ điều trị HTSS?
Như chúng ta đã biết, trong số hàng triệu tinh trùng chỉ có một số nhỏ khoảng vài trăm tinh trùng có thể đến được ống dẫn trứng để gặp noãn và thụ tinh (Williams và cs., 1993). Đây là một quá trình chọn lọc in vivo, chỉ có những tinh trùng trưởng thành, có khả năng thụ tinh cao nhất mới có cơ hội thụ tinh với noãn. Đối với thụ tinh trong ống nghiệm, do các tiện lợi cũng như hiệu quả tương tự IVF cổ điển, ICSI dần trở thành kỹ thuật được lựa chọn nhiều nhất, tuy nhiên lại vô tình loại bỏ đi sự chọn lọc cuối cùng như trong tự nhiên. Tính toàn vẹn DNA tinh trùng là một trong những thông số được nhiều nhà khoa học quan tâm. Nhiều nghiên cứu đã chứng minh rằng sự phân mảnh DNA tinh trùng sẽ làm chậm quá trình phát triển của phôi, tỷ lệ nghịch với xác suất thành công của ART (Esbert và cs., 2018; Simon và cs., 2017). Từ những dẫn chứng trên có thể thấy để có một chu kỳ điều trị HTSS thành công, việc lựa chọn tinh trùng đóng vai trò vô cùng quan trọng.
Phương pháp chọn lọc tinh trùng phổ biến
Các kỹ thuật chuẩn bị tinh trùng bên cạnh việc loại bỏ tinh trùng chất lượng thấp cũng cần phải loại bỏ tinh dịch và các tế bào khác như bạch cầu, vi khuẩn, các chất gây độc cho tế bào hay các gốc oxy hóa tự do (ROS)… Hai phương pháp được sử dụng phổ biến hiện nay là kỹ thuật Swim-up (SU) và Density Gradient Centrifugation (DGC).
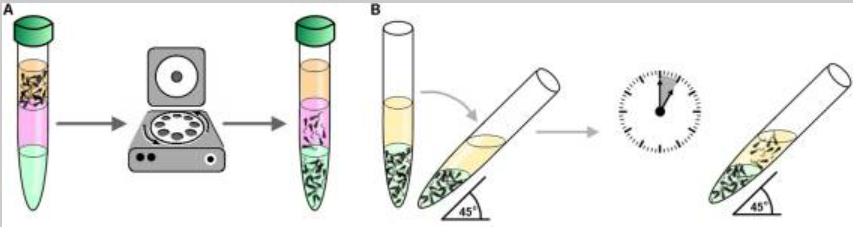
SU được mô tả lần đầu tiên bởi Mahadevan và Baker (1984) với nguyên tắc tinh trùng di động tốt có khả năng di chuyển ra khỏi tinh dịch vào môi trường cấy, trong khi đó DGC dựa vào tỷ trọng khác nhau sẽ bị giữ lại ở những lớp môi trường lọc có nồng độ khác nhau được tạo thành từ các hạt silica dưới tác động của lực ly tâm.
Các nghiên cứu đã đưa ra những kết quả trái ngược nhau về hiệu quả của hai phương pháp này trong IVF/ICSI. Trong nghiên cứu Wang và cộng sự (2014), phương pháp DGC làm giảm phân mảnh DNA ở tinh trùng ở nhóm bệnh nhân oligozoospermia và asthenozoospermia, ngoài ra khi so sánh tỷ lệ mang thai SU cho tỷ lệ thấp hơn (7 so với 18%). Điều này cũng được thể hiện trong nghiên cứu của Karamahmutogu và cộng sự (2014). Ngược lại, nghiên cứu của Oguz và cộng sự (2018) lại cho thấy SU tăng chất lượng mẫu cũng như giảm phân mảnh DNA ở những bệnh nhân vô sinh do yếu tố nam nhẹ và chưa rõ nguyên nhân.
SU và DGC đều là những phương pháp được áp dụng phổ biến tại các trung tâm hỗ trợ sinh sản. Nguyên lý của cả hai phương pháp đều là lựa chọn tinh trùng dựa trên sự di chuyển của tinh trùng nhưng điều này không có nghĩa là tất cả các tinh trùng di động tốt đều có chất lượng cao. Ngoài ra, các phương pháp này cũng không thể áp dụng với các trường hợp đặc biệt như tinh trùng bất động hoàn toàn hay tinh trùng từ phẫu thuật. Bên cạnh đó, bước ly tâm của hai phương pháp này cũng tăng tạo ROS (các gốc oxy hoá tự do) - một tác nhân ảnh hưởng bất lợi đến chất lượng tinh trùng (Henkel và Schill, 2003). Do đó, cần có các phương pháp chọn lọc dựa trên các đặc điểm tinh trùng có sự tương quan cao với các kết quả lâm sàng hơn.
MỘT SỐ XU HƯỚNG MỚI TRONG LĨNH VỰC LỰA CHỌN TINH TRÙNG
Dựa trên đặc tính màng
Annexin V Magnetic Activated Cell Sorting (AV-MACS)
MACS là phương pháp chọn lựa tinh trùng dựa trên các kháng nguyên bề mặt tinh trùng (Plouffe và cs., 2015). Trong cơ thể người, khi một tế bào tổn thương thì chúng sẽ đi vào con đường “chết theo chương trình” (apoptosis), tinh trùng cũng không ngoại lệ. Khi lượng phân mảnh DNA tinh trùng lớn quá trình apoptosis sẽ được diễn ra, kháng nguyên phosphatidylserine (PS) nằm trong màng bào tương sẽ được bộc lộ ra bên ngoài. Dựa trên cơ sở này các hạt nano từ tính được phủ Annexin V- phân tử có ái lực cao với PS sẽ có tác dụng giữ lại các tinh trùng chết trên cột MACS dưới tác động của từ trường mạnh (Gil và cs., 2013).
Việc sử dụng MACS để chọn lọc tinh trùng trong thực hành lâm sàng ở người được báo cáo lần đầu tiên năm 2001. Hiệu quả chọn lọc tinh trùng có DNA toàn vẹn của phương pháp này đã được rất nhiều nhà khoa học công nhận trên nhiều nhóm đối tượng (Zahedi và cs., 2013; Degheidy và cs., 2015). Việc kết hợp các phương pháp lọc rửa thông thường và MACS cũng rất được quan tâm với mục đích chính là giảm tinh trùng di động có bất thường về nhiễm sắc thể. Điều này đã được báo cáo trong nghiên cứu của Esbert và cộng sự (2017) khi kết hợp hai phương pháp DGC và MACS. Hầu hết các nghiên cứu đều nhận thấy ở nhóm bệnh nhân vô sinh do yếu tố nam sự kết hợp giữa DGC và MACS đem lại một số lợi ích về mặt thai lâm sàng, tuy nhiên, khá ít nghiên cứu đề cập đến tỷ lệ trẻ sinh sống. Để có thể chứng minh tiện ích của MACS đối với thực hành lâm sàng cần phải có thêm nhiều nghiên cứu lớn và đánh giá các biến số khác nhau.
Liên kết Hyaluronic Acid (HA)
Hyaluronic acid là một trong những thành phần quan trọng trên màng tế bào noãn và chỉ những tinh trùng trưởng thành mới có thể liên kết với nó. Nghiên cứu của Parmegiani và cộng sự (2010) đã cho thấy tinh trùng gắn kết vào HA có tỷ lệ phân mảnh DNA thấp và có cấu trúc nhân bình thường so với tinh trùng trong PVP (Parmegiani et al, 2010). Hiện nay, có hai dạng chế phẩm có chứa HA trên thị trường, một là đĩa petri đã được phủ một lớp HA lên trên (PICSI Sperm Selection Device; MidAtlantic Diagnostic) và chế phẩm còn lại ở dạng môi trường có chứa HA (Sperm Slow; MediCult). Các kết quả của phương pháp này vẫn còn đang gặp rất nhiều tranh cãi, điều đó đặt ra một câu hỏi rằng hiệu quả giữa các nhóm vô sinh do yếu tố nam có khác nhau hay không? Nghiên cứu Erberelli và cộng sự (2017) cho thấy rằng kết quả có thể tốt hơn đối với nhóm bệnh nhân có tinh trùng dị dạng. Tuy nhiên, ở các nhóm còn lại vẫn chưa nhận thấy sự cải thiện đáng kể khi sử dụng phương pháp này.
DGC-Zeta
Phương pháp này lựa chọn tinh trùng dựa trên điện tích màng. Theo Rivera và cộng sự (2017), những tinh trùng chưa trưởng thành có DNA không toàn vẹn sẽ tích điện dương hơn, những tinh trùng trưởng thành lại có biểu hiện cấu trúc glycocalyx cao hơn nên sẽ mang điện tích âm hơn. Khi tạo điện dương lên thành ống nghiệm, thì những tinh trùng có điện tích âm hơn sẽ bám lên thành ống nghiệm và những tinh trùng có điện tích thấp hơn sẽ không gắn lên thành và lơ lửng trong môi trường. Người ta sẽ tiến hành loại bỏ những tinh trùng không gắn kết và thu những tinh trùng gắn kết là những tinh trùng trưởng thành và có DNA toàn vẹn hơn (Ainsworth và cs., 2005). Khi so sánh về tính toàn vẹn DNA tinh trùng, phôi chất lượng tốt, tỷ lệ có thai đều cho thấy DGC-Zeta có kết quả tốt hơn DGC, MACS (Zarei và cs., 2012; Zahedi và cs., 2013). Mặc dù tiềm năng của phương pháp này đã được nhận thấy nhưng số lượng nghiên cứu vẫn còn khá hạn chế.
Lựa chọn tinh trùng dựa trên sự di chuyển của tinh trùng (Vi dòng chảy-Microfluidic)
Kỹ thuật này liên quan đến kiểm soát dòng chất lỏng bên trong các kênh có thể tích nhỏ được phát triển từ khoảng đầu những năm 90 của thế kỷ XX. Dựa vào sự chênh lệch nồng độ, tinh trùng sẽ đi từ nơi có nồng độ cao sang nơi có nồng độ thấp. Những tinh trùng có độ di động tốt có khuynh hướng tách khỏi dòng chảy có chứa tinh trùng yếu, bất động cũng như nhiều thành phần khác. Năm 2003, Cho và Schuster đã ứng dụng kỹ thuật vi dòng chảy vào quy trình phân lập tinh trùng di động trên tinh dịch người. Nosrati và cộng sự (2014) đã báo cáo sự cải thiện đáng kể khi sử dụng thiết bị vi dòng chảy bao gồm 500 vi kênh song song về sự phân mảnh DNA ở tinh trùng. Các kết quả tương tự khi so sánh với các phương pháp khác cũng được trình bày trong các nghiên cứu của Shirota và cộng sự (2016), Nagata và cộng sự (2018).
Lựa chọn tinh trùng dựa trên cơ chế hướng dẫn
Như đã biết, đường sinh dục nữ được coi là một cơ chế chọn lọc tinh trùng tự nhiên cho quá trình thụ tinh. Do đó, một chiến lược để phát triển các phương pháp chọn lọc tinh trùng mới sử dụng trong HTSS với nguyên tắc các cảm ứng của tinh trùng trong đường sinh dục nữ bên cạnh mục đích lựa chọn được các tinh trùng trưởng thành, độ di động tốt, phương pháp hỗ trợ quá trình khả năng hóa của tinh trùng. Việc kết hợp giữa đặc tính sinh học này với hệ thống vi dòng chảy đang được các nhà khoa học hi vọng sẽ là một xu hướng mới trong tương lai.
Cảm ứng dòng chảy
Định hướng bơi của tinh trùng người và chuột đều có xu hướng ngược chiều dòng chảy của chất lỏng (Miki và cs., 2013). Trên cơ sở đó, De Martin và cộng sự (2017) đã tiến hành nghiên cứu đầu tiên sử dụng cảm ứng dòng chảy nhằm chọn lọc tinh trùng. Kết quả cho thấy rằng độ nén của nhiễm sắc chất ở phương pháp này được cải thiện hơn so với trước lọc rửa và so với sử dụng phương pháp chọn lọc theo thang nồng độ. Cho đến hiện nay số lượng nghiên cứu về phương pháp này vẫn còn hạn chế.
Hóa hướng động (Chemotaxis)
Phức hợp tế bào cumulus-noãn (COC) có thể tiết ra progesterone (P4) như một chất dẫn dụ tinh trùng (Oren-Benaroya và cs., 2008). Dựa trên nguyên lý này, Gatica và cộng sự (2013) đã phát triển một hệ thống “Sperm Selection Assay” (SSA) có sự chênh lệch nồng độ P4 nhằm chọn lọc tinh trùng. Nhiều kết quả tích cực đã được báo cáo khi sử dụng phương pháp này như cải thiện về chất lượng mẫu (tăng tỷ lệ tinh trùng di động, hình dạng bình thường), giảm phân mảnh DNA tinh trùng (Li và cs., 2018). Tuy nhiên các hiệu quả trong việc cải thiện kết cục lâm sàng HTSS vẫn chưa được nghiên cứu.
Nhiệt hướng động
Các nghiên cứu về tinh trùng người cho thấy tinh trùng có khả năng cảm ứng với sự thay đổi nhiệt độ nhỏ hơn 1/1000C, chỉ những tinh trùng đã được khả năng hóa mới có thể di chuyển theo gradient nhiệt độ tại ống dẫn trứng (Bahat và cs., 2005). Các nghiên cứu trên mô hình động đã chứng minh chọn lọc tinh trùng dựa trên nguyên lý nhiệt hướng động là một phương pháp đầy tiềm năng giúp giảm phân mảnh DNA ở tinh trùng (Cerezalles và cs., 2018), tăng tỷ lệ phôi phân chia, phôi làm tổ (Mondal và cs., 2016). Tuy nhiên, tương tự như phương pháp chọn lọc nhờ hoá hướng động, vẫn chưa có công bố nào về cải thiện kết cục lâm sàng của phương pháp chọn lọc tinh trùng dựa trên nhiệt hướng động trong điều trị HTSS ở người.
.png)
Kết luận
Lựa chọn tinh trùng là một yếu tố quan trọng nhằm cải thiện tỷ lệ thành công của các kỹ thuật HTSS, đặc biệt là trong các trường hợp vô sinh do yếu tố nam. Tuy nhiên, cho đến nay vẫn chưa có một phương pháp tối ưu trong thực hành lâm sàng được xây dựng. Sự ra đời của các phương pháp chọn lọc tinh trùng mới đã mở ra nhiều tiềm năng lựa chọn tinh trùng để sử dụng trong HTSS.
Tài liệu tham khảo:
Điều trị hỗ trợ sinh sản (ART) là một trong những hướng tiếp cận hiệu quả dành cho bệnh nhân vô sinh hiện nay. Theo báo cáo của Hội Sinh sản người và Phôi học châu Âu (ESHRE) và Trung tâm kiểm soát và phòng chống dịch bệnh Hoa Kỳ (CDC) tỷ lệ mang thai thành công trên mỗi chu kỳ điều trị ART trong năm 2014 và 2016 lần lượt là khoảng 21% và 22% (De Geyter và cs., 2018; CDC, 2018). Một trong những lý do giải thích cho tỷ lệ thấp này được cho là do chất lượng tinh trùng. Sự hiện diện của tinh trùng hư hỏng DNA có thể làm giảm kết quả điều trị của bệnh nhân. Nhằm đảm bảo chất lượng tinh trùng được sử dụng trong các kỹ thuật hỗ trợ sinh sản (HTSS), nhiều phương pháp chọn lọc tinh trùng mới đã ra đời nhằm mục tiêu cải thiện kết quả lâm sàng của bệnh nhân. Mục tiêu của bài viết này là nhằm đưa ra cái nhìn tổng quan cũng như tiềm năng phát triển của các phương pháp này.
Tại sao việc chọn lựa tinh trùng quan trọng trong một chu kỳ điều trị HTSS?
Như chúng ta đã biết, trong số hàng triệu tinh trùng chỉ có một số nhỏ khoảng vài trăm tinh trùng có thể đến được ống dẫn trứng để gặp noãn và thụ tinh (Williams và cs., 1993). Đây là một quá trình chọn lọc in vivo, chỉ có những tinh trùng trưởng thành, có khả năng thụ tinh cao nhất mới có cơ hội thụ tinh với noãn. Đối với thụ tinh trong ống nghiệm, do các tiện lợi cũng như hiệu quả tương tự IVF cổ điển, ICSI dần trở thành kỹ thuật được lựa chọn nhiều nhất, tuy nhiên lại vô tình loại bỏ đi sự chọn lọc cuối cùng như trong tự nhiên. Tính toàn vẹn DNA tinh trùng là một trong những thông số được nhiều nhà khoa học quan tâm. Nhiều nghiên cứu đã chứng minh rằng sự phân mảnh DNA tinh trùng sẽ làm chậm quá trình phát triển của phôi, tỷ lệ nghịch với xác suất thành công của ART (Esbert và cs., 2018; Simon và cs., 2017). Từ những dẫn chứng trên có thể thấy để có một chu kỳ điều trị HTSS thành công, việc lựa chọn tinh trùng đóng vai trò vô cùng quan trọng.
Phương pháp chọn lọc tinh trùng phổ biến
Các kỹ thuật chuẩn bị tinh trùng bên cạnh việc loại bỏ tinh trùng chất lượng thấp cũng cần phải loại bỏ tinh dịch và các tế bào khác như bạch cầu, vi khuẩn, các chất gây độc cho tế bào hay các gốc oxy hóa tự do (ROS)… Hai phương pháp được sử dụng phổ biến hiện nay là kỹ thuật Swim-up (SU) và Density Gradient Centrifugation (DGC).
SU được mô tả lần đầu tiên bởi Mahadevan và Baker (1984) với nguyên tắc tinh trùng di động tốt có khả năng di chuyển ra khỏi tinh dịch vào môi trường cấy, trong khi đó DGC dựa vào tỷ trọng khác nhau sẽ bị giữ lại ở những lớp môi trường lọc có nồng độ khác nhau được tạo thành từ các hạt silica dưới tác động của lực ly tâm.
Các nghiên cứu đã đưa ra những kết quả trái ngược nhau về hiệu quả của hai phương pháp này trong IVF/ICSI. Trong nghiên cứu Wang và cộng sự (2014), phương pháp DGC làm giảm phân mảnh DNA ở tinh trùng ở nhóm bệnh nhân oligozoospermia và asthenozoospermia, ngoài ra khi so sánh tỷ lệ mang thai SU cho tỷ lệ thấp hơn (7 so với 18%). Điều này cũng được thể hiện trong nghiên cứu của Karamahmutogu và cộng sự (2014). Ngược lại, nghiên cứu của Oguz và cộng sự (2018) lại cho thấy SU tăng chất lượng mẫu cũng như giảm phân mảnh DNA ở những bệnh nhân vô sinh do yếu tố nam nhẹ và chưa rõ nguyên nhân.
SU và DGC đều là những phương pháp được áp dụng phổ biến tại các trung tâm hỗ trợ sinh sản. Nguyên lý của cả hai phương pháp đều là lựa chọn tinh trùng dựa trên sự di chuyển của tinh trùng nhưng điều này không có nghĩa là tất cả các tinh trùng di động tốt đều có chất lượng cao. Ngoài ra, các phương pháp này cũng không thể áp dụng với các trường hợp đặc biệt như tinh trùng bất động hoàn toàn hay tinh trùng từ phẫu thuật. Bên cạnh đó, bước ly tâm của hai phương pháp này cũng tăng tạo ROS (các gốc oxy hoá tự do) - một tác nhân ảnh hưởng bất lợi đến chất lượng tinh trùng (Henkel và Schill, 2003). Do đó, cần có các phương pháp chọn lọc dựa trên các đặc điểm tinh trùng có sự tương quan cao với các kết quả lâm sàng hơn.

Hình 1. Các phương pháp lọc rửa tinh trùng phổ biến
a. Density Gradient Centrifugation (DGC), b. Swim-up
a. Density Gradient Centrifugation (DGC), b. Swim-up
MỘT SỐ XU HƯỚNG MỚI TRONG LĨNH VỰC LỰA CHỌN TINH TRÙNG
Dựa trên đặc tính màng
Annexin V Magnetic Activated Cell Sorting (AV-MACS)
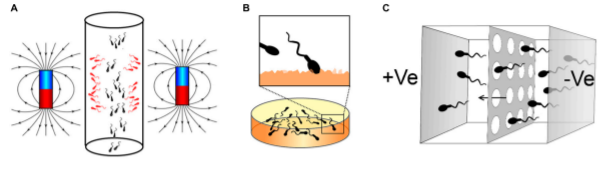
MACS là phương pháp chọn lựa tinh trùng dựa trên các kháng nguyên bề mặt tinh trùng (Plouffe và cs., 2015). Trong cơ thể người, khi một tế bào tổn thương thì chúng sẽ đi vào con đường “chết theo chương trình” (apoptosis), tinh trùng cũng không ngoại lệ. Khi lượng phân mảnh DNA tinh trùng lớn quá trình apoptosis sẽ được diễn ra, kháng nguyên phosphatidylserine (PS) nằm trong màng bào tương sẽ được bộc lộ ra bên ngoài. Dựa trên cơ sở này các hạt nano từ tính được phủ Annexin V- phân tử có ái lực cao với PS sẽ có tác dụng giữ lại các tinh trùng chết trên cột MACS dưới tác động của từ trường mạnh (Gil và cs., 2013).
Việc sử dụng MACS để chọn lọc tinh trùng trong thực hành lâm sàng ở người được báo cáo lần đầu tiên năm 2001. Hiệu quả chọn lọc tinh trùng có DNA toàn vẹn của phương pháp này đã được rất nhiều nhà khoa học công nhận trên nhiều nhóm đối tượng (Zahedi và cs., 2013; Degheidy và cs., 2015). Việc kết hợp các phương pháp lọc rửa thông thường và MACS cũng rất được quan tâm với mục đích chính là giảm tinh trùng di động có bất thường về nhiễm sắc thể. Điều này đã được báo cáo trong nghiên cứu của Esbert và cộng sự (2017) khi kết hợp hai phương pháp DGC và MACS. Hầu hết các nghiên cứu đều nhận thấy ở nhóm bệnh nhân vô sinh do yếu tố nam sự kết hợp giữa DGC và MACS đem lại một số lợi ích về mặt thai lâm sàng, tuy nhiên, khá ít nghiên cứu đề cập đến tỷ lệ trẻ sinh sống. Để có thể chứng minh tiện ích của MACS đối với thực hành lâm sàng cần phải có thêm nhiều nghiên cứu lớn và đánh giá các biến số khác nhau.
Liên kết Hyaluronic Acid (HA)
Hyaluronic acid là một trong những thành phần quan trọng trên màng tế bào noãn và chỉ những tinh trùng trưởng thành mới có thể liên kết với nó. Nghiên cứu của Parmegiani và cộng sự (2010) đã cho thấy tinh trùng gắn kết vào HA có tỷ lệ phân mảnh DNA thấp và có cấu trúc nhân bình thường so với tinh trùng trong PVP (Parmegiani et al, 2010). Hiện nay, có hai dạng chế phẩm có chứa HA trên thị trường, một là đĩa petri đã được phủ một lớp HA lên trên (PICSI Sperm Selection Device; MidAtlantic Diagnostic) và chế phẩm còn lại ở dạng môi trường có chứa HA (Sperm Slow; MediCult). Các kết quả của phương pháp này vẫn còn đang gặp rất nhiều tranh cãi, điều đó đặt ra một câu hỏi rằng hiệu quả giữa các nhóm vô sinh do yếu tố nam có khác nhau hay không? Nghiên cứu Erberelli và cộng sự (2017) cho thấy rằng kết quả có thể tốt hơn đối với nhóm bệnh nhân có tinh trùng dị dạng. Tuy nhiên, ở các nhóm còn lại vẫn chưa nhận thấy sự cải thiện đáng kể khi sử dụng phương pháp này.
DGC-Zeta
Phương pháp này lựa chọn tinh trùng dựa trên điện tích màng. Theo Rivera và cộng sự (2017), những tinh trùng chưa trưởng thành có DNA không toàn vẹn sẽ tích điện dương hơn, những tinh trùng trưởng thành lại có biểu hiện cấu trúc glycocalyx cao hơn nên sẽ mang điện tích âm hơn. Khi tạo điện dương lên thành ống nghiệm, thì những tinh trùng có điện tích âm hơn sẽ bám lên thành ống nghiệm và những tinh trùng có điện tích thấp hơn sẽ không gắn lên thành và lơ lửng trong môi trường. Người ta sẽ tiến hành loại bỏ những tinh trùng không gắn kết và thu những tinh trùng gắn kết là những tinh trùng trưởng thành và có DNA toàn vẹn hơn (Ainsworth và cs., 2005). Khi so sánh về tính toàn vẹn DNA tinh trùng, phôi chất lượng tốt, tỷ lệ có thai đều cho thấy DGC-Zeta có kết quả tốt hơn DGC, MACS (Zarei và cs., 2012; Zahedi và cs., 2013). Mặc dù tiềm năng của phương pháp này đã được nhận thấy nhưng số lượng nghiên cứu vẫn còn khá hạn chế.

Hình 2. Một số phương pháp chọn lọc tinh trùng dựa trên đặc điểm màng:
a. MACS, b. HA binding, c. Zeta
a. MACS, b. HA binding, c. Zeta
Lựa chọn tinh trùng dựa trên sự di chuyển của tinh trùng (Vi dòng chảy-Microfluidic)
Kỹ thuật này liên quan đến kiểm soát dòng chất lỏng bên trong các kênh có thể tích nhỏ được phát triển từ khoảng đầu những năm 90 của thế kỷ XX. Dựa vào sự chênh lệch nồng độ, tinh trùng sẽ đi từ nơi có nồng độ cao sang nơi có nồng độ thấp. Những tinh trùng có độ di động tốt có khuynh hướng tách khỏi dòng chảy có chứa tinh trùng yếu, bất động cũng như nhiều thành phần khác. Năm 2003, Cho và Schuster đã ứng dụng kỹ thuật vi dòng chảy vào quy trình phân lập tinh trùng di động trên tinh dịch người. Nosrati và cộng sự (2014) đã báo cáo sự cải thiện đáng kể khi sử dụng thiết bị vi dòng chảy bao gồm 500 vi kênh song song về sự phân mảnh DNA ở tinh trùng. Các kết quả tương tự khi so sánh với các phương pháp khác cũng được trình bày trong các nghiên cứu của Shirota và cộng sự (2016), Nagata và cộng sự (2018).
Lựa chọn tinh trùng dựa trên cơ chế hướng dẫn
Như đã biết, đường sinh dục nữ được coi là một cơ chế chọn lọc tinh trùng tự nhiên cho quá trình thụ tinh. Do đó, một chiến lược để phát triển các phương pháp chọn lọc tinh trùng mới sử dụng trong HTSS với nguyên tắc các cảm ứng của tinh trùng trong đường sinh dục nữ bên cạnh mục đích lựa chọn được các tinh trùng trưởng thành, độ di động tốt, phương pháp hỗ trợ quá trình khả năng hóa của tinh trùng. Việc kết hợp giữa đặc tính sinh học này với hệ thống vi dòng chảy đang được các nhà khoa học hi vọng sẽ là một xu hướng mới trong tương lai.
Cảm ứng dòng chảy
Định hướng bơi của tinh trùng người và chuột đều có xu hướng ngược chiều dòng chảy của chất lỏng (Miki và cs., 2013). Trên cơ sở đó, De Martin và cộng sự (2017) đã tiến hành nghiên cứu đầu tiên sử dụng cảm ứng dòng chảy nhằm chọn lọc tinh trùng. Kết quả cho thấy rằng độ nén của nhiễm sắc chất ở phương pháp này được cải thiện hơn so với trước lọc rửa và so với sử dụng phương pháp chọn lọc theo thang nồng độ. Cho đến hiện nay số lượng nghiên cứu về phương pháp này vẫn còn hạn chế.
Hóa hướng động (Chemotaxis)
Phức hợp tế bào cumulus-noãn (COC) có thể tiết ra progesterone (P4) như một chất dẫn dụ tinh trùng (Oren-Benaroya và cs., 2008). Dựa trên nguyên lý này, Gatica và cộng sự (2013) đã phát triển một hệ thống “Sperm Selection Assay” (SSA) có sự chênh lệch nồng độ P4 nhằm chọn lọc tinh trùng. Nhiều kết quả tích cực đã được báo cáo khi sử dụng phương pháp này như cải thiện về chất lượng mẫu (tăng tỷ lệ tinh trùng di động, hình dạng bình thường), giảm phân mảnh DNA tinh trùng (Li và cs., 2018). Tuy nhiên các hiệu quả trong việc cải thiện kết cục lâm sàng HTSS vẫn chưa được nghiên cứu.
Nhiệt hướng động
Các nghiên cứu về tinh trùng người cho thấy tinh trùng có khả năng cảm ứng với sự thay đổi nhiệt độ nhỏ hơn 1/1000C, chỉ những tinh trùng đã được khả năng hóa mới có thể di chuyển theo gradient nhiệt độ tại ống dẫn trứng (Bahat và cs., 2005). Các nghiên cứu trên mô hình động đã chứng minh chọn lọc tinh trùng dựa trên nguyên lý nhiệt hướng động là một phương pháp đầy tiềm năng giúp giảm phân mảnh DNA ở tinh trùng (Cerezalles và cs., 2018), tăng tỷ lệ phôi phân chia, phôi làm tổ (Mondal và cs., 2016). Tuy nhiên, tương tự như phương pháp chọn lọc nhờ hoá hướng động, vẫn chưa có công bố nào về cải thiện kết cục lâm sàng của phương pháp chọn lọc tinh trùng dựa trên nhiệt hướng động trong điều trị HTSS ở người.
.png)
Hình 3. Một số mô hình chọn lựa tinh trùng trên cơ chế cảm ứng của tinh trùng
a. Cảm ứng dòng chảy; b. Hóa hướng động; c. Nhiệt hướng động
a. Cảm ứng dòng chảy; b. Hóa hướng động; c. Nhiệt hướng động
Kết luận
Lựa chọn tinh trùng là một yếu tố quan trọng nhằm cải thiện tỷ lệ thành công của các kỹ thuật HTSS, đặc biệt là trong các trường hợp vô sinh do yếu tố nam. Tuy nhiên, cho đến nay vẫn chưa có một phương pháp tối ưu trong thực hành lâm sàng được xây dựng. Sự ra đời của các phương pháp chọn lọc tinh trùng mới đã mở ra nhiều tiềm năng lựa chọn tinh trùng để sử dụng trong HTSS.
Tài liệu tham khảo:
- De Geyter C., Calhaz-Jorge C., Kupka M. S., Wyns C., Mocanu E., Motrenko T., et al. (2018). ART in Europe, 2014: results generated from European registries by ESHRE. Hum. Reprod. 33 1586–1601. 10.1093/humrep/dey242
- CDC (2018). 2016 - National Summary Report - Assisted Reproductive Technology. Washington, DC: US Department of Health. Human Service.
- Simon L., Emery B. R., Carrell D. T. (2017b). Review: diagnosis and impact of sperm DNA alterations in assisted reproduction. Best Pract. Res. Clin. Obstet. Gynaecol. 44 38–56. 10.1016/j.bpobgyn.2017.07.003
- Mahadevan M., Baker G. (1984). “Assessment and preparation of semen for in vitro fertilization,” in Clinical In Vitro Fertilization, eds Wood C., Trounson A. (London: Springer), 83–97. 10.1007/978-1-4471-3317-9_7
- Sperm preparation for ART.Henkel RR, Schill WB. Reprod Biol Endocrinol. 2003 Nov 14; 1():108.
- Sperm selection using magnetic activated cell sorting (MACS) in assisted reproduction: a systematic review and meta-analysis Gil M, Sar-Shalom V, Melendez Sivira Y, Carreras R, Checa MA J Assist Reprod Genet. 2013 Apr; 30(4):479-85.
- High sperm DNA fragmentation delays human embryo kinetics when oocytes from young and healthy donors are microinjected. Esbert M, Pacheco A, Soares SR, Amorós D, Florensa M, Ballesteros A, Meseguer M Andrology. 2018 Sep; 6(5):697-706.
- Development of a novel electrophoretic system for the isolation of human spermatozoa. Ainsworth C, Nixon B, Aitken RJ Hum Reprod. 2005 Aug; 20(8):2261-70.
- "Physiologic ICSI": hyaluronic acid (HA) favors selection of spermatozoa without DNA fragmentation and with normal nucleus, resulting in improvement of embryo quality. Parmegiani L, Cognigni GE, Bernardi S, Troilo E, Ciampaglia W, Filicori M Fertil Steril. 2010 Feb; 93(2):598-604.
- Rheotaxis-based separation of sperm with progressive motility using a microfluidic corral system. Zaferani M, Cheong SH, Abbaspourrad A Proc Natl Acad Sci U S A. 2018 Aug 14; 115(33):8272-8277.
- Oseguera-López, Iván, et al. "Novel techniques of sperm selection for improving IVF and ICSI outcomes." Frontiers in cell and developmental biology 7 (2019): 298.
Các tin khác cùng chuyên mục:
TIN CẬP NHẬT
TIN CHUYÊN NGÀNH
LỊCH HỘI NGHỊ MỚI
Năm 2020
New World Saigon Hotel (Số 76 Lê Lai, Phường Bến Nghé, Quận 1, ...
Năm 2020
Caravelle Hotel Saigon, chiều thứ bảy 20.4 và chủ nhật 21.4.2024
Năm 2020
Khách sạn Caravelle Saigon, Chủ nhật 21.1.2024 (9:00 - 11:15)
GIỚI THIỆU SÁCH MỚI
Sách dự kiến phát hành đầu tháng 6.2024
Sách ra mắt ngày 9 . 3 . 2024 và gửi đến quý hội viên trước ...
Y học sinh sản số 68 ra mắt ngày 25 . 12 . 2023 và gửi đến quý ...
FACEBOOK






